Clear Sky Science · nl
Overdracht van het synechan-biosynthese- en reguleringspad maakt gesulfateerde polysacharidenproductie mogelijk in Synechococcus elongatus PCC 7942
Het omzetten van zonlicht in nuttige suikers
Gesulfateerde polysachariden zijn lange, op suiker gebaseerde moleculen met aangehechte sulfaatgroepen die hen bijzondere eigenschappen geven: ze kunnen veel water vasthouden, gels vormen en interacties aangaan met onze cellen die ze nuttig maken in medicijnen en cosmetica. Tegenwoordig komen veel van deze verbindingen uit dieren zoals varkens en haaien, of uit zeewieren, wat kosten, duurzaamheid en ethische bezwaren oproept. Deze studie onderzoekt of eenvoudige fotosynthetische microben — cyanobacteriën — kunnen worden herprogrammeerd om deze waardevolle moleculen rechtstreeks uit zonlicht en kooldioxide te produceren, wat wijst op duurzamere manieren om hoogwaardiger ingrediënten voor gezondheid en industrie te maken.
Waarom speciale suikers ertoe doen
Gesulfateerde polysachariden vervullen al stille maar belangrijke rollen in het dagelijks leven. Varianten zoals heparine helpen bloedstolling te voorkomen, en verwante moleculen worden toegevoegd aan huidcrèmes en oogdruppels vanwege hun kalmerende en waterbindende eigenschappen. Industriëel worden ze echter nog grotendeels gewonnen uit vee en mariene organismen, waardoor hun aanbod afhankelijk is van veeteelt en visserij. Chemisch sulfateren van suikers in een fabriek is mogelijk maar duur, vooral omdat de geactiveerde sulfaat-donor kostbaar is. Een levende cel die zowel de suikerketen als de sulfaatversieringen zelf kan samenstellen, met zonlicht als energiebron, zou een schoner en goedkoper alternatief kunnen bieden.
Cyanobacteriën als kleine suikerfabriekjes
Cyanobacteriën zijn microscopische, door zonlicht aangedreven organismen die vaak “blauwalgen” worden genoemd. Veel soorten omringen zichzelf van nature met complexe, slijmerige suikerlagen die gesulfateerde polysachariden kunnen bevatten. De auteurs ontdekten eerder een nieuw gesulfateerd exopolysacharide, genoemd synechan, geproduceerd door een modelcyanobacterie, Synechocystis sp. PCC 6803. Zij brachten de grote set genen in kaart — het xss-cluster — dat synechan opbouwt en reguleert wanneer het wordt geproduceerd. In de nieuwe studie vroegen ze of dit gehele genetische programma kon worden overgedragen naar een andere, goed bestudeerde cyanobacterie, Synechococcus elongatus PCC 7942, die normaal geen gesulfateerde polysachariden produceert. Als dat mogelijk was, zou het een proof of concept zijn dat zulke routes tussen microben kunnen worden verplaatst als modulaire gereedschapssets. 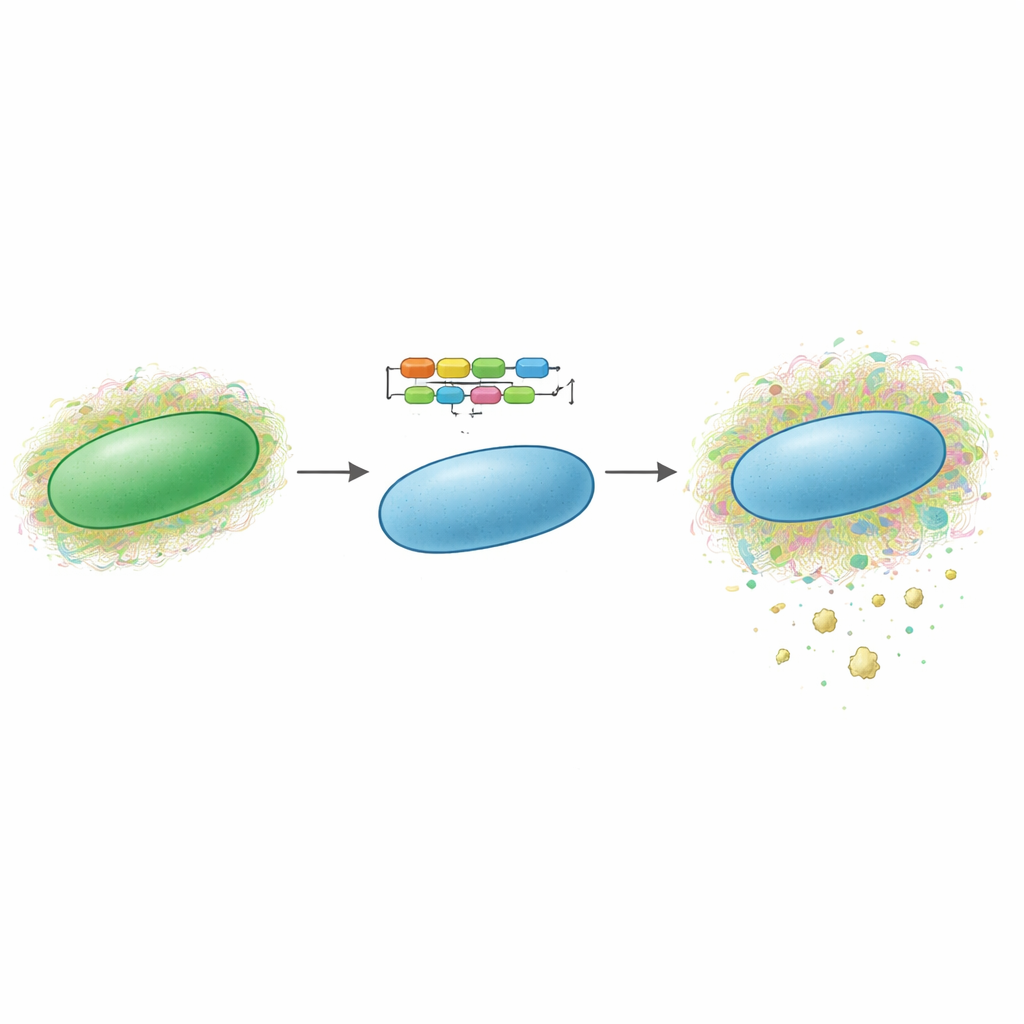
Een complex pad lenen en installeren
Om dit te bereiken verdeelde het team het synechan-systeem in twee hoofdonderdelen: de genen die het suikerpolymeer bouwen en afscheiden, en de genen die als aan‑/uit‑schakelaars voor deze bouwers fungeren. Ze plaatsten de biosynthesegenen in een shuttleplasmide en zetten één sleutelgen onder de controle van een sterke, induceerbare promotor, zodat een toegevoegd chemisch signaal (IPTG) de productie zou activeren. Vervolgens integreerden ze regulerende genen op een neutrale plek in het gastheurchromosoom, wederom onder induceerbare controle. Toen ze het systeem inschakelden, vertraagde de groei van de gemodificeerde stam sterk en begonnen de cellen samen te klonteren. Elektronenmicroscopie toonde lange vezelige materialen die het celoppervlak bedekten. Speciale kleuring die gesulfateerde polysachariden selectief zichtbaar maakt, liet duidelijke blauwe aggregaten buiten de cellen zien, en chemische assays bevestigden dat zowel celgebonden als vrijgegeven extracellulaire suikers toenamen vergeleken met controlegenen.
Hoe de nieuwe suiker er binnen en buiten uitziet
De onderzoekers vroegen vervolgens of het nieuwe materiaal echt op synechan leek. Door de polymeren af te breken en hun bouwstenen te analyseren, vonden ze dat de gemodificeerde cellen een gesulfateerd polysacharide produceerden bestaande uit glucose, galactose en mannose, met een sulfaatgehalte vergelijkbaar met het oorspronkelijke synechan maar met een andere suikerverhouding. In tegenstelling tot synechan, dat grotendeels in de omringende vloeistof wordt vrijgegeven, bleef veel van het nieuwe polymeer geassocieerd met het celoppervlak. Dit suggereert dat, hoewel de overgedragen genenset werkte, het niet de oorspronkelijke structuur perfect reproduceerde; in plaats daarvan vormden het metabolisme en de transportsystemen van de gastheer een "synechan‑achtig" product. Genoomwijde RNA-sequencing toonde aan dat het inschakelen van de xss-genen het cellengedrag wereldwijd herschakelde: stressgerelateerde factoren stegen, fotosynthetische en nutriëntopnamegenen daalden, en routes voor suiker‑ en zwavelverwerking werden aangepast, allemaal in lijn met cellen die middelen omleiden naar het maken van een energie-intensieve extracellulaire coating. 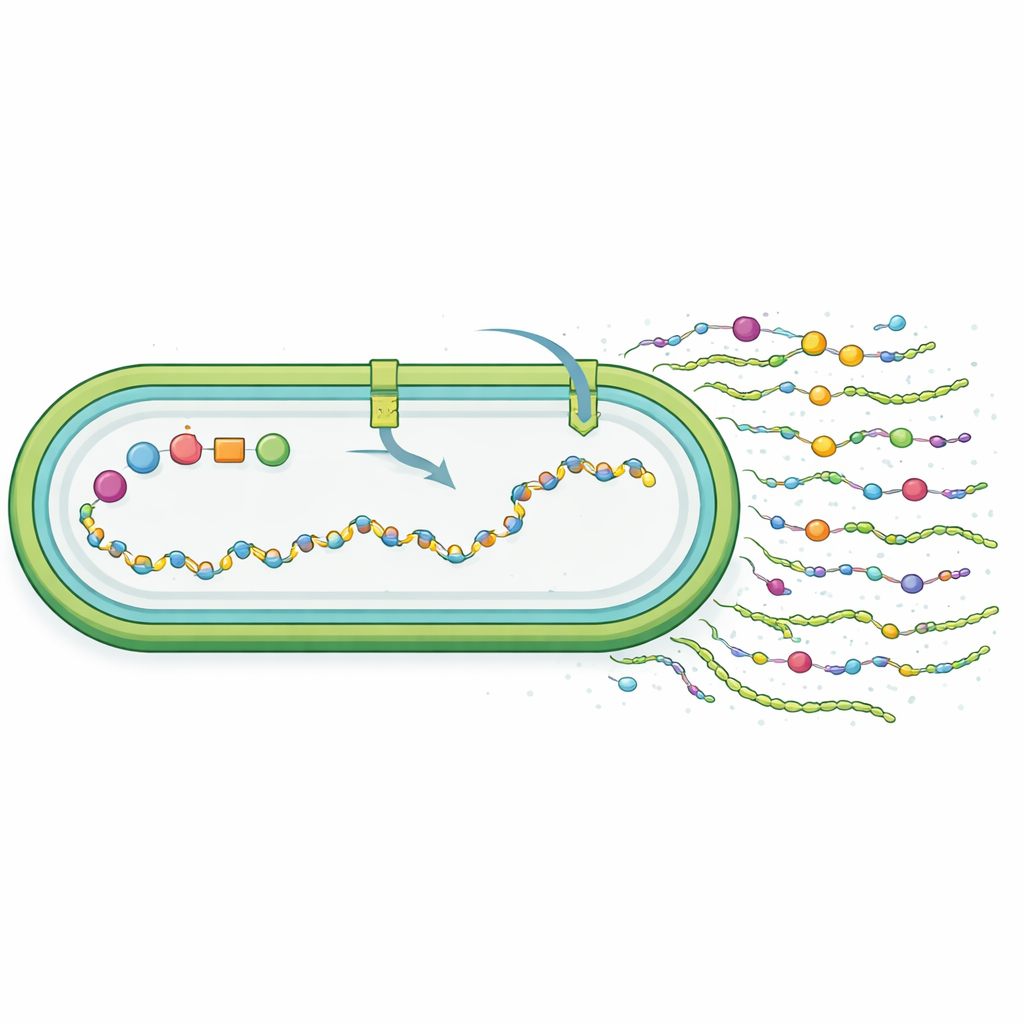
Bouwen aan groen moleculair ontwerp
Uit een populairwetenschappelijk perspectief is de kernboodschap dat wetenschappers met succes een groot, membraangebonden biosynthetisch apparaat — van de ene microbe naar een andere — hebben overgezet en de ontvanger een nieuw soort gesulfateerde suikerlaag hebben laten produceren. Het product is geen exacte kopie van het oorspronkelijke polymeer, maar die verschil is juist veelbelovend: het laat zien dat de fijne details van deze moleculen kunnen worden bijgestuurd door de gastheercel en het genetische ontwerp te veranderen. Op de lange termijn zou deze benadering "zonne‑aangedreven" microfabriekjes kunnen mogelijk maken die kooldioxide, licht en eenvoudige voedingsstoffen omzetten in bibliotheken van op maat gemaakte gesulfateerde polysachariden met specifieke texturen en biologische activiteiten, waardoor de afhankelijkheid van dierlijke bronnen afneemt en nieuwe wegen opengaan voor duurzame geneesmiddelen, cosmetica en functionele voedingsmiddelen.
Bronvermelding: Maeda, K., Ohdate, K., Sakamaki, Y. et al. Transfer of the synechan biosynthesis and regulatory pathway enables sulfated polysaccharide production in Synechococcus elongatus PCC 7942. Sci Rep 16, 13012 (2026). https://doi.org/10.1038/s41598-026-46439-4
Trefwoorden: gesulfateerde polysachariden, cyanobacteriën engineering, exopolysachariden, fotosynthetische bioproductie, synthetische biologie