Clear Sky Science · fr
Transfert de la biosynthèse et de la régulation de la voie synechan permet la production de polysaccharides sulfatés dans Synechococcus elongatus PCC 7942
Transformer la lumière du soleil en sucres utiles
Les polysaccharides sulfatés sont de longues molécules à base de sucres portant des groupes sulfate qui leur confèrent des propriétés remarquables : ils retiennent beaucoup d’eau, forment des gels et interagissent avec nos cellules de façons qui les rendent utiles en médecine et en cosmétique. Aujourd’hui, nombre de ces composés proviennent d’animaux comme le porc et le requin, ou d’algues marines, soulevant des questions de coût, de durabilité et d’éthique. Cette étude examine si des microbes photosynthétiques simples — des cyanobactéries — peuvent être reprogrammés pour fabriquer ces molécules précieuses directement à partir de la lumière et du dioxyde de carbone, ouvrant la voie à des modes de production plus durables d’ingrédients de grande valeur pour la santé et l’industrie.
Pourquoi ces sucres sont importants
Les polysaccharides sulfatés jouent déjà des rôles discrets mais importants dans la vie quotidienne. Des variantes comme l’héparine aident à prévenir la formation de caillots sanguins, et des molécules apparentées sont ajoutées aux crèmes et aux collyres pour leurs propriétés apaisantes et de rétention d’eau. Industriellement, ils sont toutefois encore majoritairement récoltés chez le bétail et les organismes marins, liant leur approvisionnement à l’élevage et à la pêche. Ajouter chimiquement des groupes sulfate aux sucres en usine est possible mais coûteux, principalement parce que la molécule donneuse de sulfate activée est onéreuse. Une cellule vivante capable d’assembler à la fois la chaîne de sucres et les décorations sulfate par elle‑même, en utilisant la lumière comme source d’énergie, offrirait une alternative plus propre et moins chère.
Les cyanobactéries, petites usines à sucre
Les cyanobactéries sont des organismes microscopiques alimentés par la lumière, souvent appelés « algues bleu‑vert ». De nombreuses espèces s’entourent naturellement de tapis sucrés complexes et visqueux qui peuvent inclure des polysaccharides sulfatés. Les auteurs ont précédemment découvert un nouvel exopolysaccharide sulfaté, baptisé synechan, produit par une cyanobactérie modèle, Synechocystis sp. PCC 6803. Ils ont cartographié le large ensemble de gènes — appelé le cluster xss — qui synthétise le synechan et contrôle sa production. Dans la nouvelle étude, ils se sont demandé si ce programme génétique complet pouvait être transféré dans une autre cyanobactérie bien étudiée, Synechococcus elongatus PCC 7942, qui ne produit normalement pas de polysaccharides sulfatés. Si oui, ce serait une preuve de concept que de telles voies peuvent être déplacées entre microbes comme des boîtes à outils modulaires. 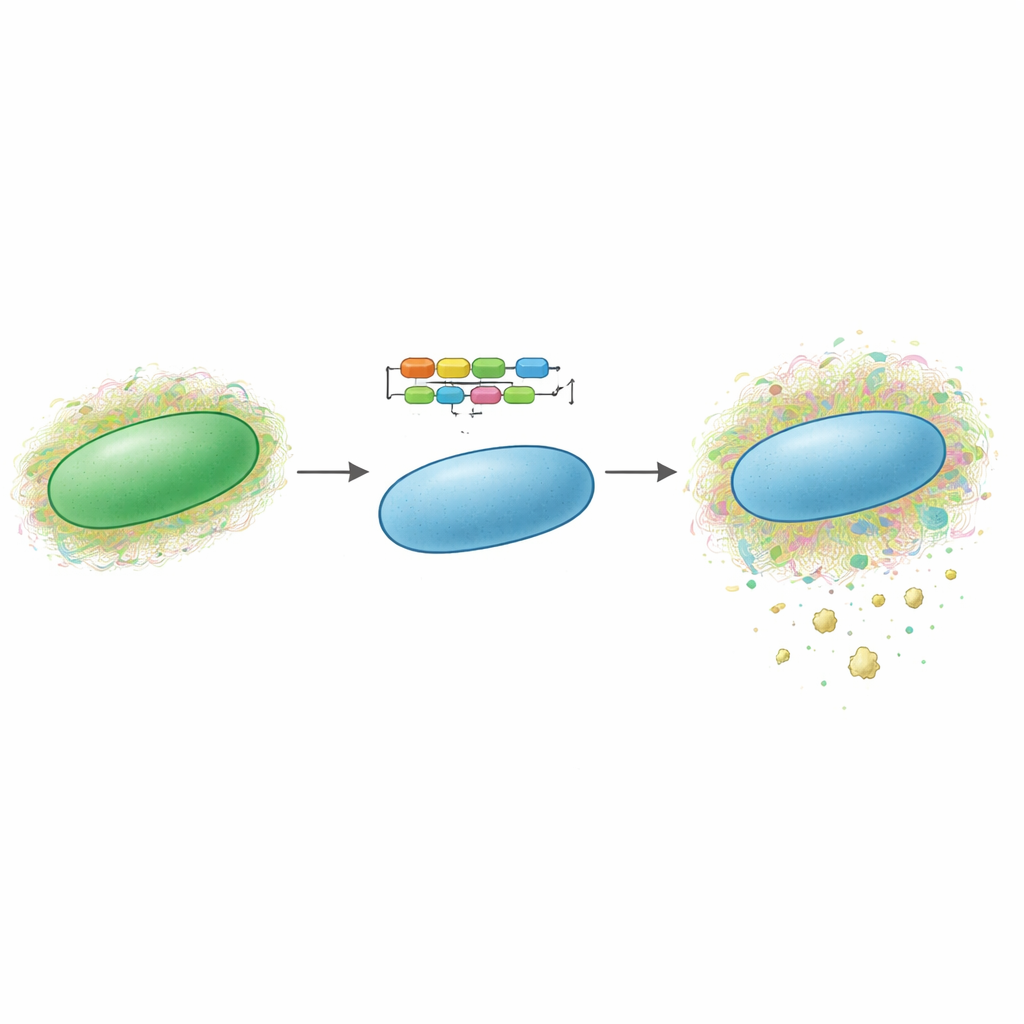
Emprunter et installer une voie complexe
Pour y parvenir, l’équipe a divisé le système synechan en deux parties principales : les gènes qui construisent et sécrètent le polymère glucidique, et les gènes qui jouent le rôle d’interrupteurs pour ces constructeurs. Ils ont inséré les gènes de biosynthèse dans un plasmide navette et placé un gène clé sous le contrôle d’un promoteur inductible et fort, de sorte qu’un signal chimique ajouté (IPTG) déclenche la production. Ils ont ensuite intégré les gènes régulateurs dans un site neutre du chromosome hôte, là encore sous contrôle inductible. Lorsqu’ils ont activé le système, la croissance de la souche modifiée a fortement ralenti et les cellules ont commencé à s’agglomérer. La microscopie électronique a révélé de longues fibres recouvrant les surfaces cellulaires. Des colorations spécifiques mettant en évidence les polysaccharides sulfatés ont montré de nets agrégats bleus à l’extérieur des cellules, et des tests chimiques ont confirmé que les sucres liés à la cellule et les sucres extraits dans le milieu extracellulaire augmentaient par rapport aux souches témoins.
À quoi ressemble le nouveau sucre, à l’intérieur comme à l’extérieur
Les chercheurs ont ensuite cherché à savoir si le nouveau matériau ressemblait vraiment au synechan. En décomposant les polymères et en analysant leurs unités constitutives, ils ont constaté que les cellules modifiées produisaient un polysaccharide sulfaté composé de glucose, galactose et mannose, avec une teneur en sulfate comparable au synechan natif mais un rapport des sucres différent. Contrairement au synechan, principalement libéré dans le liquide environnant, une grande partie du nouveau polymère est restée associée à la surface cellulaire. Cela suggère que, bien que l’ensemble génique transféré ait fonctionné, il n’a pas recréé parfaitement la structure d’origine ; le métabolisme et les systèmes de transport propres à l’hôte ont façonné un produit « de type synechan ». Le séquençage de l’ARN à l’échelle du génome a montré que l’activation des gènes xss reprogrammait globalement le comportement cellulaire : les facteurs liés au stress augmentaient, les gènes photosynthétiques et d’absorption des nutriments diminuaient, et les voies de gestion des sucres et du soufre étaient ajustées, cohérent avec une réorientation des ressources cellulaires vers la fabrication d’un manteau extracellulaire énergétiquement coûteux. 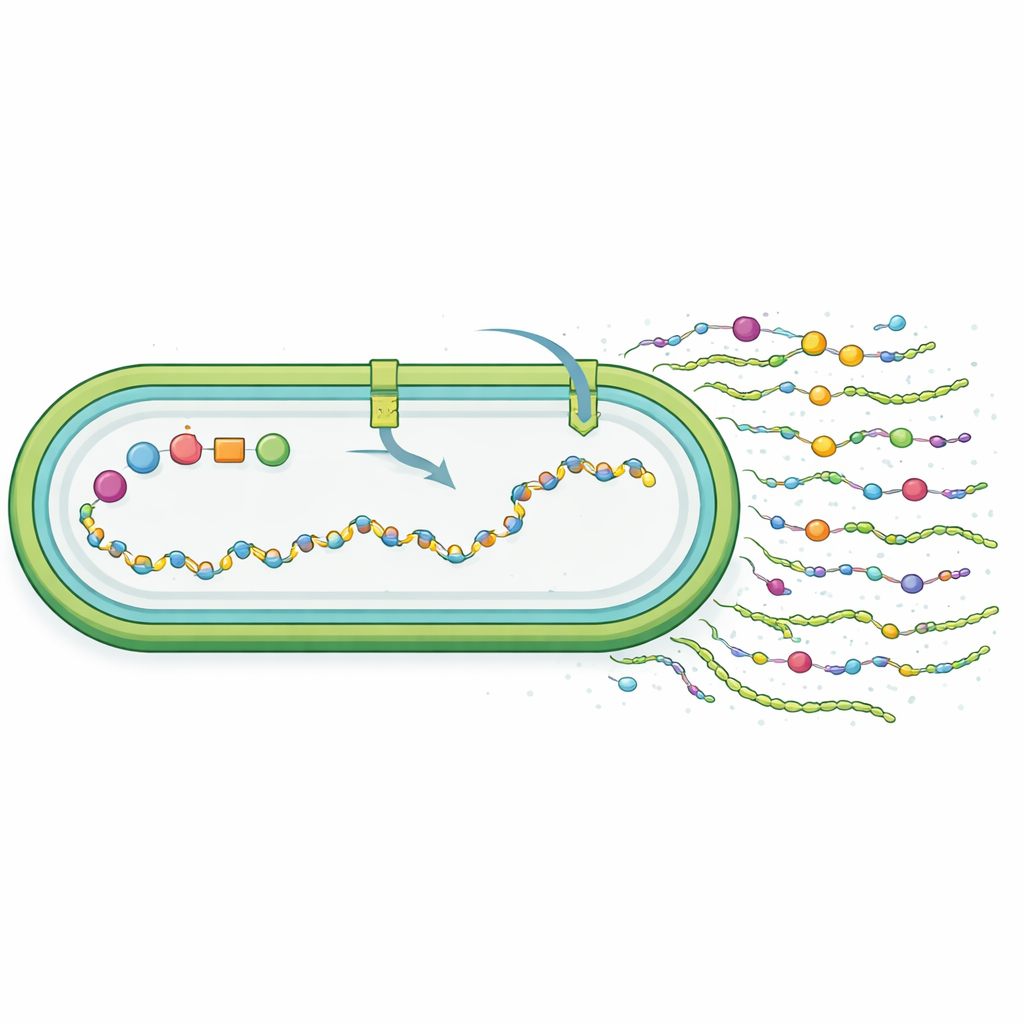
Vers une conception moléculaire plus durable
Du point de vue du grand public, le message central est que les scientifiques ont réussi à déplacer une grande machinerie biosynthétique associée à la membrane — d’un microbe à un autre — et ont obtenu chez le receveur la fabrication d’un nouveau type d’enveloppe glucidique sulfatée. Le produit n’est pas une copie exacte du polymère d’origine, mais cette différence est en réalité prometteuse : elle montre que les détails fins de ces molécules peuvent être ajustés en changeant l’hôte cellulaire et la conception génétique. À long terme, cette approche pourrait permettre des « usines microbiennes » alimentées par le soleil qui transforment le dioxyde de carbone, la lumière et des nutriments simples en bibliothèques de polysaccharides sulfatés sur mesure, aux textures et activités biologiques spécifiques, réduisant la dépendance aux sources animales et ouvrant de nouvelles voies pour des produits pharmaceutiques, cosmétiques et aliments fonctionnels plus durables.
Citation: Maeda, K., Ohdate, K., Sakamaki, Y. et al. Transfer of the synechan biosynthesis and regulatory pathway enables sulfated polysaccharide production in Synechococcus elongatus PCC 7942. Sci Rep 16, 13012 (2026). https://doi.org/10.1038/s41598-026-46439-4
Mots-clés: polysaccharides sulfatés, ingénierie des cyanobactéries, exopolysaccharides, bioproduction photosynthétique, biologie synthétique