Clear Sky Science · pt
Transferência da via biossintética e regulatória do synechan possibilita a produção de polissacarídeos sulfatados em Synechococcus elongatus PCC 7942
Transformando luz solar em açúcares úteis
Polissacarídeos sulfatados são moléculas longas à base de açúcar com grupos sulfato ligados, que lhes conferem propriedades notáveis: conseguem reter muita água, formar géis e interagir com nossas células de maneiras que os tornam úteis em medicamentos e cosméticos. Hoje, muitos desses compostos vêm de animais, como porcos e tubarões, ou de algas marinhas, o que levanta questões de custo, sustentabilidade e ética. Este estudo investiga se microrganismos fotossintéticos simples — cianobactérias — podem ser reprogramados para fabricar essas moléculas valiosas diretamente a partir da luz solar e do dióxido de carbono, apontando para maneiras mais sustentáveis de produzir ingredientes de alto valor para saúde e indústria.
Por que açúcares especiais importam
Polissacarídeos sulfatados já desempenham papéis discretos, mas importantes, no cotidiano. Variantes como a heparina ajudam a prevenir coágulos sanguíneos, e moléculas relacionadas são adicionadas a cremes para a pele e colírios por suas propriedades calmantes e de retenção de água. Industrialmente, porém, ainda são em grande parte extraídos de animais e organismos marinhos, vinculando seu suprimento à pecuária e à pesca. A sulfatação química de açúcares em fábrica é possível, mas cara, principalmente porque o doador de sulfato ativado é dispendioso. Uma célula viva que consiga montar tanto a cadeia de açúcares quanto as decorações de sulfato por conta própria, usando a luz do sol como fonte de energia, poderia oferecer uma alternativa mais limpa e barata.
Cianobactérias como pequenas fábricas de açúcar
Cianobactérias são organismos microscópicos movidos pela luz solar, frequentemente chamados de “algas azul‑verde.” Muitas espécies naturalmente se cercam de capas complexas e viscosas de açúcares que podem incluir polissacarídeos sulfatados. Os autores descobriram previamente um novo exopolissacarídeo sulfatado, batizado de synechan, produzido por uma cianobactéria modelo, Synechocystis sp. PCC 6803. Eles mapearam o grande conjunto de genes — chamado de cluster xss — que constrói o synechan e controla quando ele é produzido. No novo estudo, perguntaram se todo esse programa genético poderia ser transferido para outra cianobactéria bem caracterizada, Synechococcus elongatus PCC 7942, que normalmente não fabrica polissacarídeos sulfatados. Se sim, seria uma prova de conceito de que tais vias podem ser movidas entre micróbios como ferramentas modulares. 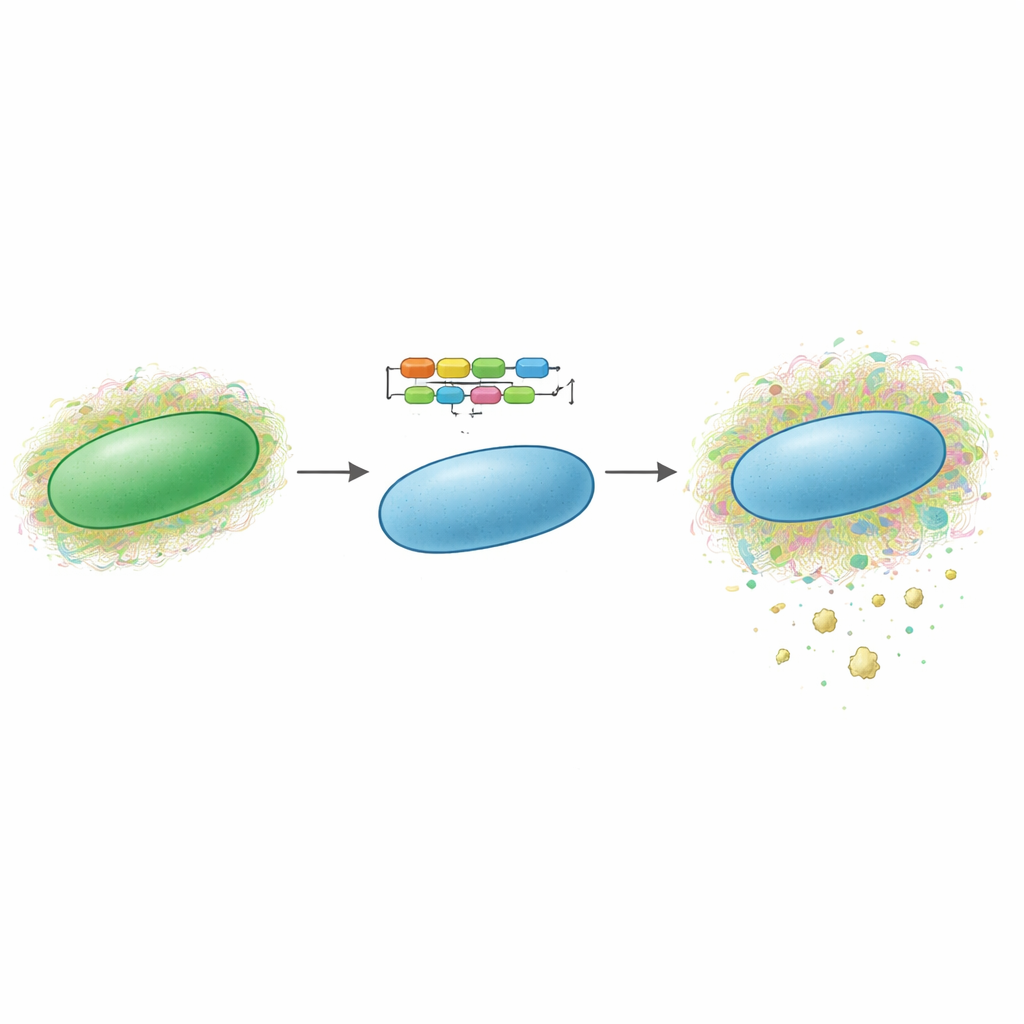
Pegando emprestado e instalando uma via complexa
Para conseguir isso, a equipe dividiu o sistema synechan em duas partes principais: os genes que constroem e secretam o polímero de açúcar, e os genes que atuam como interruptores liga‑desliga para esses construtores. Inseriram os genes de biossíntese em um plasmídeo shuttle e colocaram um gene-chave sob o controle de um promotor forte e indutível, de modo que um sinal químico adicionado (IPTG) disparasse a produção. Em seguida, integraram genes regulatórios em um local neutro do cromossomo hospedeiro, novamente sob controle indutível. Quando acionaram o sistema, o crescimento da estirpe engenheirada desacelerou drasticamente e as células começaram a aglomerar‑se. Microscopia eletrônica revelou material fibroso longo revestindo as superfícies celulares. Colorações especiais que destacam seletivamente polissacarídeos sulfatados mostraram agregados azuis claros fora das células, e ensaios químicos confirmaram que tanto os açúcares ligados às células quanto os liberados ao exterior aumentaram em comparação com as estirpes controle.
Como o novo açúcar aparece por dentro e por fora
Os pesquisadores então perguntaram se o novo material realmente se assemelhava ao synechan. Ao degradar os polímeros e analisar seus blocos construtores, descobriram que as células engenheiradas produziram um polissacarídeo sulfatado composto de glicose, galactose e manose, com um teor de sulfato semelhante ao synechan nativo, mas com uma proporção diferente de açúcares. Ao contrário do synechan, que é em grande parte liberado no líquido circundante, grande parte do novo polímero permaneceu associada à superfície celular. Isso sugere que, embora o conjunto gênico transferido funcionasse, ele não recriou perfeitamente a estrutura original; em vez disso, o próprio metabolismo e os sistemas de transporte do hospedeiro moldaram um produto “semelhante ao synechan”. Sequenciamento de RNA em escala genômica mostrou que ligar os genes xss reprogramou o comportamento celular globalmente: fatores relacionados ao estresse aumentaram, genes fotossintéticos e de captação de nutrientes diminuíram, e vias de manejo de açúcares e enxofre foram ajustadas, tudo consistente com células desviando recursos para fabricar uma cobertura extracelular que demanda muita energia. 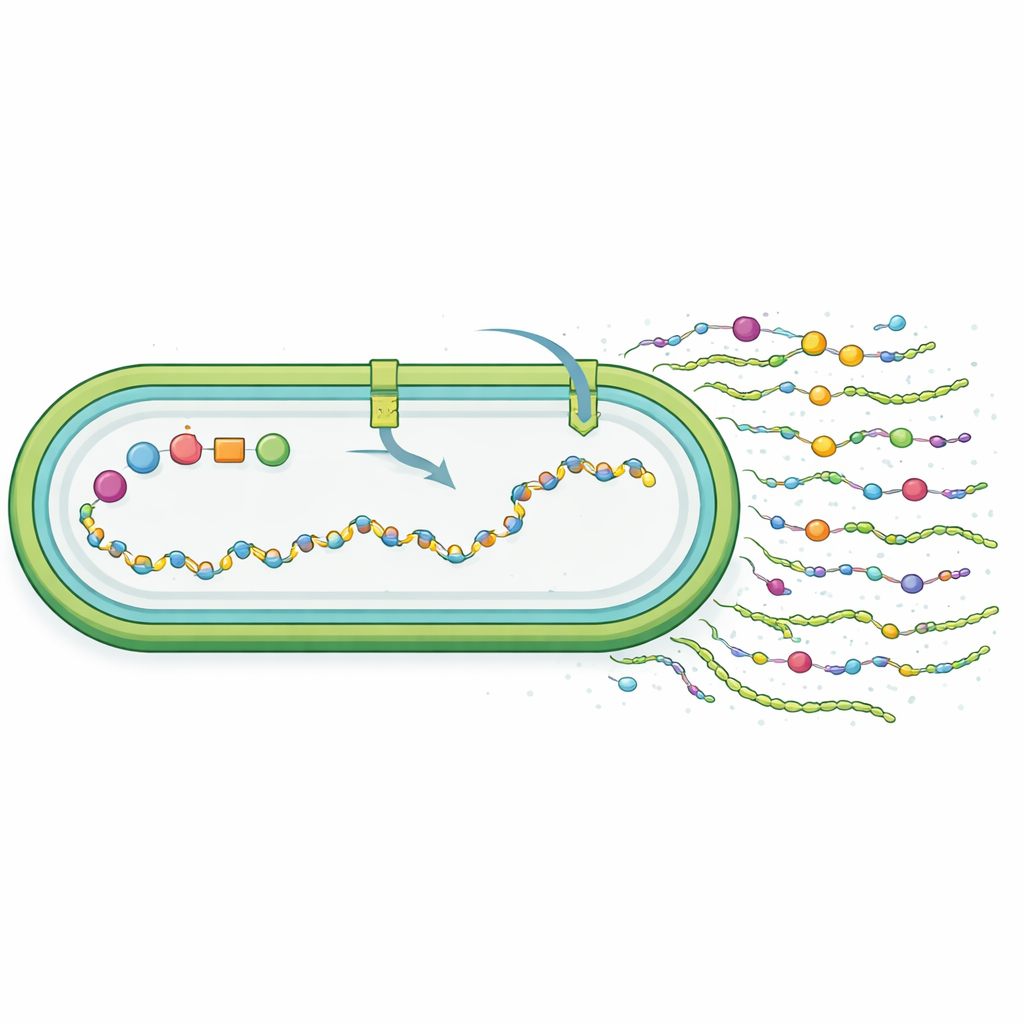
Construindo rumo ao design molecular verde
Do ponto de vista leigo, a mensagem central é que os cientistas moveram com sucesso uma grande máquina biossintética ligada à membrana — de um micro‑organismo para outro — e fizeram o receptor produzir um novo tipo de cobertura de açúcar sulfatado. O produto não é uma cópia exata do polímero original, mas essa diferença é na verdade promissora: mostra que os detalhes finos dessas moléculas podem ser ajustados alterando o hospedeiro celular e o projeto genético. A longo prazo, essa abordagem poderia viabilizar fábricas microbianas “movidas a energia solar” que transformem dióxido de carbono, luz e nutrientes simples em bibliotecas de polissacarídeos sulfatados sob medida, com texturas e atividades biológicas específicas, reduzindo a dependência de fontes animais e abrindo novos caminhos para farmacêuticos sustentáveis, cosméticos e alimentos funcionais.
Citação: Maeda, K., Ohdate, K., Sakamaki, Y. et al. Transfer of the synechan biosynthesis and regulatory pathway enables sulfated polysaccharide production in Synechococcus elongatus PCC 7942. Sci Rep 16, 13012 (2026). https://doi.org/10.1038/s41598-026-46439-4
Palavras-chave: polissacarídeos sulfatados, engenharia de cianobactérias, exopolissacarídeos, biomanufatura fotossintética, biologia sintética