Clear Sky Science · pl
Przeniesienie szlaku biosyntezy i regulacji synechanu umożliwia produkcję sulfowanych polisacharydów w Synechococcus elongatus PCC 7942
Przekształcanie światła słonecznego w przydatne cukry
Sulfowane polisacharydy to długie cząsteczki zbudowane z cukrów z przyłączonymi grupami siarczanowymi, które nadają im wyjątkowe właściwości: potrafią zatrzymywać dużą ilość wody, tworzyć żele i wchodzić w interakcje z komórkami w sposób przydatny w medycynie i kosmetyce. Obecnie wiele z tych związków pozyskuje się od zwierząt, takich jak świnie czy rekiny, albo z wodorostów, co budzi wątpliwości związane z kosztem, trwałością i etyką. W badaniu tym sprawdzono, czy proste, fotosyntetyzujące mikroorganizmy — cyjanobakterie — można przeprogramować tak, by wytwarzały te cenne związki bezpośrednio ze światła słonecznego i dwutlenku węgla, wskazując drogę do bardziej zrównoważonej produkcji składników wysokiej wartości dla zdrowia i przemysłu.
Dlaczego te szczególne cukry są ważne
Sulfowane polisacharydy odgrywają już dyskretną, lecz istotną rolę w codziennym życiu. Odmiany takie jak heparyna pomagają zapobiegać krzepnięciu krwi, a spokrewnione związki dodaje się do kremów i kropli do oczu ze względu na ich właściwości łagodzące i wiązania wody. Przemysłowo jednak nadal przede wszystkim pozyskuje się je z hodowli zwierząt i organizmów morskich, co uzależnia ich dostępność od rolnictwa i połowów. Chemiczne przyłączenie grup siarczanowych do cukrów w zakładzie jest możliwe, ale kosztowne, głównie dlatego, że aktywowany donor siarczanu jest drogi. Żywa komórka, która potrafi zarówno składać łańcuch cukrowy, jak i dołączać dekoracje siarczanowe, wykorzystując światło jako źródło energii, mogłaby stanowić czystsze i tańsze rozwiązanie.
Cyjanobakterie jako małe fabryki cukrów
Cyjanobakterie to mikroskopijne organizmy napędzane światłem, często określane jako „sinice”. Wiele gatunków naturalnie otacza się złożonym, śluzowatym płaszczem cukrowym, który może zawierać sulfowane polisacharydy. Autorzy wcześniej odkryli nowy sulfowany egzopolisacharyd nazwany synechan, produkowany przez modelową cyjanobakterię Synechocystis sp. PCC 6803. Zmapowali duży zestaw genów — nazwany klastrem xss — który buduje synechan i kontroluje jego produkcję. W nowym badaniu zapytali, czy cały ten program genetyczny da się przenieść do innej, dobrze zbadanej cyjanobakterii, Synechococcus elongatus PCC 7942, która normalnie nie wytwarza sulfowanych polisacharydów. Gdyby się to udało, byłoby dowodem, że takie szlaki można przenosić między mikroorganizmami jak modułowe narzędzia. 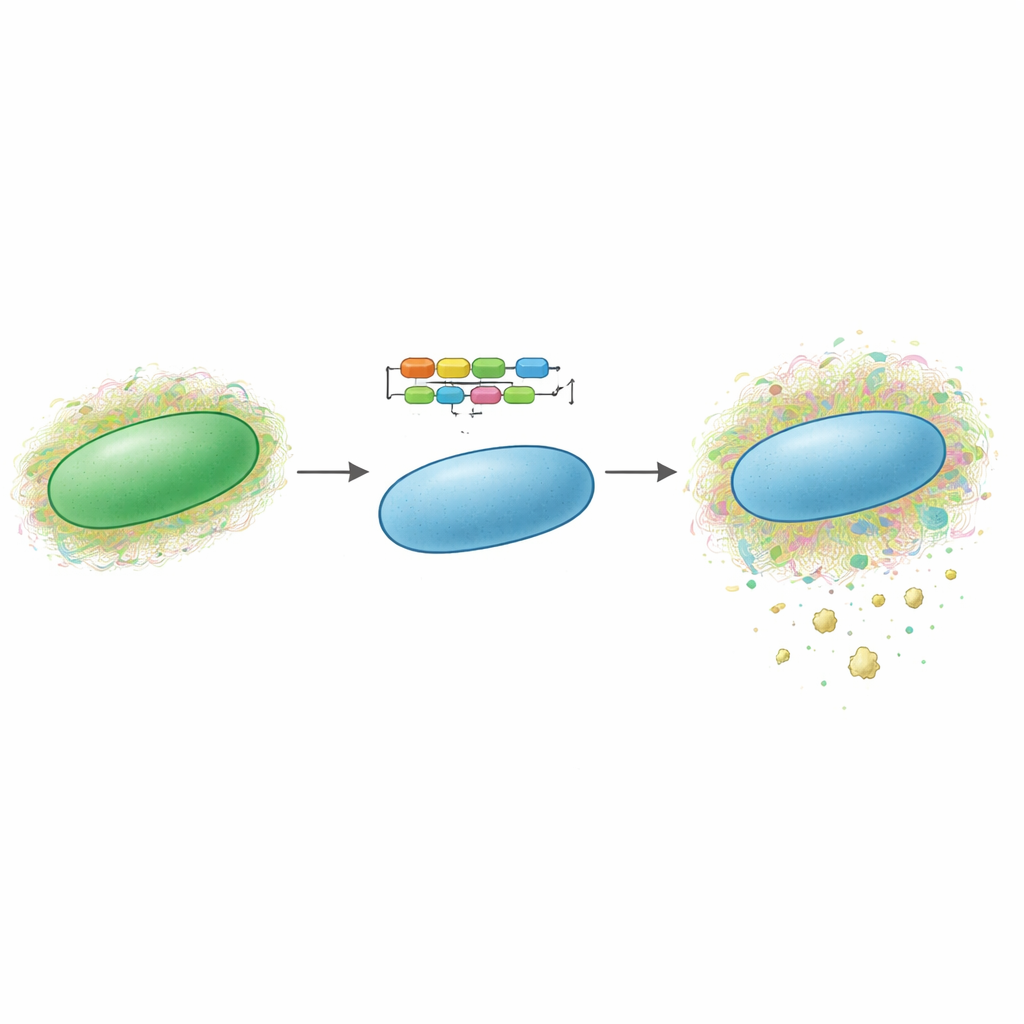
Wypożyczenie i zainstalowanie złożonego szlaku
Aby to osiągnąć, zespół podzielił system synechan na dwie główne części: geny, które budują i wydzielają polimer cukrowy, oraz geny pełniące funkcję przełączników włączających i wyłączających tych budowniczych. Wstawili geny biosyntezy do plazmidu przekaźnikowego i umieścili jeden kluczowy gen pod kontrolą silnego, indukowalnego promotora, tak że dodany sygnał chemiczny (IPTG) uruchamiał produkcję. Następnie zintegrowali geny regulacyjne w neutralnym miejscu chromosomu gospodarza, również pod kontrolą indukowalną. Po włączeniu układu wzrost wyizolowanego szczepu znacznie zwolnił, a komórki zaczęły się zbijać w skupiska. Mikroskopia elektronowa ujawniła długie włókniste materiały pokrywające powierzchnię komórek. Specjalne barwienie selektywnie uwidaczniające sulfowane polisacharydy wykazało wyraźne niebieskie agregaty poza komórkami, a testy chemiczne potwierdziły, że zarówno cukry związane z komórką, jak i wydzielone do środowiska, wzrosły w porównaniu do szczepów kontrolnych.
Jak nowy cukier wygląda wewnątrz i na zewnątrz
Naukowcy następnie sprawdzili, czy nowy materiał rzeczywiście przypomina synechan. Rozkładając polimery i analizując ich jednostki budulcowe, stwierdzili, że inżynierowane komórki produkowały sulfowany polisacharyd złożony z glukozy, galaktozy i mannozy, z zawartością siarczanów podobną do naturalnego synechanu, lecz z innym stosunkiem cukrów. W przeciwieństwie do synechanu, który jest w dużej mierze uwalniany do otaczającego płynu, znaczna część nowego polimeru pozostawała związana z powierzchnią komórek. Sugeruje to, że chociaż przeniesiony zestaw genów zadziałał, nie odtworzył pierwotnej struktury dokładnie; zamiast tego metabolizm i systemy transportowe gospodarza ukształtowały produkt „podobny do synechanu”. Sekwencjonowanie RNA obejmujące cały genom wykazało, że włączenie genów xss globalnie przeprogramowało zachowanie komórek: wzrosły czynniki związane ze stresem, spadły geny fotosyntetyczne i odpowiedzialne za pobór składników odżywczych, a ścieżki obsługujące cukry i siarkę zostały dostosowane — wszystko zgodne z przekierowaniem zasobów komórkowych na wytwarzanie energetycznie kosztownego, zewnętrznego płaszcza.
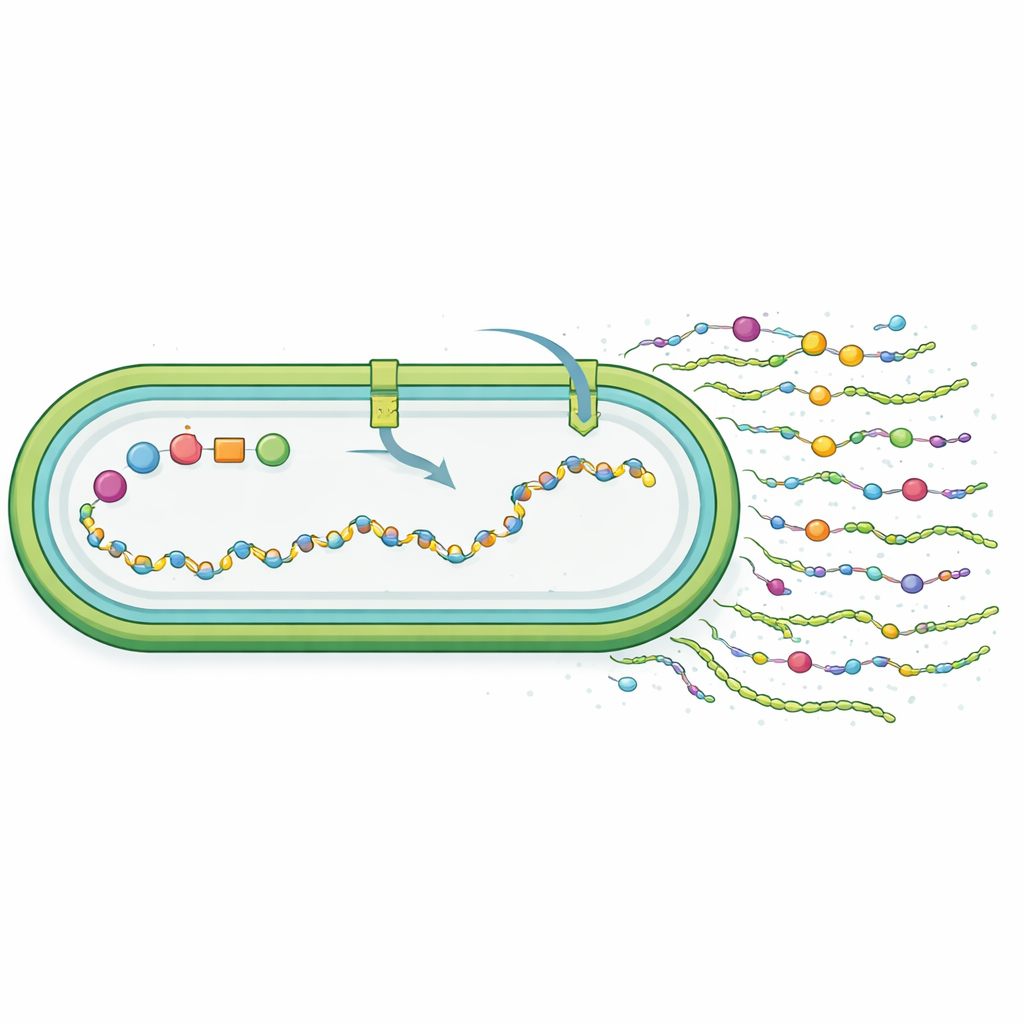
Budowanie zielonego projektowania molekularnego
Z perspektywy laika zasadniczym przesłaniem jest to, że naukowcom udało się przenieść dużą, związana z błoną maszynerię biosyntetyczną — z jednego mikroorganizmu do drugiego — i sprawić, by biorca wytwarzał nowy typ sulfowanego pokrycia cukrowego. Produkt nie jest dokładną kopią oryginalnego polimeru, ale ta różnica jest obiecująca: pokazuje, że drobne cechy tych cząsteczek można regulować przez zmianę gospodarza i projektu genetycznego. W dłuższej perspektywie podejście to mogłoby umożliwić „fabryki mikrobowe napędzane słońcem”, które przekształcają dwutlenek węgla, światło i proste składniki odżywcze w biblioteki sprofilowanych sulfowanych polisacharydów o określonych teksturach i aktywnościach biologicznych, zmniejszając zależność od źródeł zwierzęcych i otwierając nowe drogi dla zrównoważonych leków, kosmetyków i żywności funkcjonalnej.
Cytowanie: Maeda, K., Ohdate, K., Sakamaki, Y. et al. Transfer of the synechan biosynthesis and regulatory pathway enables sulfated polysaccharide production in Synechococcus elongatus PCC 7942. Sci Rep 16, 13012 (2026). https://doi.org/10.1038/s41598-026-46439-4
Słowa kluczowe: sulfowane polisacharydy, inżynieria cyjanobakterii, egzopolisacharydy, fototrofowe bioprodukcje, biologia syntetyczna