Clear Sky Science · es
Transferencia de la biosíntesis y la vía reguladora de synechan permite la producción de polisacáridos sulfatados en Synechococcus elongatus PCC 7942
Convertir la luz solar en azúcares útiles
Los polisacáridos sulfatados son largas moléculas basadas en azúcares con grupos sulfato unidos que les confieren propiedades notables: pueden retener gran cantidad de agua, formar geles e interaccionar con nuestras células de maneras que los hacen útiles en medicina y cosmética. Hoy muchos de estos compuestos provienen de animales como cerdos y tiburones, o de algas marinas, lo que plantea problemas de coste, sostenibilidad y ética. Este estudio explora si microbios fotosintéticos sencillos —las cianobacterias— pueden reprogramarse para fabricar estas valiosas moléculas directamente a partir de la luz solar y el dióxido de carbono, señalando rutas más sostenibles para producir ingredientes de alto valor para la salud y la industria.
Por qué importan estos azúcares especiales
Los polisacáridos sulfatados ya desempeñan papeles discretos pero importantes en la vida cotidiana. Variantes como la heparina ayudan a prevenir coágulos sanguíneos, y moléculas relacionadas se añaden a cremas para la piel y colirios por su capacidad calmante y de retención de agua. Industrialmente, sin embargo, todavía se obtienen sobre todo de ganado y organismos marinos, lo que vincula su suministro a la cría de animales y la pesca. Es posible sulfatar químicamente azúcares en una fábrica, pero es caro, principalmente porque la molécula donadora de sulfato activada tiene un coste elevado. Una célula viva que pueda ensamblar tanto la cadena de azúcares como las decoraciones de sulfato por sí sola, usando la luz solar como fuente de energía, podría ofrecer una alternativa más limpia y económica.
Las cianobacterias como pequeñas fábricas de azúcares
Las cianobacterias son organismos microscópicos impulsados por la luz solar, a menudo llamados “algas verdeazuladas”. Muchas especies se rodean de manera natural con complejos recubrimientos viscosos de azúcares que pueden incluir polisacáridos sulfatados. Los autores descubrieron previamente un nuevo exopolisacárido sulfatado, denominado synechan, producido por una cianobacteria modelo, Synechocystis sp. PCC 6803. Identificaron el gran conjunto de genes —llamado clúster xss— que sintetiza synechan y controla su producción. En el nuevo estudio preguntaron si todo este programa genético podría transferirse a otra cianobacteria bien estudiada, Synechococcus elongatus PCC 7942, que normalmente no produce polisacáridos sulfatados. Si era posible, sería una prueba de concepto de que tales vías pueden trasladarse entre microbios como si fueran herramientas modulares. 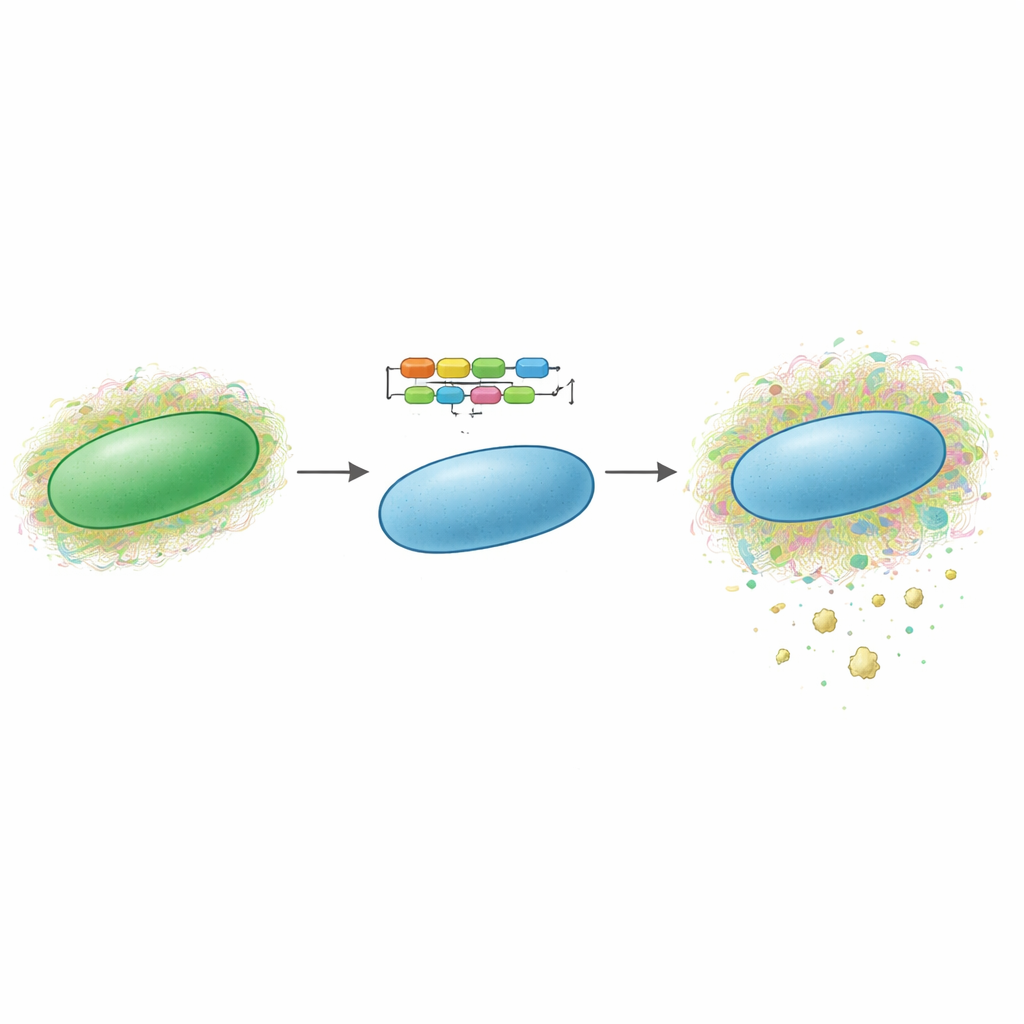
Tomar prestada e instalar una vía compleja
Para lograrlo, el equipo dividió el sistema synechan en dos partes principales: los genes que construyen y secretan el polímero de azúcar, y los genes que actúan como interruptores de encendido y apagado para esos ensambladores. Insertaron los genes de biosíntesis en un plásmido de transporte y colocaron un gen clave bajo el control de un promotor fuerte e inducible, de modo que una señal química añadida (IPTG) desencadenara la producción. Luego integraron los genes reguladores en un lugar neutro del cromosoma del hospedador, también bajo control inducible. Al activar el sistema, el crecimiento de la cepa modificada se ralentizó notablemente y las células comenzaron a agregarse. La microscopía electrónica reveló materiales fibrosos largos recubriendo las superficies celulares. Tinciones especiales que resaltan selectivamente los polisacáridos sulfatados mostraron agregados azules claros fuera de las células, y ensayos químicos confirmaron que tanto los azúcares ligados a la célula como los liberados al exterior aumentaron en comparación con las cepas de control.
Cómo es el nuevo azúcar por dentro y por fuera
Los investigadores preguntaron a continuación si el nuevo material realmente se parecía a synechan. Al degradar los polímeros y analizar sus bloques constituyentes, encontraron que las células modificadas producían un polisacárido sulfatado compuesto por glucosa, galactosa y mannosa, con un contenido de sulfato similar al synechan nativo pero una proporción diferente de azúcares. A diferencia de synechan, que se libera principalmente al líquido circundante, gran parte del nuevo polímero permaneció asociado a la superficie celular. Esto sugiere que, aunque el conjunto de genes transferidos funcionó, no recreó perfectamente la estructura original; en cambio, el propio metabolismo y los sistemas de transporte del hospedador modelaron un producto “tipo synechan”. El análisis de ARN a nivel genómico mostró que activar los genes xss reconfiguró globalmente el comportamiento celular: aumentaron factores relacionados con el estrés, disminuyeron genes fotosintéticos y de captación de nutrientes, y se ajustaron vías para el manejo de azúcares y azufre, todo coherente con células que desvían recursos para fabricar una cubierta extracelular demandante de energía. 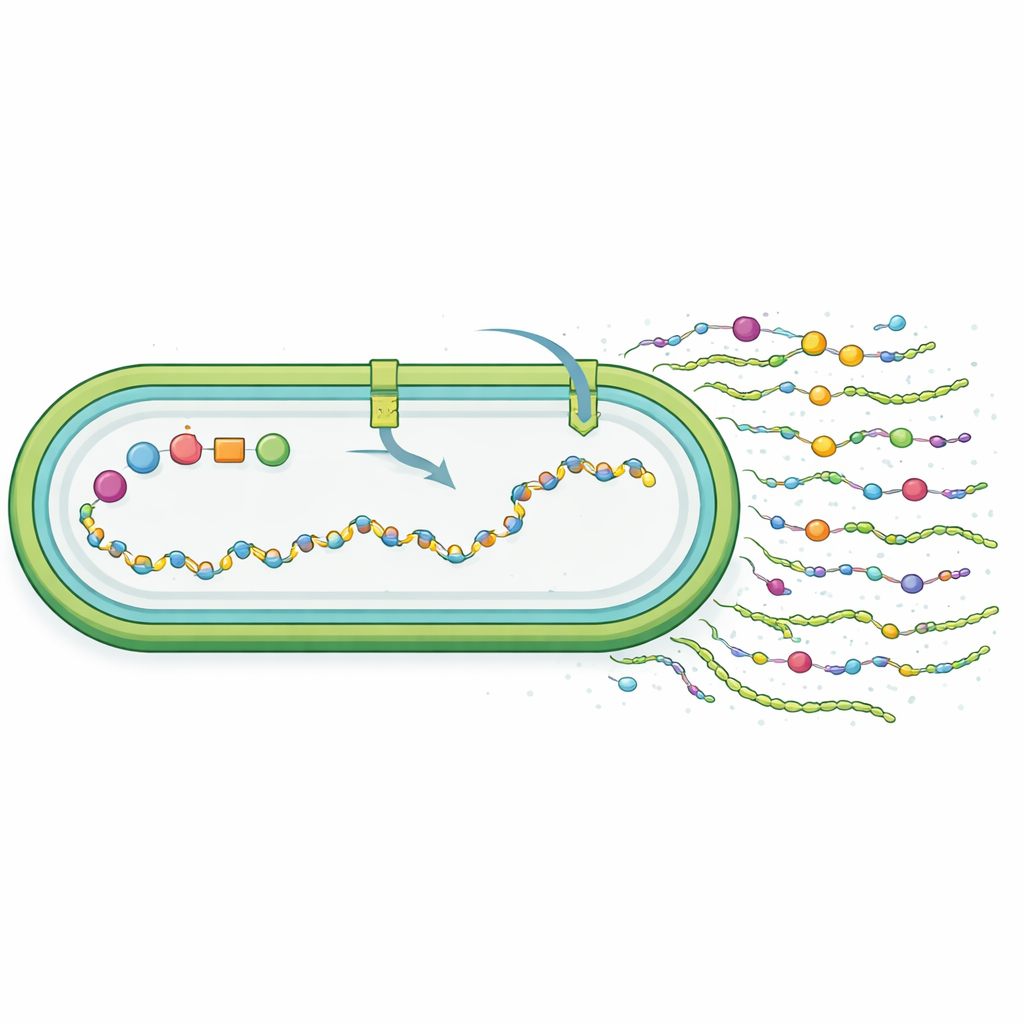
Avanzando hacia el diseño molecular sostenible
Desde una perspectiva general, el mensaje central es que los científicos trasladaron con éxito una maquinaria biosintética grande y ligada a la membrana —de un microbio a otro— y lograron que el receptor fabricara un nuevo tipo de recubrimiento azucarado sulfatado. El producto no es una copia exacta del polímero original, pero esa diferencia es en realidad prometedora: muestra que los detalles finos de estas moléculas pueden ajustarse cambiando la célula hospedadora y el diseño genético. A largo plazo, este enfoque podría permitir “fábricas” microbianas impulsadas por la luz que conviertan dióxido de carbono, luz y nutrientes simples en bibliotecas de polisacáridos sulfatados diseñados a medida con texturas y actividades biológicas específicas, reduciendo la dependencia de fuentes animales y abriendo nuevas vías para fármacos sostenibles, cosméticos y alimentos funcionales.
Cita: Maeda, K., Ohdate, K., Sakamaki, Y. et al. Transfer of the synechan biosynthesis and regulatory pathway enables sulfated polysaccharide production in Synechococcus elongatus PCC 7942. Sci Rep 16, 13012 (2026). https://doi.org/10.1038/s41598-026-46439-4
Palabras clave: polisacáridos sulfatados, ingeniería de cianobacterias, exopolisacáridos, biomanufactura fotosintética, biología sintética