Clear Sky Science · zh
基于免疫信息学的多表位亚单位疫苗设计:利用减法组学和分子动力学模拟针对啮菌属Ruminococcus torques
为何这种肠道微生物重要
在人体肠道深处藏着一种名为Ruminococcus torques的细菌,它有助于分解覆盖肠道的黏液。当这种细菌失去平衡性生长时,与炎症性肠病和肠易激综合征等肠道疾病相关,并且在易感患者中甚至可能导致肠外感染。然而,目前尚无针对它的疫苗。本研究利用基于计算的工具设计了一种候选疫苗,旨在引导免疫系统对抗R. torques,同时尽量保留对有益肠道细菌的整体影响。 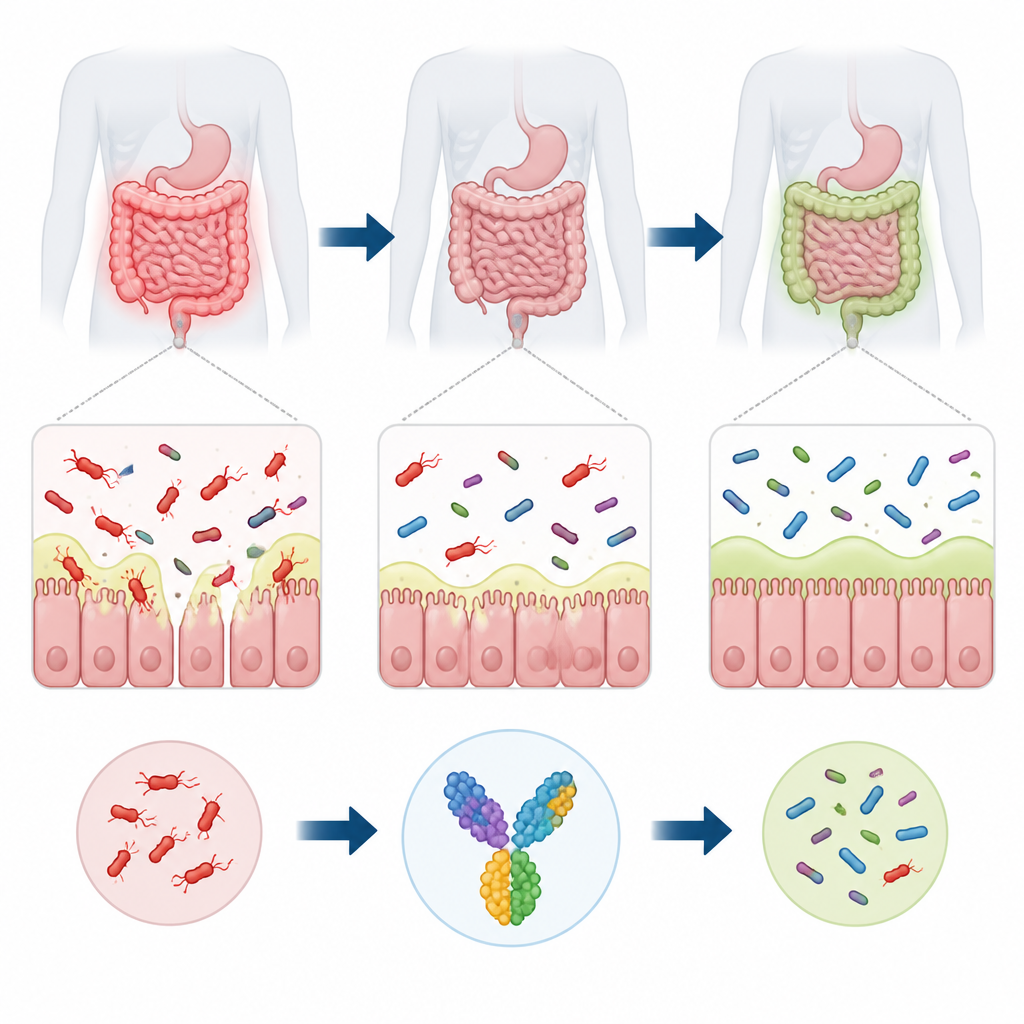
肠黏膜的麻烦制造者
覆盖肠道的黏液层像一层柔软但重要的护盾,将大多数微生物与我们的细胞保持在安全距离。R. torques擅长使用强力酶分解黏蛋白分子的糖侧链,从而“啃食”这种黏液。在平衡的肠道环境中,这种活性可以支持健康的生态系统。但当R. torques过度增殖时,它会使黏液屏障变薄,增加肠壁的通透性,并使免疫细胞持续暴露于微生物碎片。这种持续的刺激与克罗恩病和溃疡性结肠炎等慢性炎症有关,也可能促成肥胖及代谢问题。
用计算机寻找疫苗靶点
由于R. torques在实验室中难以研究,研究者转而利用其完整的蛋白质目录(即蛋白组),该数据可在公开数据库中获得。他们采用分步的“减法”策略,将近2800种蛋白质筛减到仅为数个有前景的疫苗靶点。首先,他们识别对细菌生存必不可少的蛋白。接着,剔除与人类蛋白或有益细菌蛋白高度相似的项,以降低不良交叉反应的风险。剩余候选蛋白按其触发免疫反应的可能性、以及是否无毒、无致敏性进行评分。此过程突出显示了三种参与DNA保护和细胞壁构建的关键蛋白作为有吸引力的靶点。
构建多片段疫苗
研究团队没有使用完整蛋白,而是聚焦于其中被称为表位的短片段,这些片段可被免疫细胞识别。他们预测了对杀伤性T细胞、辅助性T细胞和B细胞的表位,并按若干标准进行筛选:预测具有强免疫刺激能力、无毒无致敏信号、且不与人类蛋白显著相似。选定的表位像有色珠子一样被串联成单一的“多表位”疫苗链,使用短连接肽使每个片段能被免疫系统恰当展示。为增强免疫效果,在构建的前端连接了源自霍乱毒素亚单位的免疫增效组分。计算模型表明,所得蛋白稳定、可溶且高度抗原性。 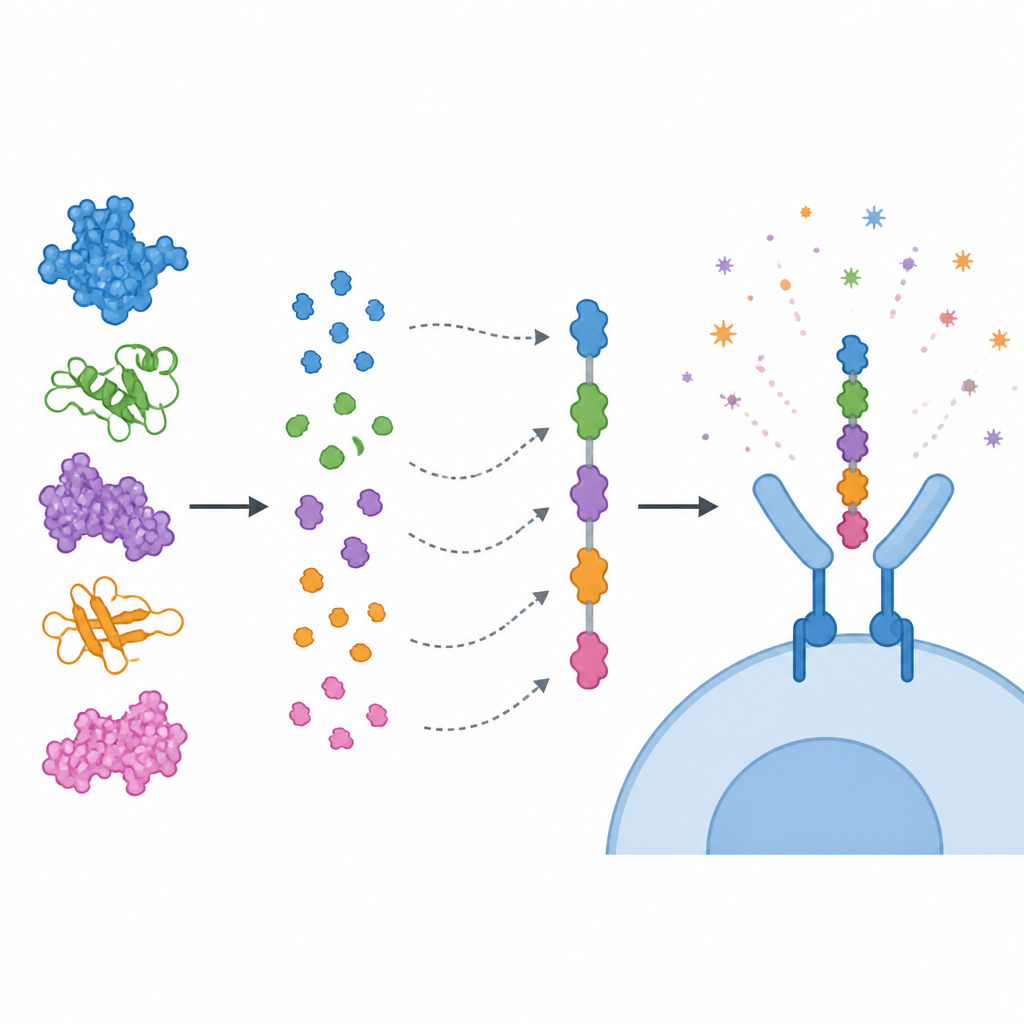
屏幕上测试结合与稳定性
为了评估该设计分子是否能与人体免疫系统发生相互作用,作者模拟了它与Toll样受体4(TLR4)的结合——TLR4是免疫细胞上检测微生物威胁的哨兵蛋白。对接研究显示二者有紧密相互作用并形成多处稳定接触,针对100纳秒的详细运动学模拟表明该复合物在水环境中保持紧密且稳定。额外的免疫反应模拟预测该疫苗可刺激抗体产生并诱导持久的T细胞反应。疫苗的基因序列也在数字上优化,使其能在常用的实验室细菌中易于表达,这是迈向真实世界测试的第一步。
这对未来治疗意味着什么
这项工作并没有提供可直接使用的疫苗,但描绘了一份经过严谨推理的蓝图。仅凭数据与算法,研究者设计出一个看似安全、稳定并能唤醒针对R. torques免疫应答的多组分蛋白。如果未来的实验室和动物研究证实这些预测,这类疫苗可能成为预防或减轻与这种黏液分解微生物相关肠道疾病的工具之一,并力求在不破坏肠道微生物群整体平衡的前提下发挥作用。
引用: Kousar, S., Manzoor, I., Muhammad, S. et al. Immunoinformatic-based design of a multi-epitope subunit vaccine against Ruminococcus torques using subtractive proteomics and molecular dynamics simulations. Sci Rep 16, 15072 (2026). https://doi.org/10.1038/s41598-026-45572-4
关键词: Ruminococcus torques, 肠道微生物组, 多表位疫苗, 逆向疫苗学, 免疫信息学