Clear Sky Science · ru
Дизайн мультиепитопной субъединичной вакцины против Ruminococcus torques на основе иммуноинформатики с использованием субтрактивной протеомики и молекулярно-динамических симуляций
Почему этот кишечный микроб важен
Глубоко в человеческом кишечнике обитает бактерия Ruminococcus torques, которая помогает расщеплять слизь, покрывающую стенки кишечника. При нарушении равновесия ее рост связывают с кишечными расстройствами, такими как воспалительные заболевания кишечника и синдром раздражённого кишечника, а у уязвимых пациентов — даже с инфекциями за пределами кишечника. В настоящее время вакцины, направленной на неё, не существует. В этом исследовании используются компьютерные инструменты для проектирования кандидата в вакцины, призванного подтолкнуть иммунную систему против R. torques при сохранении более широкой популяции полезных кишечных бактерий. 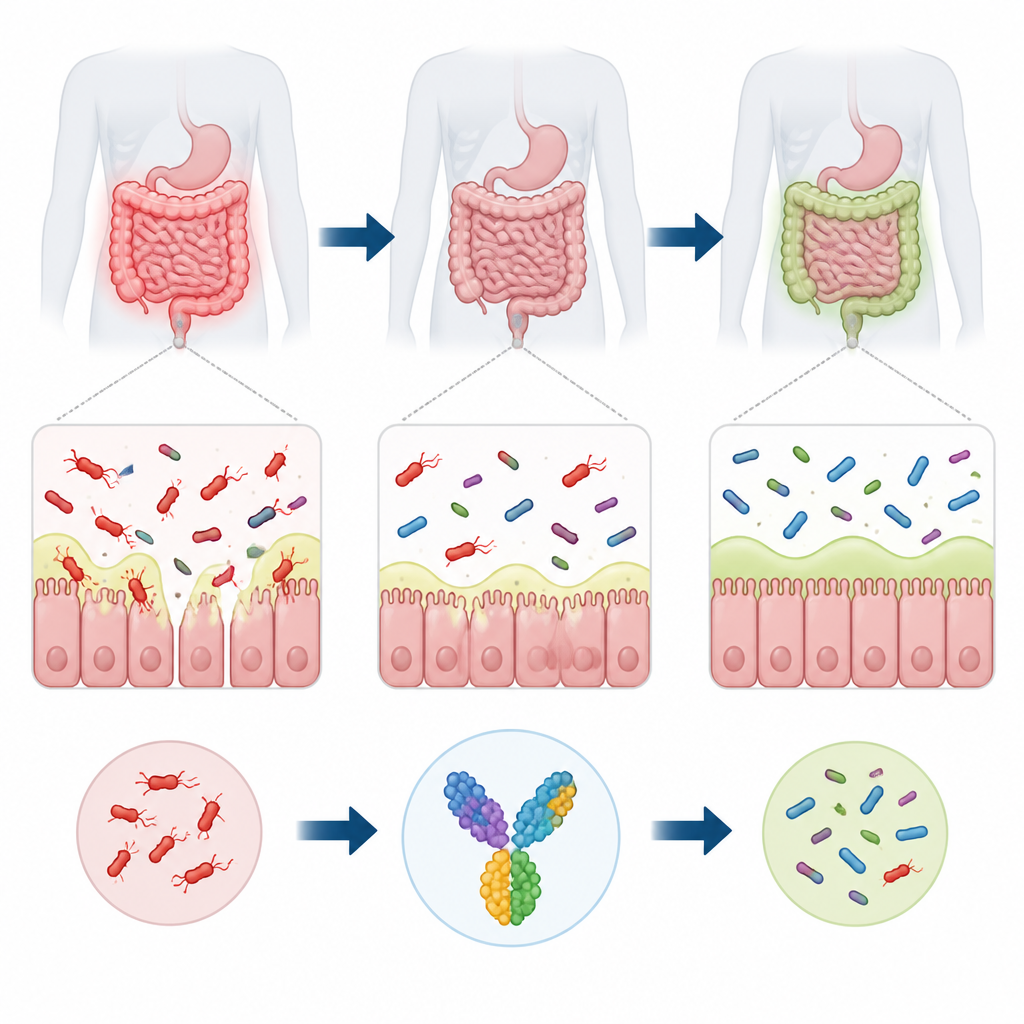
Нарушитель в слизистой оболочке кишечника
Слой слизи, покрывающий кишечник, служит мягким, но жизненно важным щитом, удерживающим большинство микробов на безопасном расстоянии от наших клеток. R. torques специализируется на «поедании» этой слизи с помощью мощных ферментов, разрушающих сахарные боковые цепи молекул муцина. В уравновешенном кишечнике такая активность может поддерживать здоровую экосистему. Но когда R. torques становится чрезмерно многочисленной, она может истончать слизистый барьер, увеличивать проницаемость стенки кишечника и подвергать иммунные клетки постоянному потоку микробных фрагментов. Это хроническое раздражение ассоциируется с воспалением при таких состояниях, как болезнь Крона и язвенный колит, и может также способствовать ожирению и метаболическим проблемам.
Использование компьютеров для поиска мишеней вакцины
Поскольку R. torques трудно изучать в лаборатории, исследователи обратились к её полному каталогу белков, или протеому, доступному в онлайн-базах данных. Они применили пошаговую «субтрактивную» стратегию, чтобы сузить список почти 2800 белков до всего нескольких перспективных мишеней для вакцины. Сначала они определили белки, необходимые для выживания бактерии. Затем исключили любые белки, которые сильно похожи на белки человека или полезных бактерий, чтобы снизить риск нежелательных перекрестных реакций. Оставшиеся кандидаты оценивали по вероятности вызова иммунного ответа без токсичности или аллергенности. Этот процесс выделил три ключевых белка, участвующих в защите ДНК и построении клеточной стенки, как привлекательные мишени.
Создание многокомпонентной вакцины
Вместо использования целых белков команда сосредоточилась на коротких участках внутри них, называемых эпитопами, которые распознают клетки иммунной системы. Они предсказали эпитопы для цитотоксических Т-клеток, помощников Т-клеток и В-клеток, затем отфильтровали их по нескольким критериям: сильная предсказанная иммунная стимуляция, отсутствие сигналов токсичности или аллергии и отсутствие высокой схожести с белками человека. Выбранные эпитопы были собраны вместе, как бусины в одну цепочку «мультиепитопной» вакцины, соединённые короткими линкерами, чтобы каждая часть правильно отображалась иммунной системе. К концу конструкта прикрепили иммуностимулирующий компонент, полученный из субъединицы холерного токсина, чтобы усилить эффект. Компьютерные модели показали, что полученный белок устойчив, растворим и обладает высокой антигенностью. 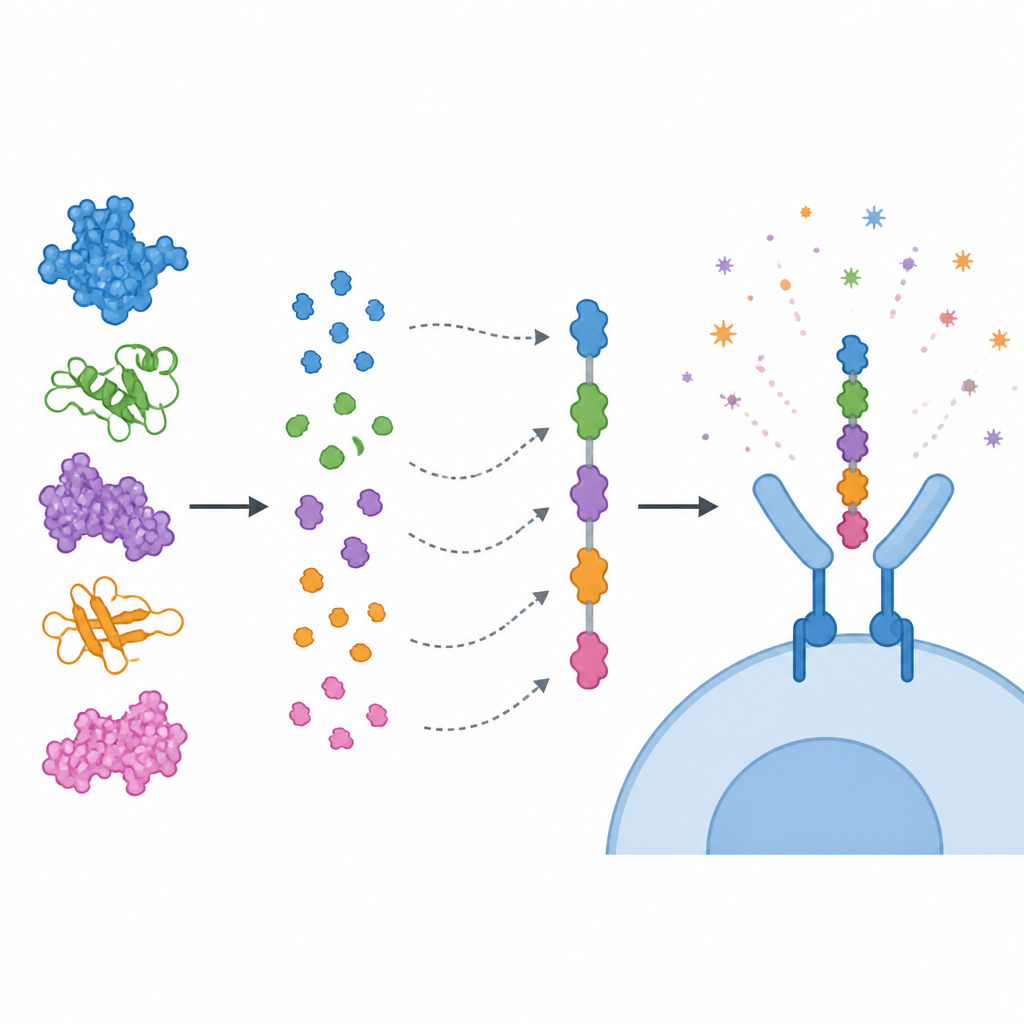
Проверка сочетаемости и стабильности на экране
Чтобы выяснить, сможет ли этот сконструированный молекула взаимодействовать с иммунной системой человека, авторы смоделировали её связывание с рецептором распознавания образов TLR4, белком-часовым на иммунных клетках, обнаруживающим микробные угрозы. Исследования докинга показали плотное взаимодействие с множеством стабилизирующих контактов, а детальные молекулярно-динамические симуляции в течение 100 миллиардных долей секунды указали, что комплекс остаётся компактным и стабильным в водной среде. Дополнительные симуляции иммунного ответа предсказали, что вакцина может стимулировать как выработку антител, так и длительные T-клеточные ответы. Последовательность гена вакцины также цифрово оптимизировали для лёгкого производства в стандартных лабораторных бактериях — первый шаг к реальному тестированию.
Что это может значить для будущих методов лечения
Эта работа не представляет готового к использованию препарата, но предлагает тщательно продуманный проект. Используя только данные и алгоритмы, исследователи спроектировали многокомпонентный белок, который по-видимому безопасен, стабилен и способен пробудить иммунный ответ против R. torques. Если будущие лабораторные и доклинические исследования подтвердят эти предсказания, такая вакцина могла бы стать частью инструментов для предотвращения или смягчения кишечных нарушений, связанных с этой «поедающей слизь» бактерией, при этом по возможности не нарушая общего баланса кишечного микробиома.
Цитирование: Kousar, S., Manzoor, I., Muhammad, S. et al. Immunoinformatic-based design of a multi-epitope subunit vaccine against Ruminococcus torques using subtractive proteomics and molecular dynamics simulations. Sci Rep 16, 15072 (2026). https://doi.org/10.1038/s41598-026-45572-4
Ключевые слова: Ruminococcus torques, кишечный микробиом, мультиепитопная вакцина, обратная вакцинология, иммуноинформатика