Clear Sky Science · de
Immunoinformatorisch entwickelter Multi-Epitop-Subunit-Impfstoff gegen Ruminococcus torques unter Verwendung subtractiver Proteomik und Molekulardynamik-Simulationen
Warum dieses Darmmikroben wichtig ist
Tief im menschlichen Darm lebt ein Bakterium namens Ruminococcus torques, das dabei hilft, die Schleimschicht des Darms abzubauen. Wenn es aus dem Gleichgewicht gerät, wird dieses Mikroorganismus mit Darmerkrankungen wie entzündlichen Darmerkrankungen und Reizdarmsyndrom sowie mit Infektionen außerhalb des Darms bei gefährdeten Patienten in Verbindung gebracht. Gegenwärtig gibt es jedoch keinen Impfstoff, der gezielt gegen es gerichtet ist. Diese Studie verwendet computerbasierte Werkzeuge, um einen Impfstoffkandidaten zu entwerfen, der das Immunsystem gegen R. torques lenken soll, ohne die breitere Gemeinschaft nützlicher Darmbakterien zu beeinträchtigen. 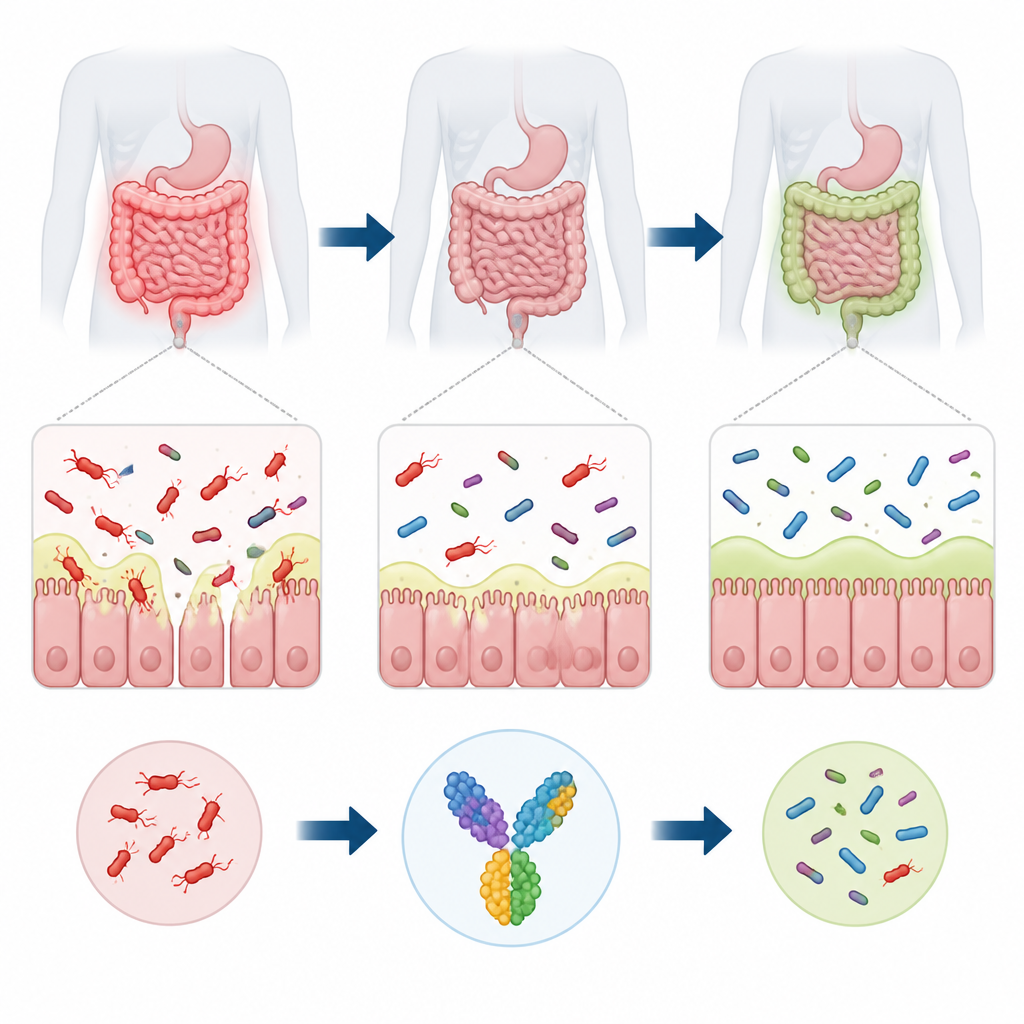
Ein Unruhestifter in der Schleimhaut
Die Schleimschicht, die den Darm überzieht, fungiert als weicher, aber lebenswichtiger Schutz und hält die meisten Mikroben auf Abstand von unseren Zellen. R. torques ist darauf spezialisiert, diesen Schleim mit kraftvollen Enzymen zu zersetzen, die die zuckerartigen Seitenketten der Muzinmoleküle abbauen. In einem ausgeglichenen Darm kann diese Aktivität ein gesundes Ökosystem unterstützen. Wenn R. torques jedoch zu dominant wird, kann es die Schleimbarriere ausdünnen, die Durchlässigkeit der Darmwand erhöhen und Immunzellen konstanten Strömen von mikrobiellen Fragmenten aussetzen. Diese anhaltende Reizung steht im Zusammenhang mit chronischer Entzündung bei Erkrankungen wie Morbus Crohn und Colitis ulcerosa und kann auch zu Fettleibigkeit und Stoffwechselstörungen beitragen.
Mit Computern nach Impfstoffzielen suchen
Da R. torques im Labor schwer zu untersuchen ist, nutzten die Forschenden dessen vollständiges Proteinkatalog, das Proteom, das öffentlich in Online-Datenbanken verfügbar ist. Sie verwendeten eine schrittweise „subtraktive“ Strategie, um fast 2800 Proteine auf nur wenige vielversprechende Impfstoffziele einzugrenzen. Zuerst identifizierten sie Proteine, die für das Überleben des Bakteriums essentiell sind. Anschließend entfernten sie alle Proteine, die dem Menschen oder nützlichen Bakterien stark ähneln, um das Risiko unerwünschter Kreuzreaktionen zu verringern. Die verbleibenden Kandidaten wurden danach bewertet, wie wahrscheinlich sie eine Immunantwort auslösen, ohne toxisch oder allergen zu sein. Dieser Prozess hob drei Schlüsselproteine hervor, die an DNA-Schutz und Zellwandaufbau beteiligt sind und als attraktive Ziele gelten.
Aufbau eines Impfstoffs aus mehreren Teilen
Anstatt ganze Proteine zu verwenden, konzentrierte sich das Team auf kurze Abschnitte in diesen Proteinen, sogenannte Epitope, die von Immunzellen erkannt werden. Sie sagten Epitope für zytotoxische T-Zellen, Helfer-T-Zellen und B-Zellen voraus und filterten sie dann mit mehreren Kriterien: hohe vorhergesagte Immunstimulation, kein Hinweis auf Toxizität oder Allergie und keine enge Ähnlichkeit zu menschlichen Proteinen. Ausgewählte Epitope wurden wie farbige Perlen zu einer einzigen „Multi-Epitop“-Impfstoffkette aneinandergereiht und mit kurzen Linkern verbunden, damit jedes Fragment dem Immunsystem korrekt präsentiert werden kann. Eine immunverstärkende Komponente, abgeleitet von einer Untereinheit des Cholera-Toxins, wurde an den N-terminalen Bereich des Konstrukts angefügt, um die Wirkung zu steigern. Computermodelle deuteten darauf hin, dass das resultierende Protein stabil, löslich und stark antigen ist. 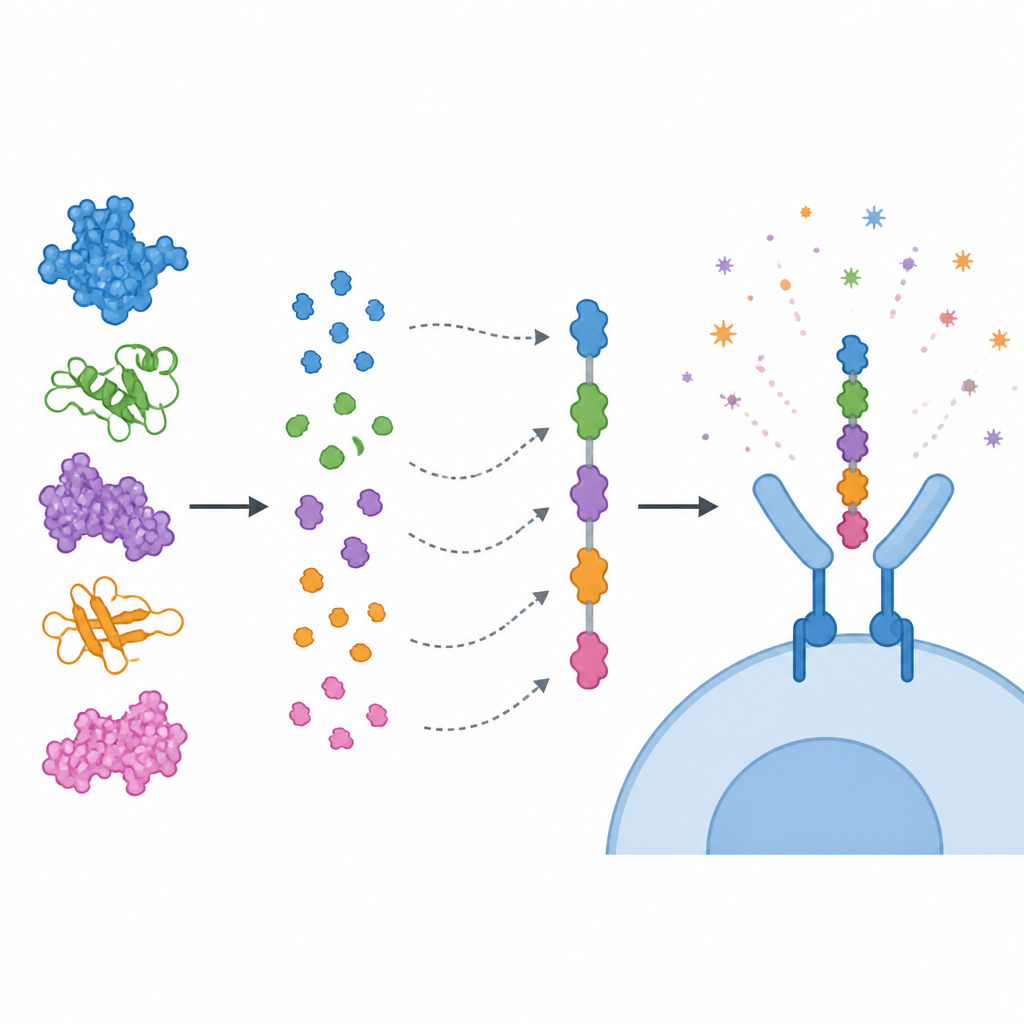
Prüfung von Bindung und Stabilität auf dem Bildschirm
Um zu prüfen, ob dieses entworfene Molekül mit dem menschlichen Immunsystem in Kontakt treten könnte, simulierten die Autoren, wie es an den Toll-like receptor 4 binden könnte, ein Wächterprotein auf Immunzellen, das mikrobielle Bedrohungen erkennt. Docking-Studien zeigten eine enge Interaktion mit vielen stabilisierenden Kontakten, und detaillierte Bewegungssimulationen über 100 Nanosekunden deuteten darauf hin, dass der Komplex in einer wässrigen Umgebung kompakt und stabil bleibt. Zusätzliche Simulationen der Immunantwort sagten voraus, dass der Impfstoff sowohl Antikörperbildung als auch langlebige T-Zell-Antworten stimulieren könnte. Die Gensequenz für den Impfstoff wurde zudem digital angepasst, um in gängigen Laborbakterien leicht produziert werden zu können, ein erster Schritt in Richtung realer Prüfungen.
Was das für künftige Behandlungen bedeuten könnte
Diese Arbeit liefert keinen sofort einsatzbereiten Impfstoff, sondern skizziert einen sorgfältig begründeten Bauplan. Allein mit Daten und Algorithmen entwarfen die Forschenden ein mehrteiliges Protein, das sicher, stabil und in der Lage zu sein scheint, das Immunsystem gegen R. torques zu wecken. Sollten zukünftige Labor- und Tierstudien diese Vorhersagen bestätigen, könnte ein solcher Impfstoff Teil eines Instrumentariums werden, um Darmerkrankungen zu verhindern oder abzuschwächen, die mit diesem schleimabbauenden Mikroben in Verbindung stehen — idealerweise ohne das übergeordnete Gleichgewicht des intestinalen Mikrobioms zu stören.
Zitation: Kousar, S., Manzoor, I., Muhammad, S. et al. Immunoinformatic-based design of a multi-epitope subunit vaccine against Ruminococcus torques using subtractive proteomics and molecular dynamics simulations. Sci Rep 16, 15072 (2026). https://doi.org/10.1038/s41598-026-45572-4
Schlüsselwörter: Ruminococcus torques, Darmmikrobiom, Multi-Epitop-Impfstoff, Reverse Vaccinology, Immunoinformatik