Clear Sky Science · fr
Conception immunoinformatique d’un vaccin sous-unitaire multi-épitopes contre Ruminococcus torques en utilisant la protéomique soustractive et des simulations de dynamique moléculaire
Pourquoi ce microbe intestinal compte
Cachée au plus profond de l’intestin humain vit une bactérie appelée Ruminococcus torques qui participe à la dégradation du mucus tapissant l’intestin. Lorsqu’elle prolifère de manière déséquilibrée, ce microbe est associé à des troubles intestinaux tels que les maladies inflammatoires de l’intestin et le syndrome de l’intestin irritable, et peut même provoquer des infections hors du tube digestif chez des patients vulnérables. Pourtant, il n’existe actuellement aucun vaccin qui la cible. Cette étude utilise des outils informatiques pour concevoir un candidat vaccin destiné à orienter le système immunitaire contre R. torques tout en préservant la communauté plus large des bactéries intestinales bénéfiques. 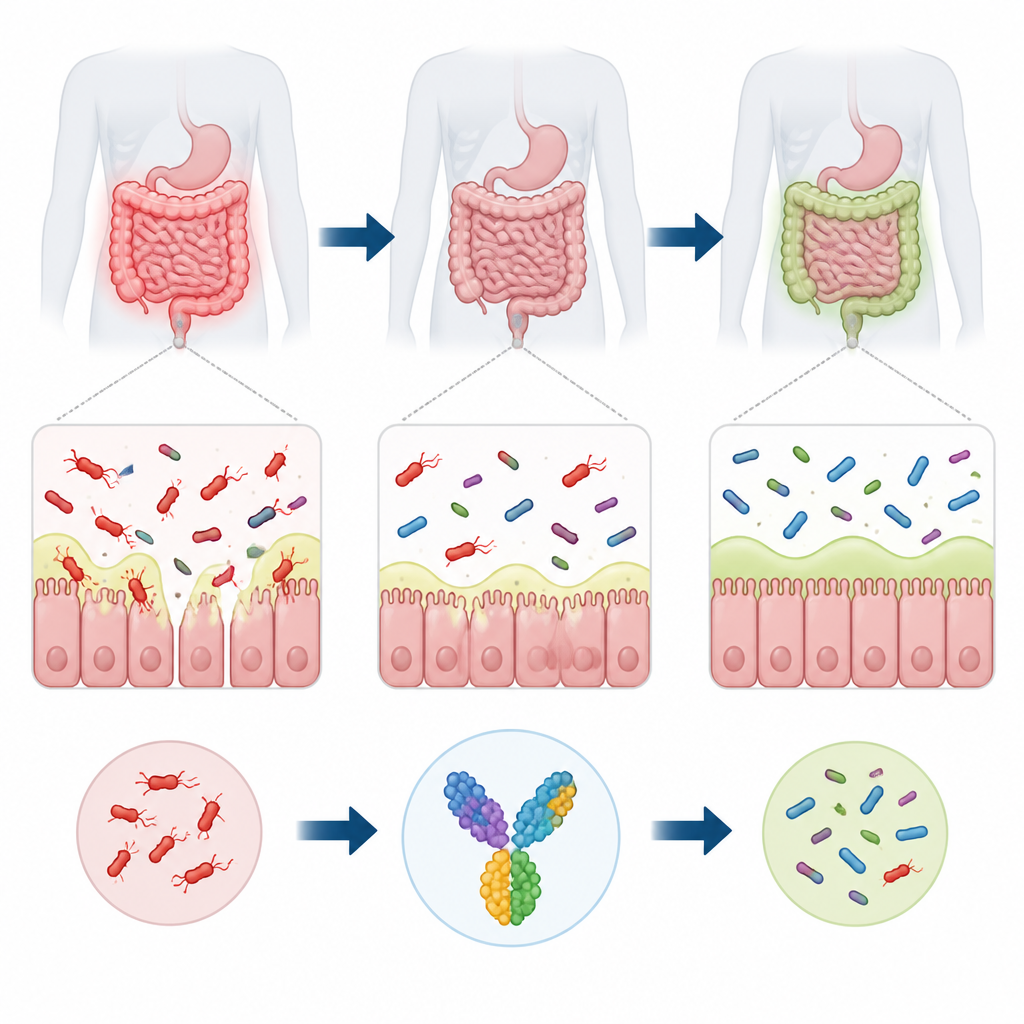
Un fauteur de troubles de la couche muqueuse
La couche de mucus qui revêt l’intestin agit comme un bouclier souple mais vital, maintenant la plupart des microbes à une distance sûre de nos cellules. R. torques est spécialisé dans la dégradation de ce mucus grâce à des enzymes puissantes qui démantèlent les chaînes sucrées des molécules de mucine. Dans un intestin équilibré, cette activité peut soutenir un écosystème sain. Mais lorsque R. torques devient trop abondant, il peut amincir la barrière muqueuse, augmenter la perméabilité de la paroi intestinale et exposer les cellules immunitaires à un flux constant de fragments microbiens. Cette irritation persistante est associée à une inflammation chronique dans des affections comme la maladie de Crohn et la rectocolite hémorragique, et peut aussi contribuer à l’obésité et à des troubles métaboliques.
Utiliser l’informatique pour repérer des cibles vaccinales
Parce que R. torques est difficile à étudier en laboratoire, les chercheurs se sont tournés vers son catalogue protéique complet, ou protéome, qui est disponible publiquement dans des bases de données en ligne. Ils ont employé une stratégie « soustractive » par étapes pour réduire près de 2 800 protéines à seulement quelques cibles vaccinales prometteuses. D’abord, ils ont identifié les protéines essentielles à la survie de la bactérie. Ensuite, ils ont écarté toute protéine présentant une forte similarité avec des protéines humaines ou celles de bactéries bénéfiques, afin de réduire le risque de réactions croisées indésirables. Les candidats restants ont été évalués selon leur probabilité de déclencher une réponse immunitaire sans être toxiques ni allergènes. Ce processus a mis en lumière trois protéines clés impliquées dans la protection de l’ADN et la construction de la paroi cellulaire comme cibles attractives.
Assembler un vaccin en plusieurs pièces
Plutôt que d’utiliser des protéines entières, l’équipe s’est concentrée sur de courts segments qu’elles contiennent, appelés épitopes, que les cellules immunitaires reconnaissent. Ils ont prédit des épitopes pour les lymphocytes T cytotoxiques, les lymphocytes T auxiliaires et les lymphocytes B, puis les ont filtrés selon plusieurs critères : fort potentiel de stimulation immunitaire prévu, absence de signaux de toxicité ou d’allergie, et absence de similarité étroite avec des protéines humaines. Les épitopes sélectionnés ont été enchaînés comme des perles colorées pour former une seule protéine vaccinale « multi-épitopes », reliés par de courts linkers afin que chaque fragment puisse être correctement présenté au système immunitaire. Un adjuvant dérivé d’une sous-unité de la toxine cholérique a été attaché à l’avant du construct pour renforcer son effet. Les modèles informatiques ont suggéré que la protéine résultante est stable, soluble et fortement antigénique. 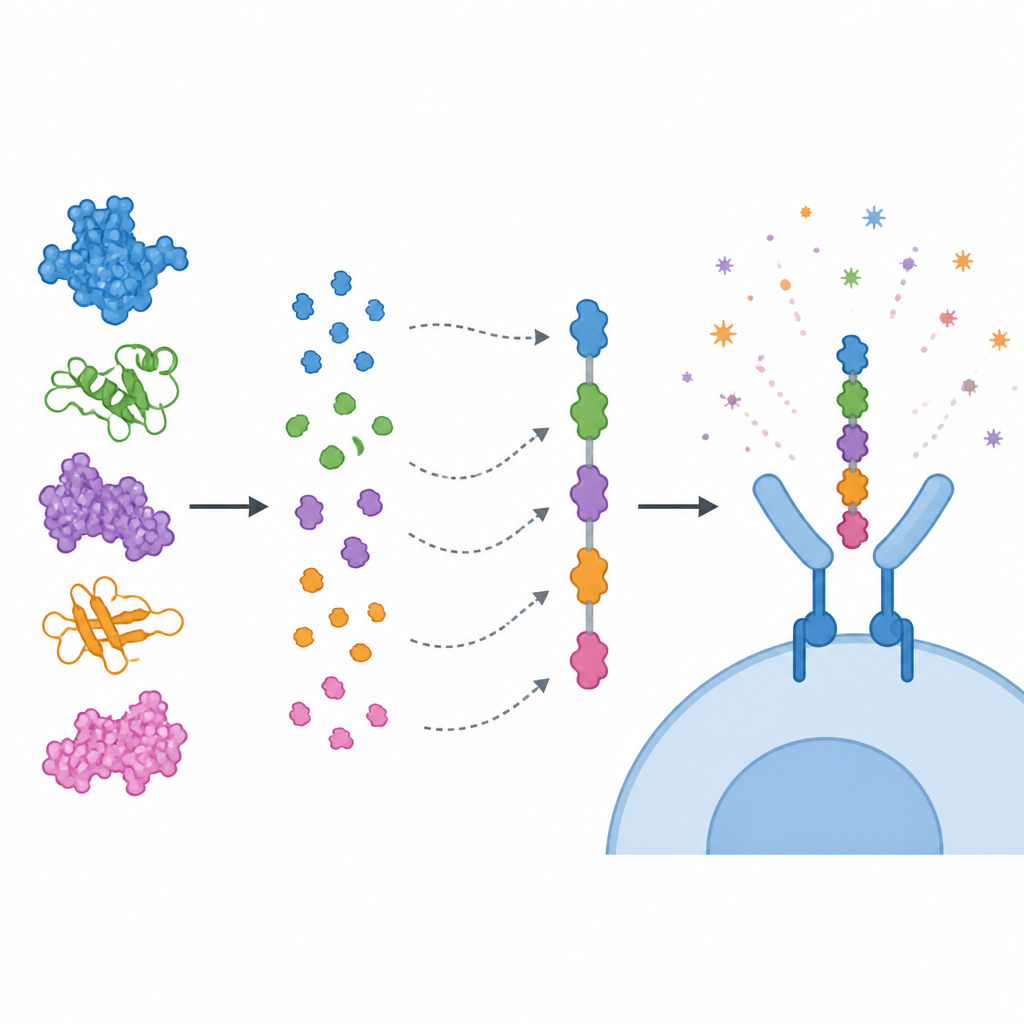
Évaluer l’ajustement et la stabilité sur écran
Pour vérifier si cette molécule conçue pouvait interagir avec le système immunitaire humain, les auteurs ont simulé son liaison au récepteur de type Toll 4, une protéine sentinelle des cellules immunitaires qui détecte les menaces microbiennes. Les études de docking ont indiqué une interaction serrée avec de nombreux contacts stabilisants, et des simulations de mouvement détaillées sur 100 milliardièmes de seconde ont suggéré que le complexe reste compact et stable dans un environnement aqueux. Des simulations complémentaires de la réponse immunitaire ont prédit que le vaccin pourrait stimuler à la fois la production d’anticorps et des réponses durables des lymphocytes T. La séquence génique du vaccin a également été adaptée numériquement pour être facilement exprimée dans des bactéries de laboratoire standard, une première étape vers des tests expérimentaux en conditions réelles.
Ce que cela pourrait signifier pour les traitements futurs
Ce travail ne délivre pas une injection prête à l’emploi, mais il expose un plan soigneusement argumenté. En n’utilisant que des données et des algorithmes, les chercheurs ont conçu une protéine multi-éléments qui semble sûre, stable et capable d’éveiller le système immunitaire contre R. torques. Si des études futures en laboratoire et chez l’animal confirment ces prédictions, un tel vaccin pourrait devenir un outil pour prévenir ou atténuer les troubles intestinaux liés à ce microbe qui consomme le mucus, idéalement sans perturber l’équilibre global du microbiome intestinal.
Citation: Kousar, S., Manzoor, I., Muhammad, S. et al. Immunoinformatic-based design of a multi-epitope subunit vaccine against Ruminococcus torques using subtractive proteomics and molecular dynamics simulations. Sci Rep 16, 15072 (2026). https://doi.org/10.1038/s41598-026-45572-4
Mots-clés: Ruminococcus torques, microbiote intestinal, vaccin multi-épitopes, vaccinologie inverse, immunoinformatique