Clear Sky Science · it
Progettazione immunoinformatica di un vaccino sotto-unità multi-epitopo contro Ruminococcus torques mediante proteomica sottrattiva e simulazioni di dinamica molecolare
Perché questo microbo intestinale è importante
Nascosto nelle profondità dell’intestino umano vive un batterio chiamato Ruminococcus torques che contribuisce a degradare il muco che riveste l’intestino. Quando la sua popolazione si sbilancia, questo microrganismo è associato a disturbi intestinali come le malattie infiammatorie croniche dell’intestino e la sindrome dell’intestino irritabile, e può persino causare infezioni extra-intestinali in pazienti vulnerabili. Al momento non esiste un vaccino mirato contro di esso. Questo studio utilizza strumenti informatici per progettare un candidato vaccino pensato per orientare il sistema immunitario contro R. torques preservando al contempo la comunità più ampia dei batteri intestinali benefici. 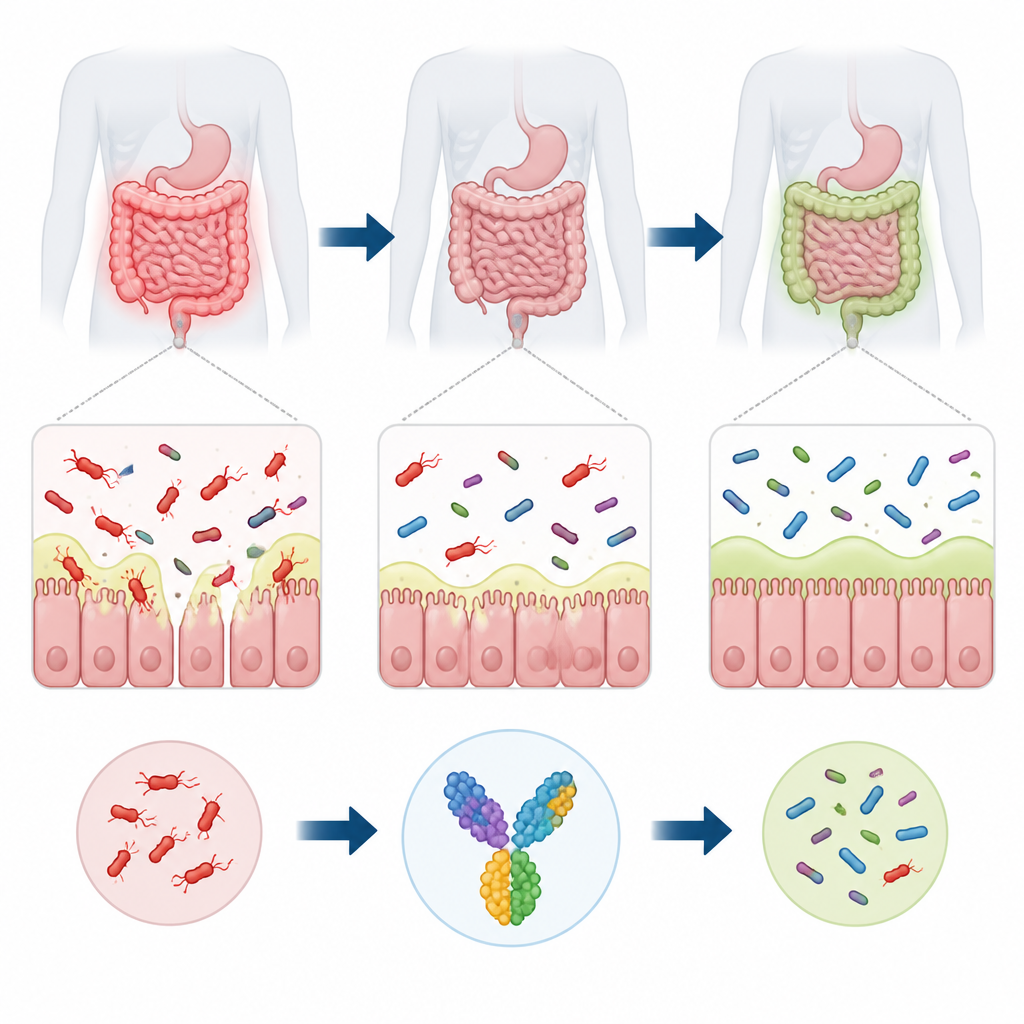
Un disturbo nello strato mucoso
Lo strato di muco che riveste l’intestino agisce come uno scudo morbido ma vitale, mantenendo la maggior parte dei microbi a distanza sicura dalle nostre cellule. R. torques è specializzato nel degradare questo muco grazie a potenti enzimi che smantellano le catene zuccherine laterali delle molecole di mucina. In un intestino equilibrato questa attività può contribuire a sostenere un ecosistema sano. Ma quando R. torques diventa troppo abbondante, può assottigliare la barriera mucosa, aumentare la permeabilità della parete intestinale ed esporre le cellule immunitarie a un flusso costante di frammenti microbici. Questa irritazione persistente è associata a infiammazione cronica in condizioni come il morbo di Crohn e la colite ulcerosa, e può anche contribuire a obesità e problemi metabolici.
Usare i computer per individuare i target vaccinali
Poiché R. torques è difficile da studiare in laboratorio, i ricercatori si sono rivolti al suo catalogo proteico completo, o proteoma, disponibile pubblicamente nelle banche dati online. Hanno adottato una strategia “sottrattiva” a più fasi per ridurre quasi 2800 proteine a pochi promettenti target vaccinali. Per prima cosa hanno identificato le proteine essenziali per la sopravvivenza del batterio. Successivamente hanno escluso le proteine che assomigliano strettamente a proteine umane o di batteri benefici, per ridurre il rischio di reazioni crociate indesiderate. I candidati rimanenti sono stati valutati per la loro probabilità di indurre una risposta immunitaria senza essere tossici o allergenici. Questo processo ha evidenziato tre proteine chiave coinvolte nella protezione del DNA e nella costruzione della parete cellulare come target attraenti.
Costruire un vaccino a più parti
Piuttosto che utilizzare proteine intere, il gruppo si è concentrato su brevi tratti al loro interno, chiamati epitopi, che le cellule immunitarie riconoscono. Hanno previsto epitopi per le cellule T citotossiche, le cellule T helper e le cellule B, quindi li hanno filtrati usando diversi criteri: forte potenziale di stimolazione immunitaria, assenza di segnali di tossicità o allergenicità e nessuna somiglianza ravvicinata con proteine umane. Gli epitopi selezionati sono stati concatenati come perle colorate in un’unica catena vaccinale “multi-epitopo”, unite con brevi linker in modo che ogni frammento possa essere correttamente esposto al sistema immunitario. Un componente immuno-stimolante derivato da una subunità della tossina del colera è stato aggiunto all’estremità del costrutto per potenziarne l’effetto. I modelli al computer hanno suggerito che la proteina risultante è stabile, solubile e altamente antigenica. 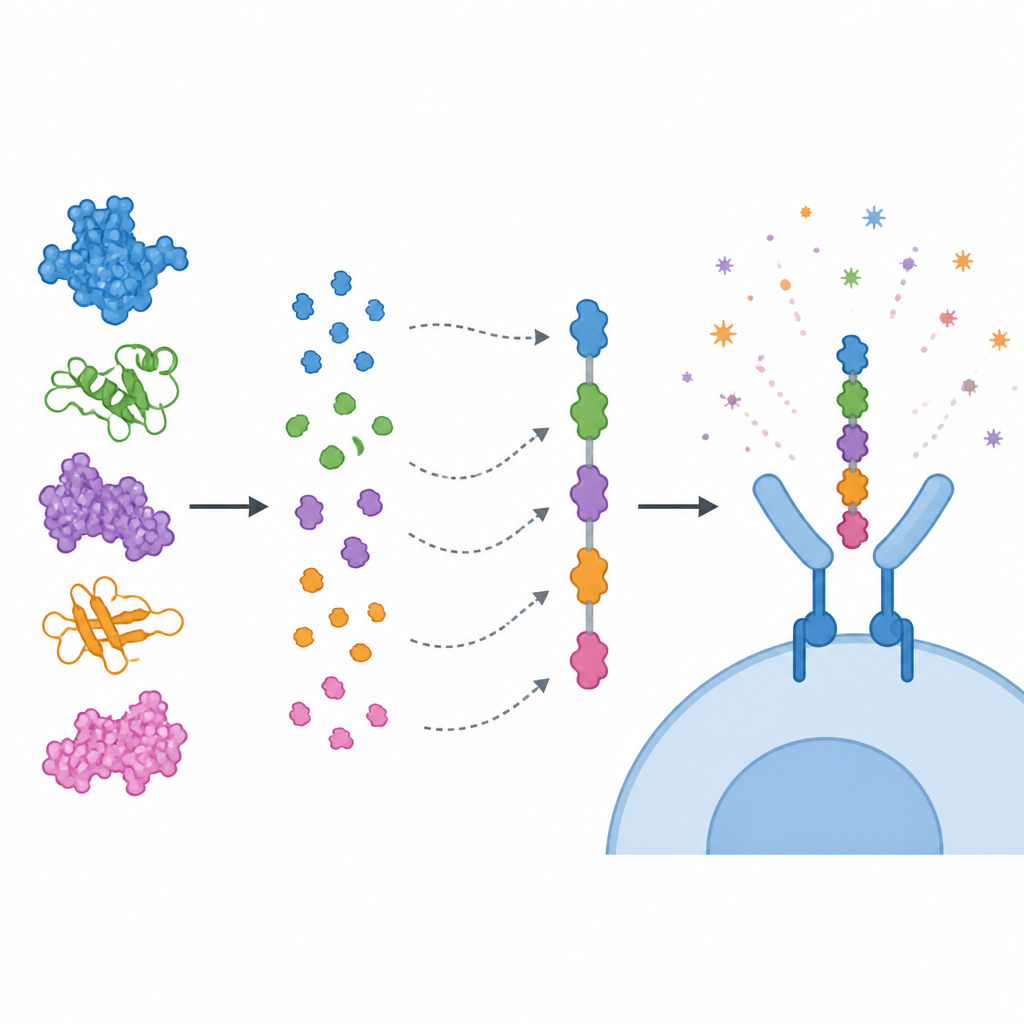
Verificare interazione e stabilità in silico
Per valutare se questa molecola progettata potesse interagire con il sistema immunitario umano, gli autori hanno simulato il suo potenziale legame con il recettore Toll-like 4, una proteina sentinella delle cellule immunitarie che rileva le minacce microbiche. Studi di docking hanno indicato un’interazione stretta con numerosi contatti stabilizzanti, e simulazioni dinamiche dettagliate per 100 miliardesimi di secondo hanno suggerito che il complesso rimane compatto e stabile in un ambiente acquoso. Ulteriori simulazioni della risposta immunitaria hanno previsto che il vaccino potrebbe stimolare sia la produzione di anticorpi sia risposte T di lunga durata. La sequenza genica del vaccino è stata inoltre ottimizzata digitalmente per essere facilmente espressa in batteri da laboratorio standard, un primo passo verso test sperimentali reali.
Cosa potrebbe significare per i trattamenti futuri
Questo lavoro non fornisce un vaccino pronto all’uso, ma delinea un progetto attentamente motivato. Utilizzando solo dati e algoritmi, i ricercatori hanno progettato una proteina multi-componente che appare sicura, stabile e capace di risvegliare il sistema immunitario contro R. torques. Se studi di laboratorio e su modelli animali futuri confermeranno queste previsioni, un tale vaccino potrebbe entrare a far parte di un arsenale per prevenire o attenuare i disturbi intestinali legati a questo microrganismo che degrada il muco, idealmente senza disturbare l’equilibrio complessivo del microbioma intestinale.
Citazione: Kousar, S., Manzoor, I., Muhammad, S. et al. Immunoinformatic-based design of a multi-epitope subunit vaccine against Ruminococcus torques using subtractive proteomics and molecular dynamics simulations. Sci Rep 16, 15072 (2026). https://doi.org/10.1038/s41598-026-45572-4
Parole chiave: Ruminococcus torques, microbioma intestinale, vaccino multi-epitopo, vaccinologia inversa, immunoinformatica