Clear Sky Science · es
Diseño inmunoinformático de una vacuna subunitaria multi-epítopo contra Ruminococcus torques mediante proteómica sustractiva y simulaciones de dinámica molecular
Por qué importa este microbio intestinal
Oculta en lo profundo del intestino humano vive una bacteria llamada Ruminococcus torques que ayuda a descomponer la mucosa que recubre el intestino. Cuando se descontrola su proliferación, este microbio se ha vinculado a trastornos intestinales como la enfermedad inflamatoria intestinal y el síndrome del intestino irritable, e incluso a infecciones fuera del tubo digestivo en pacientes vulnerables. Sin embargo, actualmente no existe una vacuna dirigida contra ella. Este estudio emplea herramientas computacionales para diseñar un candidato vacunal pensado para orientar al sistema inmunitario contra R. torques sin perjudicar a la comunidad más amplia de bacterias intestinales beneficiosas. 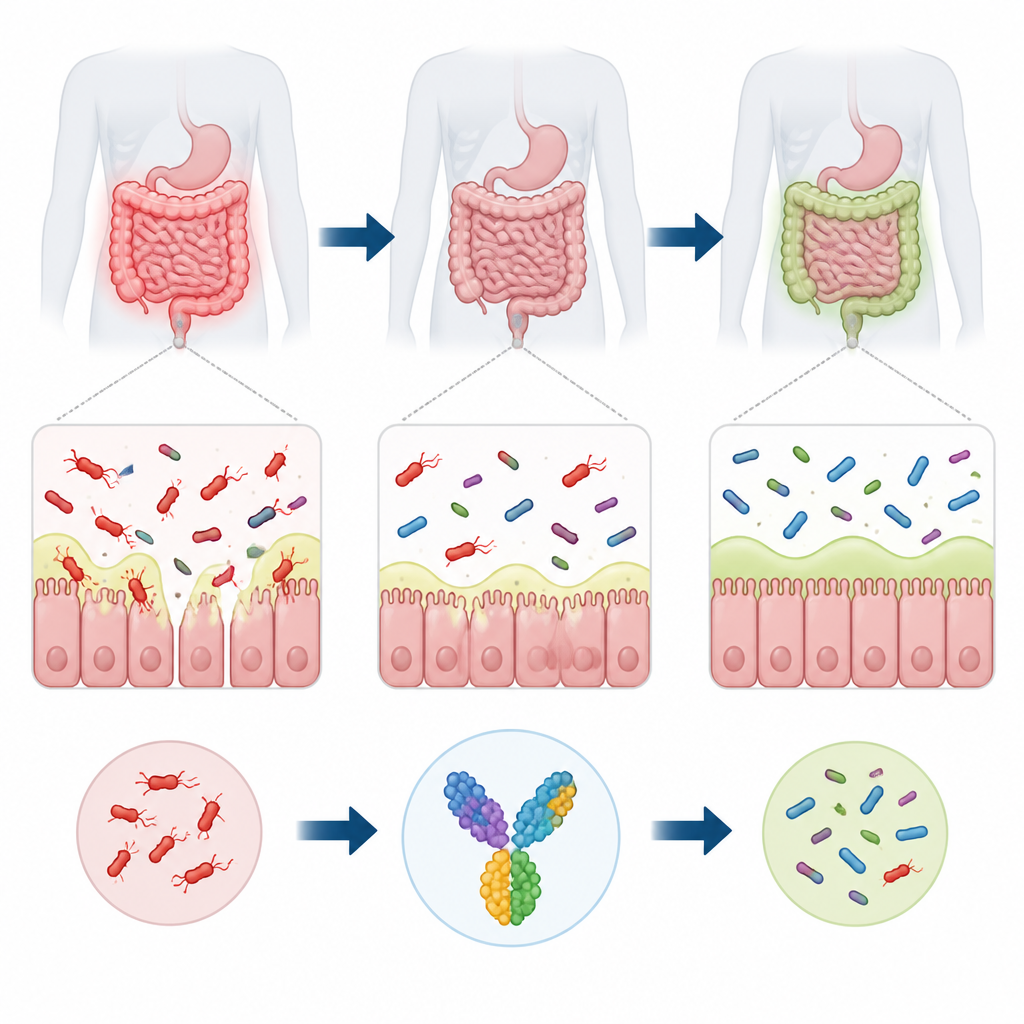
Un alborotador en el revestimiento intestinal
La capa de mucosa que recubre el intestino actúa como un escudo blando pero vital, manteniendo a la mayoría de los microbios a una distancia segura de nuestras células. R. torques se especializa en devorar esta mucosa mediante potentes enzimas que desmantelan las cadenas azucaradas de las moléculas de mucina. En un intestino equilibrado, esa actividad puede contribuir a un ecosistema saludable. Pero cuando R. torques se vuelve demasiado abundante, puede adelgazar la barrera mucosa, aumentar la permeabilidad de la pared intestinal y exponer a las células inmunitarias a un flujo constante de fragmentos microbianos. Esta irritación persistente se asocia con inflamación crónica en afecciones como la enfermedad de Crohn y la colitis ulcerosa, y también puede contribuir a la obesidad y a problemas metabólicos.
Usar ordenadores para explorar dianas vacunales
Puesto que R. torques es difícil de estudiar en el laboratorio, los investigadores recurrieron a su catálogo completo de proteínas, o proteoma, que está disponible públicamente en bases de datos en línea. Emplearon una estrategia «sustractiva» por etapas para reducir casi 2.800 proteínas a solo unas pocas dianas vacunales prometedoras. Primero identificaron las proteínas esenciales para la supervivencia de la bacteria. A continuación, eliminaron las proteínas que se parecieran mucho a proteínas humanas o a las de bacterias beneficiosas, para reducir el riesgo de reacciones cruzadas no deseadas. Los candidatos restantes se valoraron según la probabilidad de inducir una respuesta inmunitaria sin ser tóxicos ni alergénicos. Este proceso destacó tres proteínas clave implicadas en la protección del ADN y la construcción de la pared celular como dianas atractivas.
Construir una vacuna de varias piezas
En lugar de usar proteínas completas, el equipo se centró en tramos cortos dentro de ellas, llamados epítopos, que son reconocidos por las células inmunitarias. Predijeron epítopos para células T citotóxicas, células T ayudantes y células B, y luego los filtraron con varios criterios: fuerte capacidad predictiva de estimulación inmune, ausencia de señales de toxicidad o alergia y no presentar similitud estrecha con proteínas humanas. Los epítopos seleccionados se unieron en serie como cuentas de colores en una única cadena vacunal «multi-epítopo», enlazados con fragmentos cortos para que cada pieza pueda mostrarse correctamente al sistema inmunitario. Un componente potenciador inmune derivado de una subunidad de la toxina del cólera se añadió al extremo delantero de la construcción para aumentar su efecto. Los modelos computacionales sugirieron que la proteína resultante es estable, soluble y altamente antigénica. 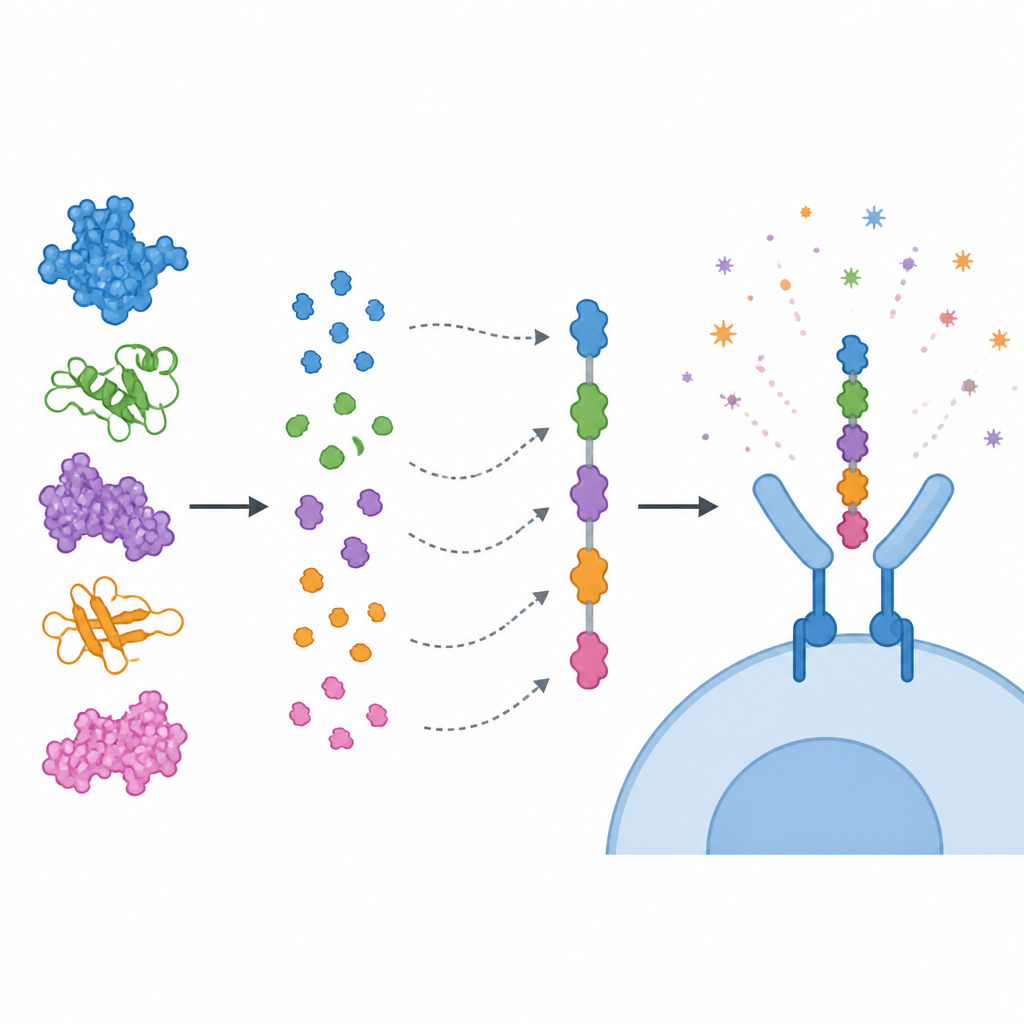
Comprobar encaje y estabilidad en pantalla
Para saber si esta molécula diseñada podría interactuar con el sistema inmune humano, los autores simularon cómo podría unirse al receptor Toll-like 4, una proteína centinela en las células inmunitarias que detecta amenazas microbianas. Estudios de acoplamiento indicaron una interacción ajustada con numerosos contactos estabilizadores, y simulaciones detalladas de movimiento durante 100 milmillonésimas de segundo sugirieron que el complejo permanece compacto y estable en un entorno acuoso. Simulaciones adicionales de la respuesta inmune predijeron que la vacuna podría estimular tanto la producción de anticuerpos como respuestas duraderas de células T. La secuencia génica de la vacuna también se ajustó digitalmente para facilitar su producción en bacterias de laboratorio estándar, un primer paso hacia las pruebas en el mundo real.
Qué podría significar esto para futuros tratamientos
Este trabajo no entrega una vacuna lista para usar, pero traza un plan cuidadosamente razonado. Usando solo datos y algoritmos, los investigadores diseñaron una proteína multipartita que parece segura, estable y capaz de activar al sistema inmunitario frente a R. torques. Si estudios futuros en laboratorio y en animales confirman estas predicciones, tal vacuna podría formar parte de un conjunto de herramientas para prevenir o mitigar trastornos intestinales vinculados a este microbio que consume mucosa, idealmente sin alterar el equilibrio global del microbioma intestinal.
Cita: Kousar, S., Manzoor, I., Muhammad, S. et al. Immunoinformatic-based design of a multi-epitope subunit vaccine against Ruminococcus torques using subtractive proteomics and molecular dynamics simulations. Sci Rep 16, 15072 (2026). https://doi.org/10.1038/s41598-026-45572-4
Palabras clave: Ruminococcus torques, microbioma intestinal, vacuna multi-epítopo, vacunología inversa, inmunoinformática