Clear Sky Science · zh
胶原特异分子伴侣 Hsp47 在腹股沟白色脂肪组织中促进雄性小鼠高脂饮食诱导的炎性基因表达
为何脂肪组织隐秘的支架很重要
肥胖常被描述为“额外的脂肪”,但脂肪组织内部的情况远比这更复杂。脂肪细胞生活在一个柔性的蛋白质支架中,当我们长期摄入高脂饮食时,这个支架可能变得僵硬、发生炎症并最终损害机体。本研究聚焦于一个较少为人所知的分子 Hsp47,它通过指导胶原生成来构建该支架。通过研究高脂饮食的小鼠,研究者提出了一个看似简单但影响深远的问题:在脂肪细胞中降低 Hsp47 是否能保护机体免受饮食诱导的损伤?
细看脂肪库的差异
并非所有体脂都是相同的。研究者聚焦于雄性小鼠的两个主要脂肪库:皮下位于腹股沟区域的脂肪(腹股沟白色脂肪组织,简称 ingWAT)和包裹器官的深层腹部脂肪(附睾白色脂肪组织,简称 epiWAT)。早期工作表明高脂饮食会增加脂肪组织中胶原及其他支架成分的基因表达,暗示结构重塑在肥胖中起关键作用。Hsp47 是细胞内的一个伴侣蛋白,确保分泌前胶原正确折叠。它已知在肝等器官的瘢痕形成中起推动作用,但在长期过量供能条件下不同脂肪库中的长期作用尚不明确。 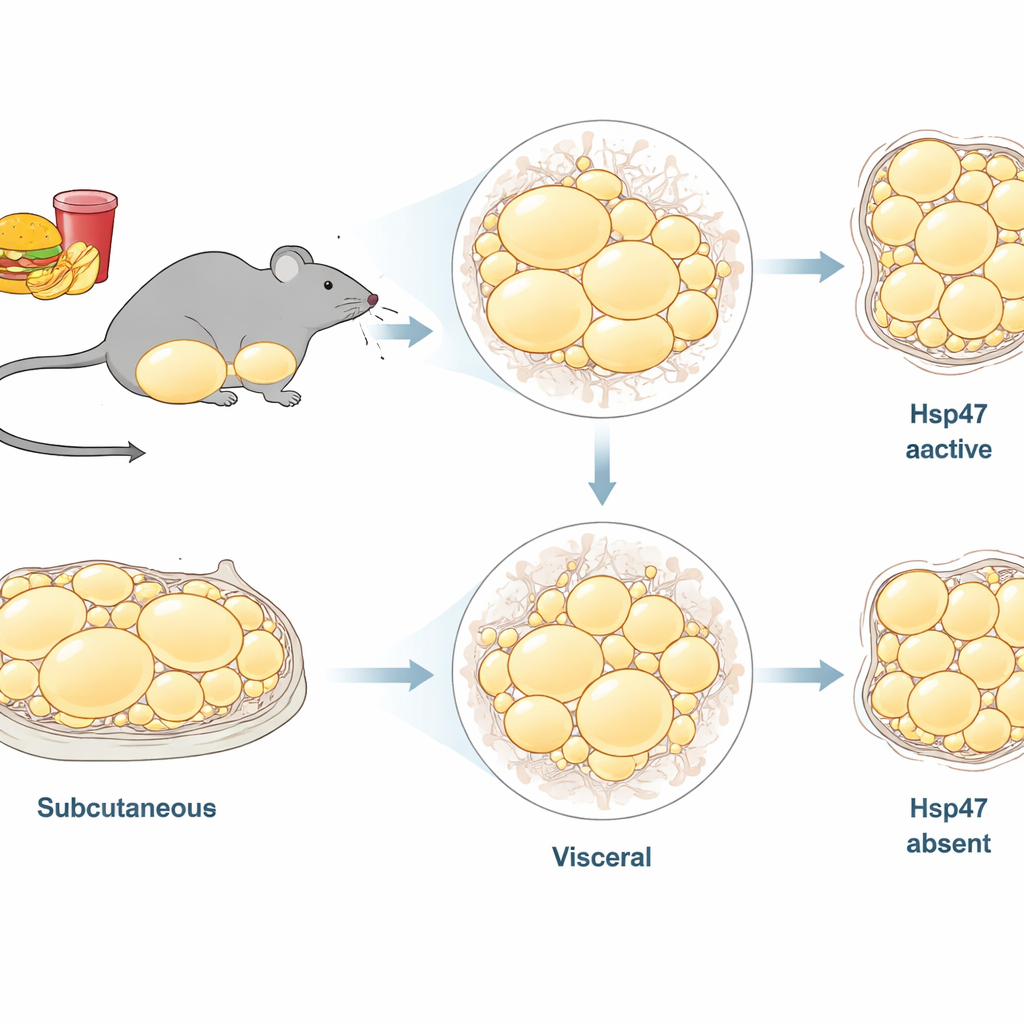
在脂肪细胞中关闭 Hsp47
为测试 Hsp47 的作用,团队构建了仅能在成熟脂肪细胞中去除 Hsp47 的小鼠,使其他组织保持完整。这样得到的脂肪细胞特异性敲除(aKO)小鼠及其正常(flox)同窝对照被喂以标准饮食或高脂饮食 12 周,时间足以触发早期炎症和胶原变化。在高脂饮食下,Hsp47 水平特异性在脂肪组织中上升,但在肾或肺中未见上调。重要的是,在脂肪细胞中删除 Hsp47 并未引发这些细胞内的压力迹象,表明与富含胶原的组织(如软骨或骨骼)相比,脂肪组织可以耐受降低的胶原伴侣活性。
Hsp47 损害最大的部位
最明显的结果出现在皮下的 ingWAT。在正常小鼠中,高脂饮食使两个库的脂肪细胞均发生膨大(肥大)。然而在 aKO 小鼠中,ingWAT 细胞抵抗这种扩张,而 epiWAT 仍然显著增大。当研究者对组织切片进行胶原染色以可视化时,他们发现总体上高脂喂养尚未引起大量胶原堆积,但在 ingWAT 中 aKO 动物的胶原阳性区域低于对照。基因表达分析强化了这种库特异性模式:在 ingWAT 中,丧失 Hsp47 使胶原基因轻度下调,并明显降低了包括白细胞介素-6、肿瘤坏死因子、Ccl2 和纤连蛋白等炎症及基质相关基因的表达。相比之下,在 epiWAT 中,Hsp47 的缺失对这些转录本影响甚微。 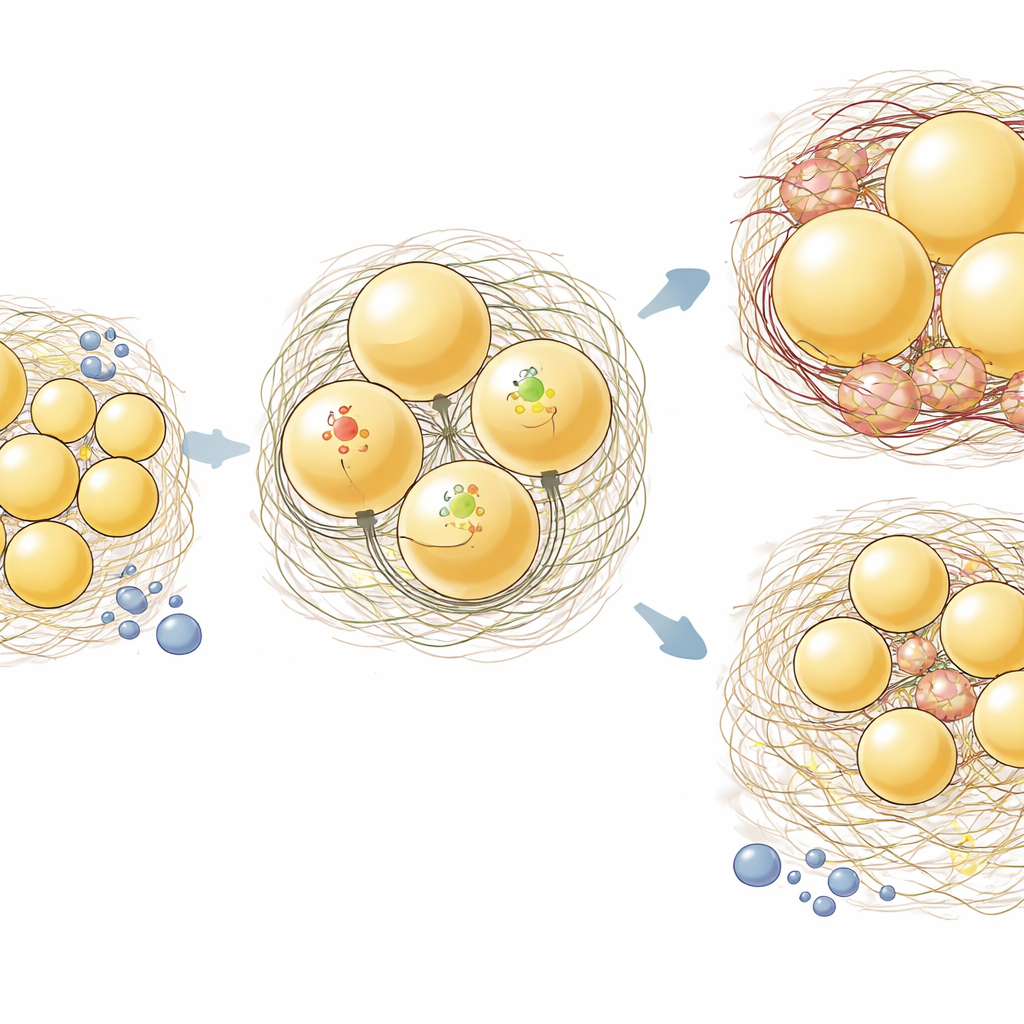
从局部脂肪变化到全身应激
由于脂肪组织通过激素和炎性信号与机体其他部位通信,团队接着检查了血液和尿液化学指标。如预期的那样,对照小鼠的高脂喂养扰乱了多项血液标志物,包括与早期肾脏应激相关的葡萄糖和矿物质水平。在 aKO 小鼠中,这些紊乱在一定程度上被缓和:无机磷和钙水平向正常值回归,若干尿液标志物提示肾相关压力较轻。数据尚未显示肾脏自身存在明确的结构性保护,但它们表明了一条事件链:由 Hsp47 驱动的 ingWAT 重塑和炎症在整体代谢与矿物质失衡中可能起到不成比例的推动作用。
这对治疗肥胖可能意味着什么
总体而言,该研究揭示了 Hsp47 是高脂饮食下脂肪支架发生不良变化的关键放大器,尤其是在皮下 ingWAT 中。当 Hsp47 活跃时,脂肪细胞周围的胶原变得更多且可能更僵硬,脂肪细胞增大,炎症基因被激活,推动机体走向系统性问题。当仅在脂肪细胞中去除 Hsp47 时,这些过程被减弱,而在正常饮食条件下未见明显问题。鉴于已经存在可用于实验的抑制 Hsp47 的小分子药物,这些发现提示了一种有前景的策略:有选择性地抑制 Hsp47 活性,可能缓解肥胖相关的有害脂肪组织重塑和炎症,同时大体保留日常脂肪功能。
引用: Ito, S., Kamei, R., Kasai, A. et al. Collagen-specific molecular chaperone Hsp47 in inguinal white adipose tissue promotes high-fat diet-induced inflammatory gene expression in male mice. Sci Rep 16, 14301 (2026). https://doi.org/10.1038/s41598-026-45003-4
关键词: 肥胖, 脂肪组织, 胶原, 炎症, 代谢性疾病