Clear Sky Science · nl
Collageenspecifieke moleculaire chaperonne Hsp47 in inguïnaal wit vetweefsel bevordert hoog-vet-dieet-geïnduceerde ontstekingsgenenexpressie bij mannelijke muizen
Waarom het verborgen geraamte van vetweefsel ertoe doet
Obesitas wordt vaak kortweg beschreven als “extra vet”, maar wat er binnen ons vetweefsel gebeurt is veel complexer. Vetcellen leven binnen een flexibel eiwitgeraamte, en bij langdurige consumptie van een vetrijk dieet kan dat geraamte verharden, ontsteken en uiteindelijk schade veroorzaken. Deze studie richt zich op een minder bekend molecuul, Hsp47, dat helpt bij het opbouwen van dat geraamte door de productie van collageen te begeleiden. Door muizen op een hoog-vet-dieet te bestuderen, stelden de onderzoekers een eenvoudige vraag met grote implicaties: beschermt het omlaag brengen van Hsp47 in vetcellen het lichaam tegen dieet-geïnduceerde schade?
Een nadere blik op vetdepots
Niet alle lichaamsvet is hetzelfde. De onderzoekers concentreerden zich op twee belangrijke vetdepots bij mannelijke muizen: onderhuids vet onder de huid in de liesstreek (inguïnaal wit vetweefsel, of ingWAT) en dieper buikvet rondom organen (epididimaal wit vetweefsel, of epiWAT). Eerder werk toonde aan dat een vetrijk dieet genen voor collageen en andere geraamtecomponenten in vet doet toenemen, wat suggereert dat structurele hermodellering centraal staat bij obesitas. Hsp47 is een hulp-eiwit binnen cellen dat ervoor zorgt dat collageen correct wordt gevouwen voordat het wordt uitgescheiden. Het staat bekend als een aanjager van littekenvorming in organen zoals de lever, maar zijn langdurige rol in verschillende vetdepots bij chronische overvoeding was onduidelijk. 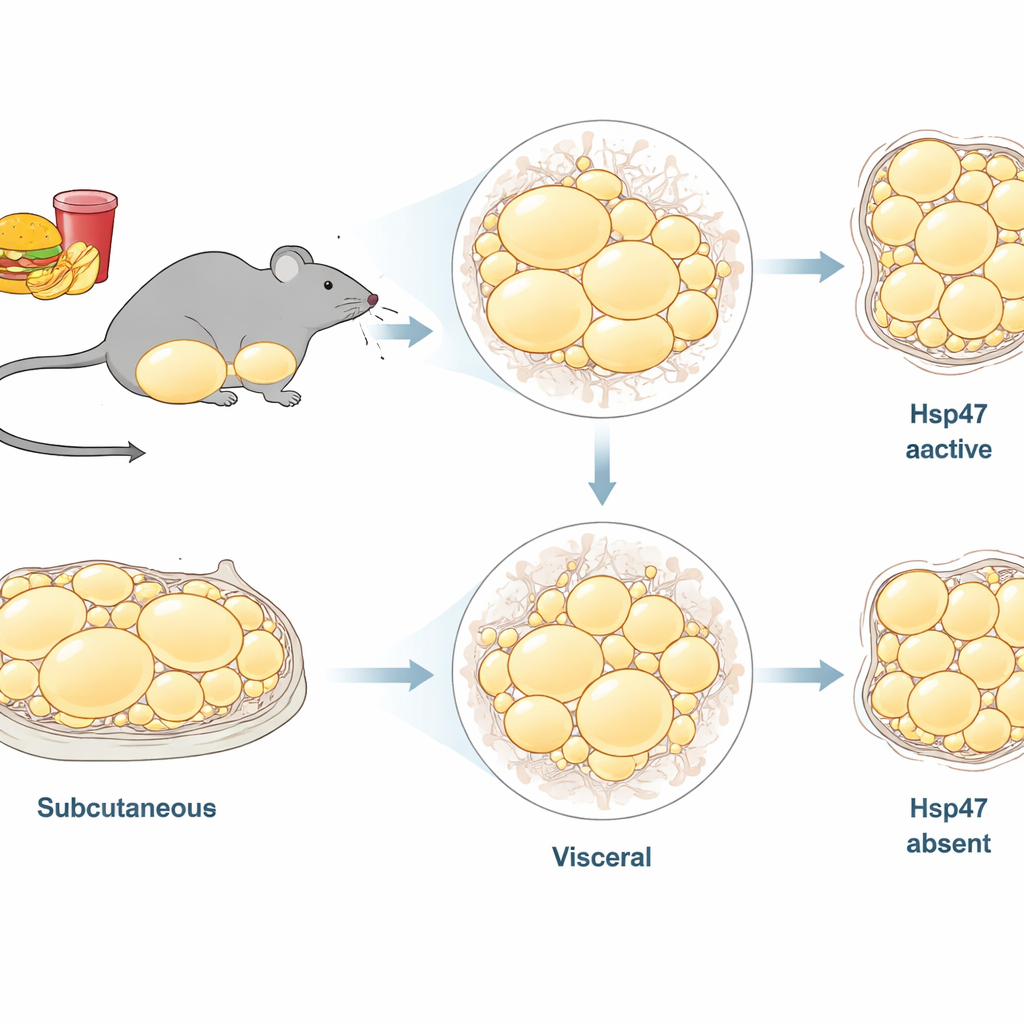
Hsp47 uitschakelen in vetcellen
Om de rol van Hsp47 te testen, bouwde het team muizen waarin Hsp47 alleen uit rijpe vetcellen kon worden verwijderd, terwijl andere weefsels intact bleven. Deze adipocytspecifieke knockout (aKO) muizen en hun normale (flox) nestgenoten kregen gedurende 12 weken ofwel een standaarddieet of een hoog-vet-dieet, lang genoeg om vroege ontsteking en collageenveranderingen te veroorzaken. Onder het hoog-vet-dieet steeg het Hsp47-niveau specifiek in vetweefsels, maar niet in de nier of long. Belangrijk is dat het verwijderen van Hsp47 in vetcellen geen tekenen van cellulair stress in die cellen veroorzaakte, wat suggereert dat vetweefsel verminderde collageen-chaperonnering kan verdragen, in tegenstelling tot collageenrijke weefsels zoals kraakbeen of bot.
Waar Hsp47 het meeste kwaad doet
De meest opvallende resultaten verschenen in het subcutane ingWAT. Bij normale muizen zorgde een vetrijk dieet ervoor dat vetcellen in beide depots opzwollen (hypertrofie). Bij aKO-muizen weigerden de ingWAT-cellen echter uit te zetten, terwijl epiWAT nog steeds groter werd. Wanneer de onderzoekers weefselsecties kleurden om collageen te visualiseren, vonden ze dat het hoog-vet-dieet nog geen massale collageenopbouw veroorzaakte in het algemeen, maar binnen ingWAT hadden de aKO-dieren minder collageen-positief gebied dan de controles. Genexpressie-analyses bevestigden dit depotspecifieke patroon: in ingWAT verminderde verlies van Hsp47 de collageengen bescheiden en verlaagde duidelijk ontstekings- en matrixgerelateerde genen zoals interleukine-6, tumor necrose factor, Ccl2 en fibronectine. In epiWAT daarentegen had Hsp47-deletie weinig invloed op deze transcripties. 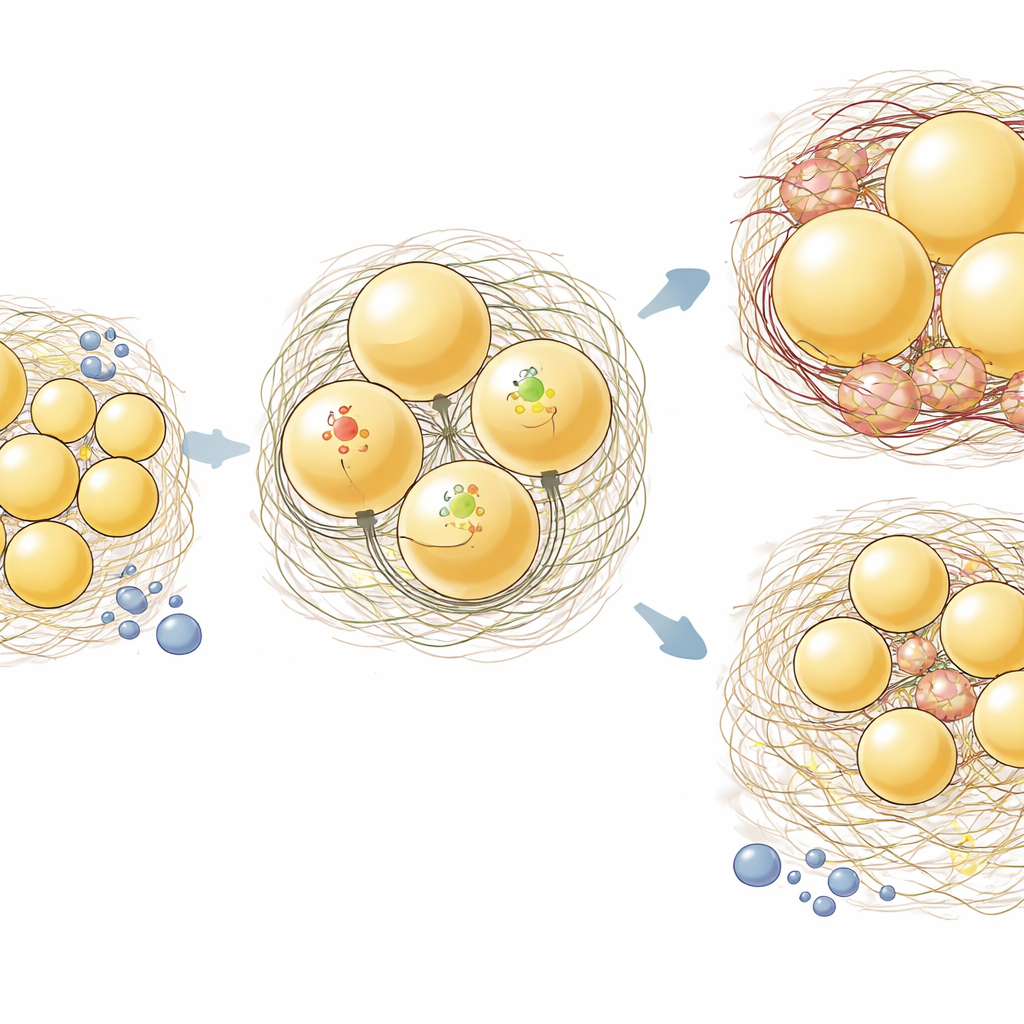
Van lokale vetveranderingen naar lichaamwijde stress
Omdat vetweefsel via hormonen en ontstekingssignalen met de rest van het lichaam communiceert, bekeken de onderzoekers vervolgens bloed- en urinechemie. Zoals verwacht verstoorde hoog-vet-voeding bij controlemuizen meerdere bloedmarkers, waaronder glucose en mineralen die samenhangen met vroege nierbelasting. Bij de aKO-muizen werden enkele van deze verstoringen verzacht: anorganisch fosfaat- en calciumspiegels verschanen naar normalere waarden, en verschillende urinemarkers duidden op minder niergerelateerde stress. De gegevens toonden nog geen duidelijke structurele bescherming in de nier zelf, maar wijzen op een keten van gebeurtenissen waarbij Hsp47-gedreven hermodellering en ontsteking in ingWAT onevenredig bijdragen aan lichaamwijde metabole en mineraalonevenwichtigheden.
Wat dit kan betekenen voor de behandeling van obesitas
Al met al onthult de studie Hsp47 als een belangrijke versterker van ongezonde veranderingen in het vetgeraamte onder een vetrijk dieet, met name in subcutaan ingWAT. Wanneer Hsp47 actief is, wordt collageen rond vetcellen talrijker en waarschijnlijk stijver, vetcellen worden groter en ontstekingsgenen gaan aan, waardoor het lichaam richting systemische problemen wordt geduwd. Wanneer Hsp47 alleen uit vetcellen wordt verwijderd, worden deze processen gedempt, zonder duidelijke problemen onder normale dieetcondities. Aangezien kleine-molecuul medicijnen die Hsp47 blokkeren al experimenteel bestaan, suggereren deze bevindingen een veelbelovende strategie: het selectief dempen van Hsp47-activiteit zou schadelijke vetweefselhermodellering en ontsteking bij obesitas kunnen verminderen terwijl de dagelijkse vetfunctie grotendeels intact blijft.
Bronvermelding: Ito, S., Kamei, R., Kasai, A. et al. Collagen-specific molecular chaperone Hsp47 in inguinal white adipose tissue promotes high-fat diet-induced inflammatory gene expression in male mice. Sci Rep 16, 14301 (2026). https://doi.org/10.1038/s41598-026-45003-4
Trefwoorden: obesitas, vetweefsel, collageen, ontsteking, metabole ziekte