Clear Sky Science · pl
Specyficzna dla kolagenu molekularna chaperona Hsp47 w pachwinowej białej tkance tłuszczowej sprzyja indukowanej dietą wysokotłuszczową ekspresji genów zapalnych u samców myszy
Dlaczego ukryte rusztowanie tkanki tłuszczowej ma znaczenie
Otyłość często określa się jako „nadmiar tłuszczu”, ale to, co dzieje się wewnątrz naszej tkanki tłuszczowej, jest znacznie bardziej złożone. Komórki tłuszczowe żyją w obrębie elastycznego białkowego rusztowania, które przy długotrwałej diecie wysokotłuszczowej może stawać się sztywniejsze, zapalne i ostatecznie szkodzić organizmowi. W pracy tej skupiono się na mniej znanej cząsteczce, Hsp47, która pomaga budować to rusztowanie, kierując produkcją kolagenu. Na modelu myszy karmionych dietą wysokotłuszczową badacze postawili proste pytanie o dalekosiężnych konsekwencjach: czy ograniczenie Hsp47 w komórkach tłuszczowych chroni organizm przed uszkodzeniami wywołanymi dietą?
Bliższe spojrzenie na depozyty tłuszczu
Nie cały tłuszcz w organizmie jest taki sam. Badacze skupili się na dwóch głównych depozytach tłuszczu u samców myszy: tkance podskórnej w okolicy pachwiny (pachwinowa biała tkanka tłuszczowa, ingWAT) oraz głębszym tłuszczu brzusznym otaczającym narządy (jajnikowo-nasieniowodowa biała tkanka tłuszczowa, epiWAT). Wcześniejsze prace wykazały, że dieta wysokotłuszczowa zwiększa aktywność genów kodujących kolagen i inne składniki rusztowania w tłuszczu, co sugeruje, że przebudowa strukturalna jest istotna dla otyłości. Hsp47 to białko pomocnicze wewnątrzkomórkowe, które zapewnia poprawne fałdowanie kolagenu przed jego wydzieleniem. Wiadomo, że napędza procesy bliznowacenia w narządach, takich jak wątroba, ale jego długoterminowa rola w różnych depozytach tłuszczu przy przewlekłym przejadaniu była niejasna. 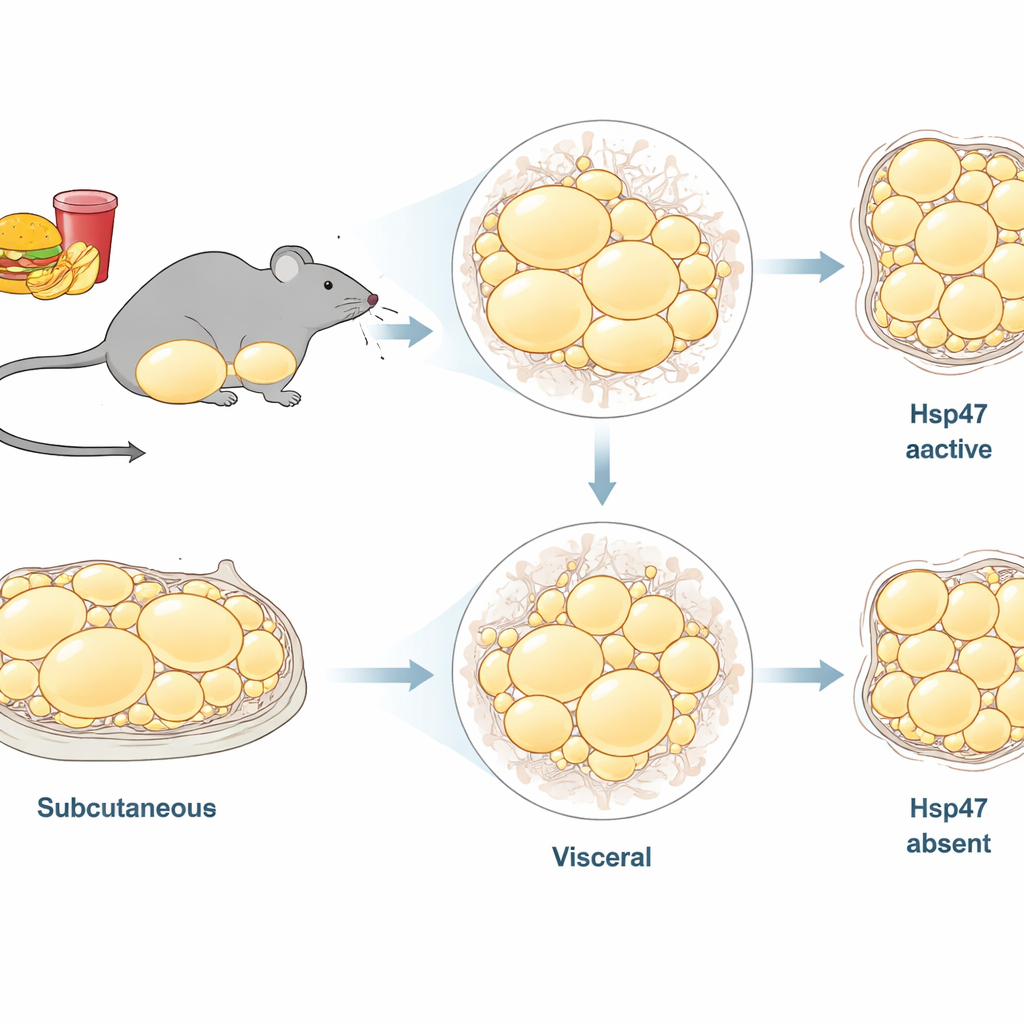
Wyłączanie Hsp47 w komórkach tłuszczowych
Aby przetestować rolę Hsp47, zespół stworzył myszy, u których Hsp47 można było usunąć wyłącznie z dojrzałych komórek tłuszczowych, pozostawiając inne tkanki nienaruszone. Te myszy z adipozytowo-specyficznym wyłączeniem genu (aKO) oraz ich normalne (flox) laktacyjne kontrolne rodzeństwo karmiono albo dietą standardową, albo dietą wysokotłuszczową przez 12 tygodni — wystarczająco długo, by wywołać wczesne zapalenie i zmiany w kolagenie. Przy diecie wysokotłuszczowej poziomy Hsp47 wzrastały specyficznie w tkankach tłuszczowych, ale nie w nerce ani płucu. Co istotne, usunięcie Hsp47 w komórkach tłuszczowych nie wywołało objawów stresu wewnątrzkomórkowego w tych komórkach, co sugeruje, że tkanka tłuszczowa może tolerować zmniejszone wsparcie przy fałdowaniu kolagenu, w przeciwieństwie do tkanek bogatych w kolagen, takich jak chrząstka czy kość.
Gdzie Hsp47 szkodzi najbardziej
Najbardziej uderzające wyniki pojawiły się w podskórnej ingWAT. U myszy kontrolnych dieta wysokotłuszczowa powodowała powiększenie komórek tłuszczowych (hipertrofię) w obu depozytach. U myszy aKO jednak komórki ingWAT przeciwstawiały się temu powiększeniu, podczas gdy epiWAT nadal się rozrastała. Gdy badacze barwili przekroje tkanki, by uwidocznić kolagen, stwierdzili, że karmienie dietą wysokotłuszczową nie wywołało jeszcze masywnego nagromadzenia kolagenu ogólnie, ale w ingWAT zwierząt aKO obszar dodatni dla kolagenu był mniejszy niż u kontrolnych. Analizy ekspresji genów potwierdziły ten depot-specyficzny wzorzec: w ingWAT utrata Hsp47 nieznacznie zmniejszyła poziomy genów kolagenowych i wyraźnie obniżyła geny zapalne i związane z macierzą zewnątrzkomórkową, takie jak interleukina-6, czynnik martwicy nowotworów, Ccl2 i fibrynogen. W epiWAT natomiast delecja Hsp47 miała niewielki wpływ na te transkrypty. 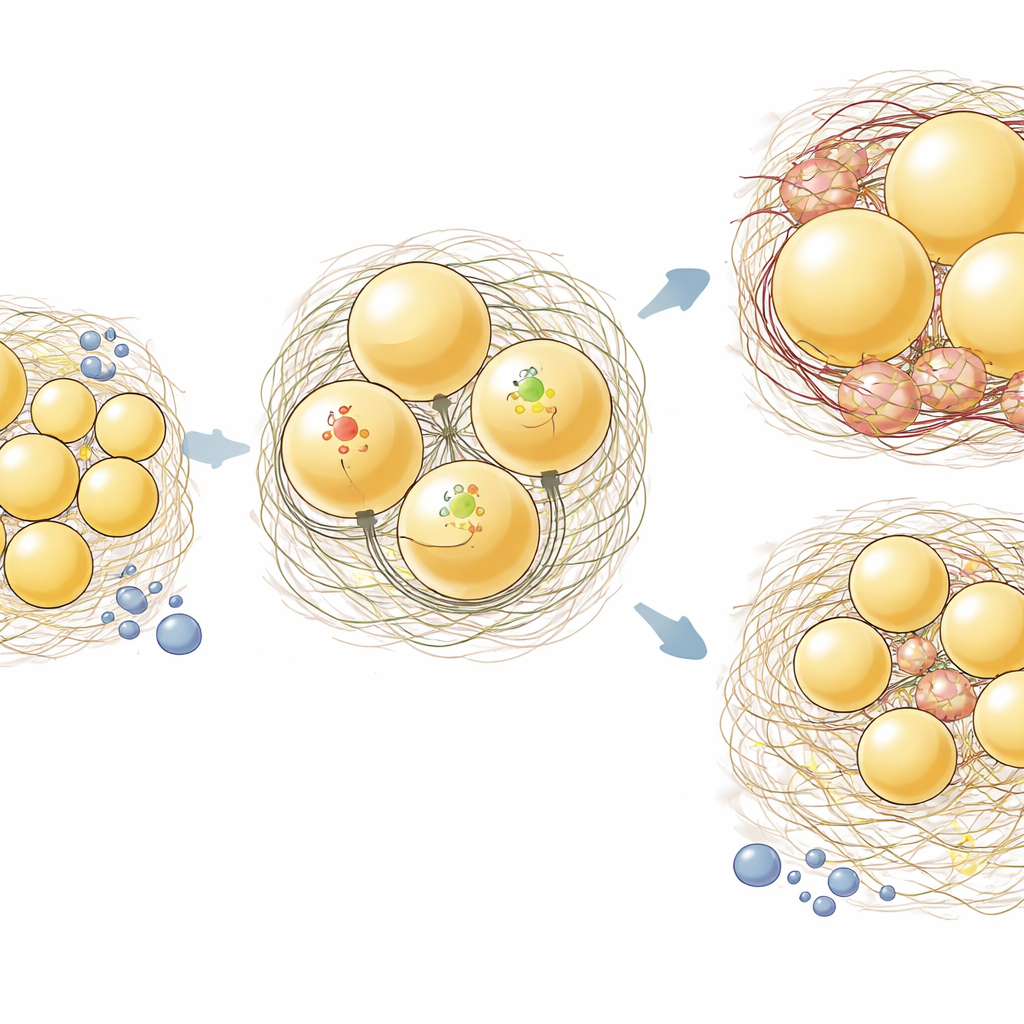
Od lokalnych zmian tłuszczu do stresu całego organizmu
Ponieważ tkanka tłuszczowa komunikuje się z resztą organizmu poprzez hormony i sygnały zapalne, zespół zbadał następnie chemię krwi i moczu. Jak przewidywano, dieta wysokotłuszczowa u myszy kontrolnych zaburzyła wiele markerów krwi, w tym poziomy glukozy i minerałów związanych z wczesnym napięciem nerek. U myszy aKO niektóre z tych zaburzeń uległy złagodzeniu: poziomy fosforanów nieorganicznych i wapnia przesunęły się z powrotem w kierunku normy, a kilka markerów w moczu sugerowało mniejsze obciążenie nerkowe. Dane nie wykazały jeszcze wyraźnej strukturalnej ochrony samej nerki, ale wskazują na łańcuch zdarzeń, w którym przebudowa i zapalenie napędzane przez Hsp47 w ingWAT przyczyniają się nieproporcjonalnie do metabolicznej i mineralnej nierównowagi całego organizmu.
Co to może oznaczać dla leczenia otyłości
Podsumowując, badanie identyfikuje Hsp47 jako kluczowy wzmacniacz niekorzystnych zmian w rusztowaniu tkanki tłuszczowej pod wpływem diety wysokotłuszczowej, zwłaszcza w podskórnym ingWAT. Gdy Hsp47 jest aktywny, kolagen wokół komórek tłuszczowych staje się obfitszy i prawdopodobnie sztywniejszy, komórki tłuszczowe powiększają się, a geny zapalne ulegają aktywacji, popychając organizm w kierunku ogólnoustrojowych problemów. Gdy Hsp47 zostaje usunięty tylko z komórek tłuszczowych, te procesy słabną, bez ewidentnych problemów przy diecie standardowej. Ponieważ dostępne są już w formie eksperymentalnej małe cząsteczki blokujące Hsp47, te ustalenia sugerują obiecującą strategię: selektywne osłabienie aktywności Hsp47 mogłoby złagodzić szkodliwe przebudowy i zapalenie tkanki tłuszczowej w otyłości, przy jednoczesnym zachowaniu podstawowych funkcji tłuszczu.
Cytowanie: Ito, S., Kamei, R., Kasai, A. et al. Collagen-specific molecular chaperone Hsp47 in inguinal white adipose tissue promotes high-fat diet-induced inflammatory gene expression in male mice. Sci Rep 16, 14301 (2026). https://doi.org/10.1038/s41598-026-45003-4
Słowa kluczowe: otyłość, tkanka tłuszczowa, kolagen, zapalenie, choroba metaboliczna