Clear Sky Science · ru
Специфический коллагеновый молекулярный шаперон Hsp47 в паховой белой жировой ткани усиливает индукцию провоспалительной генетической программы при высокожировой диете у самцов мышей
Почему важна скрытая «опора» жировой ткани
Ожирение часто сводят к «избытку жира», но происходящие внутри жировой ткани процессы гораздо сложнее. Адипоциты живут в гибком протеиновом каркасе, и при длительной высокожировой диете этот каркас может уплотняться, воспаляться и в конце концов причинять вред организму. В этом исследовании внимание сосредоточено на малоизвестной молекуле Hsp47, которая помогает строить этот каркас, направляя синтез коллагена. На мышах, получавших высокожировую диету, авторы задали простой вопрос с важными последствиями: защищает ли ослабление Hsp47 в жировых клетках организм от повреждений, вызванных диетой?
Ближе к разным жировым депо
Не весь жир в организме одинаков. Исследователи сосредоточились на двух основных депо у самцов мышей: подкожной жировой ткани в паховой области (inguinal white adipose tissue, ingWAT) и глубокой брюшной жировой ткани вокруг органов (epididymal white adipose tissue, epiWAT). Предыдущие работы показали, что высокожировая диета усиливает экспрессию генов коллагена и других компонентов матрикса в жировой ткани, что указывает на ключевую роль структурной перестройки в ожирении. Hsp47 — внутриклеточный белок-помощник, который обеспечивает правильную сворачивание коллагена перед его секрецией. Известно, что он способствует фиброзу в органах, например в печени, но его долгосрочная роль в разных жировых депо при хроническом переедании оставалась неясной. 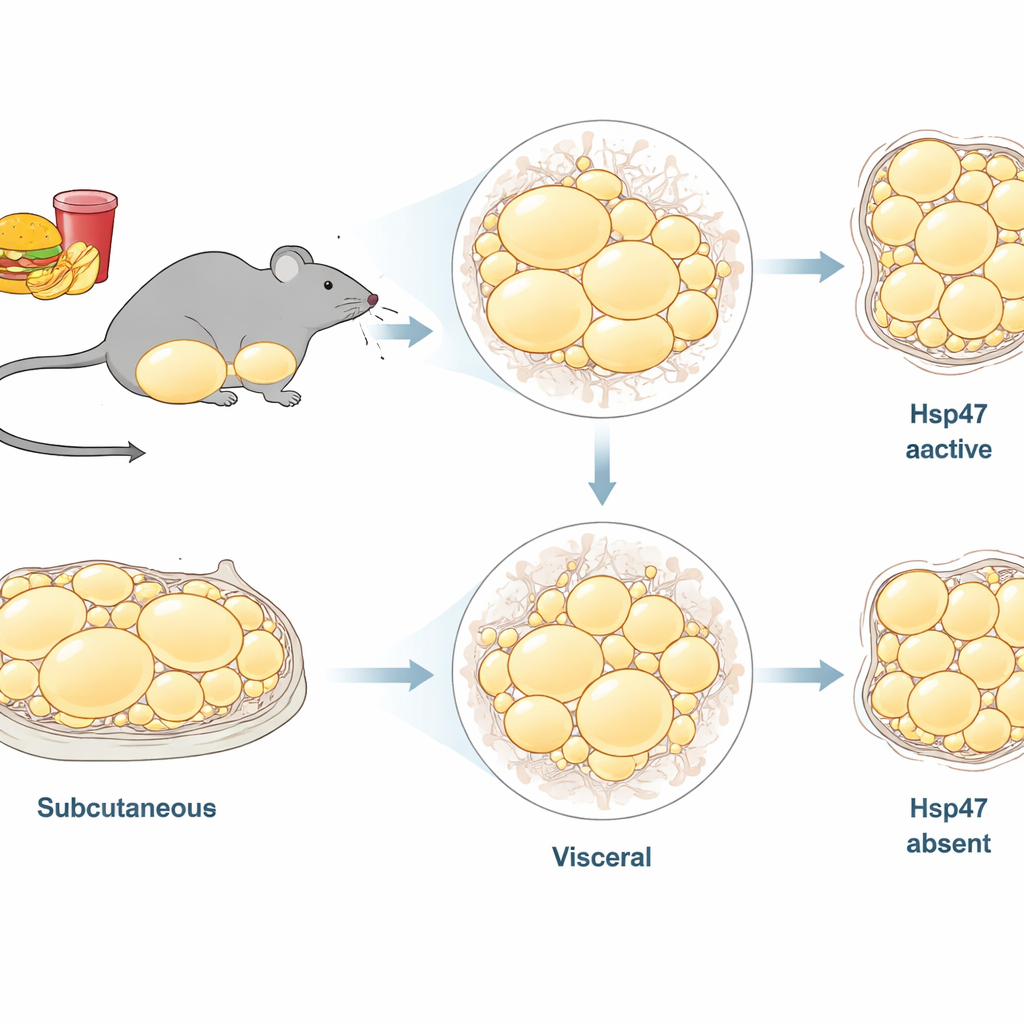
Отключение Hsp47 в адипоцитах
Чтобы проверить роль Hsp47, команда создала мышей, у которых Hsp47 можно было удалить исключительно из зрелых жировых клеток, не затрагивая другие ткани. Эти адипоцит-специфические нокауты (aKO) и их нормальные (flox) сибсы получали либо стандартную диету, либо высокожировую в течение 12 недель — сроки, достаточные для запуска раннего воспаления и изменений коллагена. При высокожировой диете уровни Hsp47 повышались именно в жировой ткани, но не в почке или лёгком. Важно, что удаление Hsp47 в жировых клетках не вызвало признаков внутриклеточного стресса, что говорит о том, что жировая ткань может выдерживать снижение шаперонной поддержки коллагена, в отличие от тканей с большим содержанием коллагена, таких как хрящ или кость.
Где Hsp47 приносит наибольший вред
Наиболее заметные результаты наблюдались в подкожной ingWAT. У нормальных мышей высокожировая диета вызывала увеличение (гипертрофию) жировых клеток в обоих депо. У aKO мышей, однако, клетки ingWAT сопротивлялись этому расширению, тогда как epiWAT по-прежнему увеличивалась. При окраске срезов ткани для визуализации коллагена выяснилось, что общая массивная его депозиция ещё не наступила, но в ingWAT у aKO животных площадь, положительная по коллагену, была меньше, чем у контроля. Анализ экспрессии генов подтвердил этот депо-специфический паттерн: в ingWAT потеря Hsp47 умеренно снизила уровни генов коллагена и заметно уменьшила экспрессию провоспалительных и матрикс-ассоциированных генов, таких как интерлейкин-6, фактор некроза опухоли, Ccl2 и фибронектин. В epiWAT, напротив, удаление Hsp47 мало повлияло на эти транскрипты. 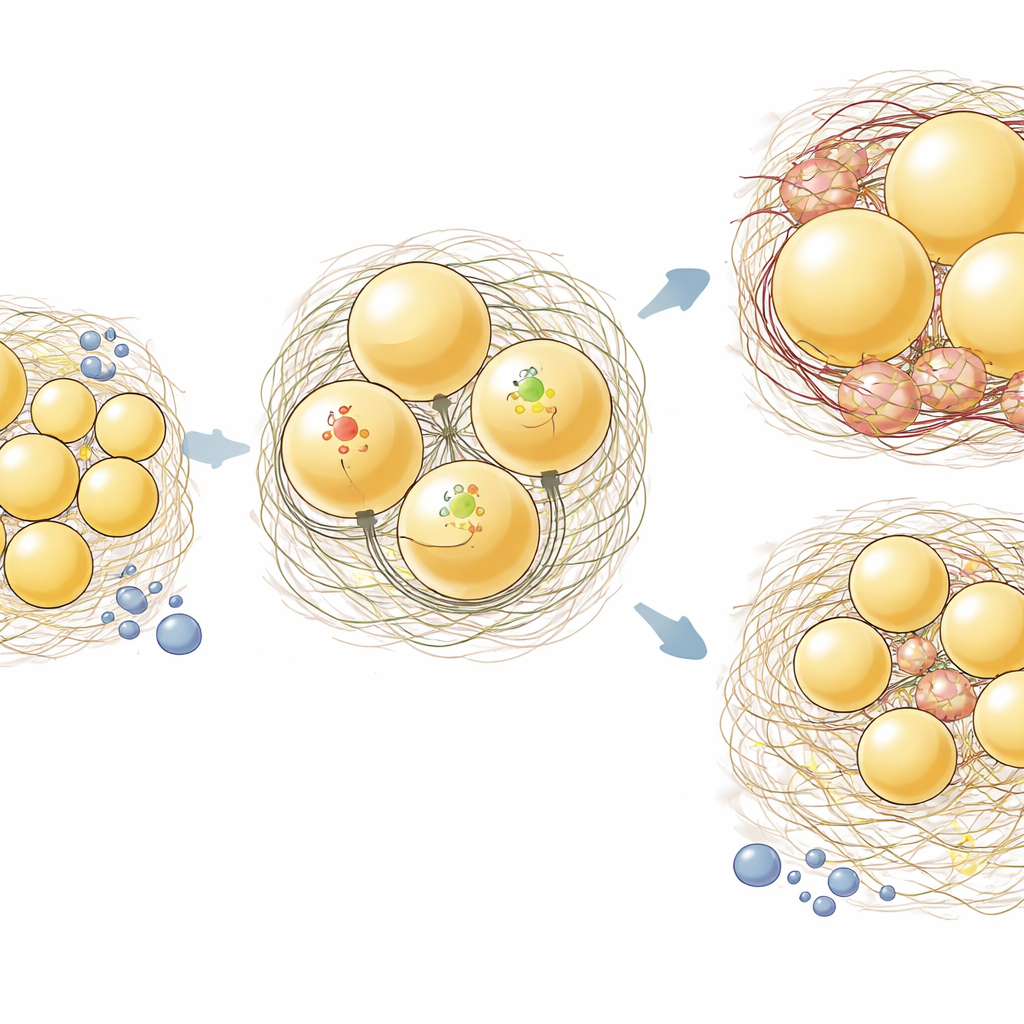
От локальных изменений жира к стрессу всего организма
Поскольку жировая ткань общается с остальным организмом через гормоны и провоспалительные сигналы, команда далее изучила кровь и мочу. Как и следовало ожидать, у контрольных мышей высокожировая диета нарушала несколько кровяных маркеров, включая глюкозу и минеральные уровни, связанные с ранним напряжением почек. У aKO мышей некоторые из этих нарушений смягчились: уровни неорганического фосфата и кальция сместились обратно в сторону нормы, и несколько мочевых маркеров указывали на меньшее почечное напряжение. Данные ещё не демонстрировали явной структурной защиты самой почки, но они указывают на цепочку событий, в которой ремоделирование и воспаление ingWAT, опосредованные Hsp47, вносят непропорциональный вклад в системный метаболический и минеральный дисбаланс.
Что это может означать для лечения ожирения
В целом исследование выявляет Hsp47 как ключевой усилитель неблагоприятных изменений в «опоре» жировой ткани при высокожировой диете, особенно в подкожной ingWAT. Когда Hsp47 активен, коллаген вокруг жировых клеток становится более обильным и, вероятно, более жёстким, адипоциты увеличиваются в размерах, и включаются провоспалительные гены, подталкивая организм к системным проблемам. При удалении Hsp47 только из жировых клеток эти процессы приглушаются, без очевидных проблем при обычной диете. Поскольку малые молекулы, блокирующие Hsp47, уже существуют в экспериментальной форме, эти результаты предлагают перспективную стратегию: выборочное подавление активности Hsp47 может смягчить вредную перестройку и воспаление жировой ткани при ожирении, сохраняя при этом повседневные функции жира в целом.
Цитирование: Ito, S., Kamei, R., Kasai, A. et al. Collagen-specific molecular chaperone Hsp47 in inguinal white adipose tissue promotes high-fat diet-induced inflammatory gene expression in male mice. Sci Rep 16, 14301 (2026). https://doi.org/10.1038/s41598-026-45003-4
Ключевые слова: ожирение, жировая ткань, коллаген, воспаление, метаболическое заболевание