Clear Sky Science · de
Collagen-spezifischer molekularer Chaperon Hsp47 im inguinalen weißen Fettgewebe fördert bei männlichen Mäusen die durch fettreiche Ernährung induzierte Expression entzündlicher Gene
Warum das versteckte Gerüst des Fettgewebes wichtig ist
Adipositas wird oft als „überflüssiges Fett“ beschrieben, doch innerhalb unseres Fettgewebes läuft deutlich komplexeres ab. Fettzellen leben in einem flexiblen Protein-Gerüst; bei langfristiger fettreicher Ernährung kann dieses Gerüst versteifen, sich entzünden und schließlich dem Körper schaden. Diese Studie konzentriert sich auf ein weniger bekanntes Molekül, Hsp47, das den Aufbau dieses Gerüsts unterstützt, indem es die Kollagenproduktion steuert. An Hand von Mäusen auf fettreicher Kost stellten die Forschenden eine einfache Frage mit weitreichenden Folgen: Schützt eine Herunterregulierung von Hsp47 in Fettzellen den Körper vor ernährungsinduzierten Schäden?
Ein genauerer Blick auf Fettdepots
Nicht jedes Körperfett ist gleich. Die Forschenden konzentrierten sich auf zwei wichtige Fettdepots bei männlichen Mäusen: subkutanes Fett unter der Haut in der Leistengegend (inguinales weißes Fettgewebe, ingWAT) und tiefer liegendes Bauchfett, das die Organe umgibt (epididymales weißes Fettgewebe, epiWAT). Frühere Arbeiten zeigten, dass eine fettreiche Ernährung Gene für Kollagen und andere Gerüstbestandteile in Fettgewebe hochfährt, was darauf hindeutet, dass strukturelles Remodeling zentral für die Adipositas ist. Hsp47 ist ein Hilfsprotein innerhalb von Zellen, das sicherstellt, dass Kollagen korrekt gefaltet wird, bevor es sekretiert wird. Es ist bekannt dafür, Fibrosen in Organen wie der Leber zu fördern, aber seine langfristige Rolle in verschiedenen Fettdepots bei chronischer Überernährung war unklar. 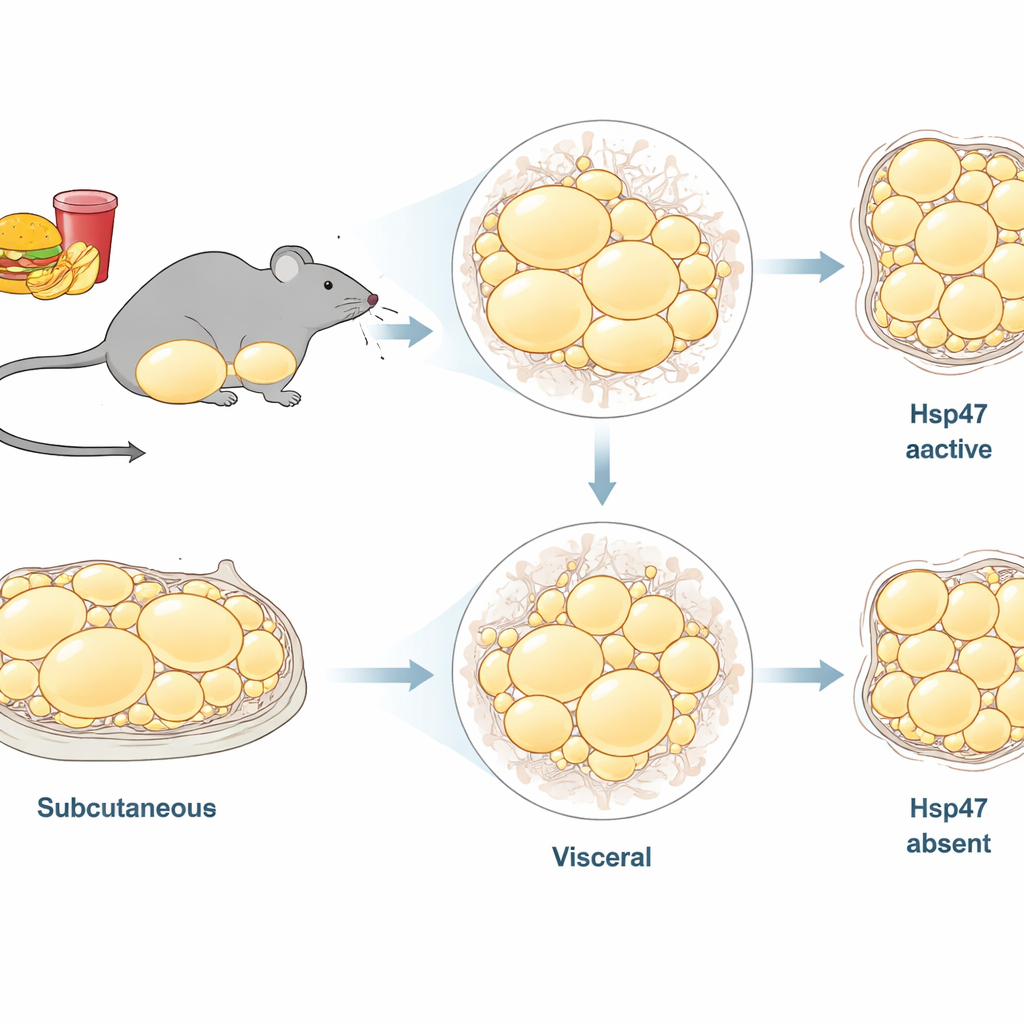
Hsp47 in Fettzellen ausschalten
Um die Rolle von Hsp47 zu prüfen, erzeugte das Team Mäuse, bei denen Hsp47 nur in ausgereiften Fettzellen entfernt werden konnte, während andere Gewebe intakt blieben. Diese adipozytenspezifischen Knockout-(aKO)-Mäuse und ihre normalen (flox) Wurfgeschwister wurden entweder mit einer Standarddiät oder einer fettreichen Diät für 12 Wochen gefüttert – lange genug, um frühe Entzündungen und Kollagenveränderungen auszulösen. Unter der fettreichen Diät stiegen die Hsp47-Spiegel spezifisch in Fettgeweben an, nicht jedoch in Niere oder Lunge. Wichtig ist, dass das Entfernen von Hsp47 in Fettzellen keine Anzeichen von zellulärem Stress in diesen Zellen hervorrief, was darauf hindeutet, dass Fettgewebe eine reduzierte Kollagen-Chaperonfunktion tolerieren kann – im Gegensatz zu kollagenreichen Geweben wie Knorpel oder Knochen.
Wo Hsp47 am schädlichsten wirkt
Die auffälligsten Ergebnisse zeigten sich im subkutanen ingWAT. Bei normalen Mäusen führte eine fettreiche Diät dazu, dass Fettzellen in beiden Depots anschwollen (Hypertrophie). Bei den aKO-Mäusen jedoch widersetzten sich die ingWAT-Zellen dieser Vergrößerung, während das epiWAT weiterhin anwuchs. Als die Forschenden Gewebeschnitte anfärbten, um Kollagen sichtbar zu machen, stellten sie fest, dass die fettreiche Ernährung noch nicht zu einem massiven Kollagenaufbau insgesamt führte, aber im ingWAT hatten die aKO-Tiere eine geringere kollagenpositive Fläche als die Kontrollen. Analysen der Genexpression bestätigten dieses depot-spezifische Muster: Im ingWAT verringerte der Verlust von Hsp47 moderat Kollagen-Gene und senkte deutlich entzündliche und matrixbezogene Gene wie Interleukin-6, Tumornekrosefaktor, Ccl2 und Fibronectin. Im epiWAT hingegen hatte die Hsp47-Deletion wenig Einfluss auf diese Transkripte. 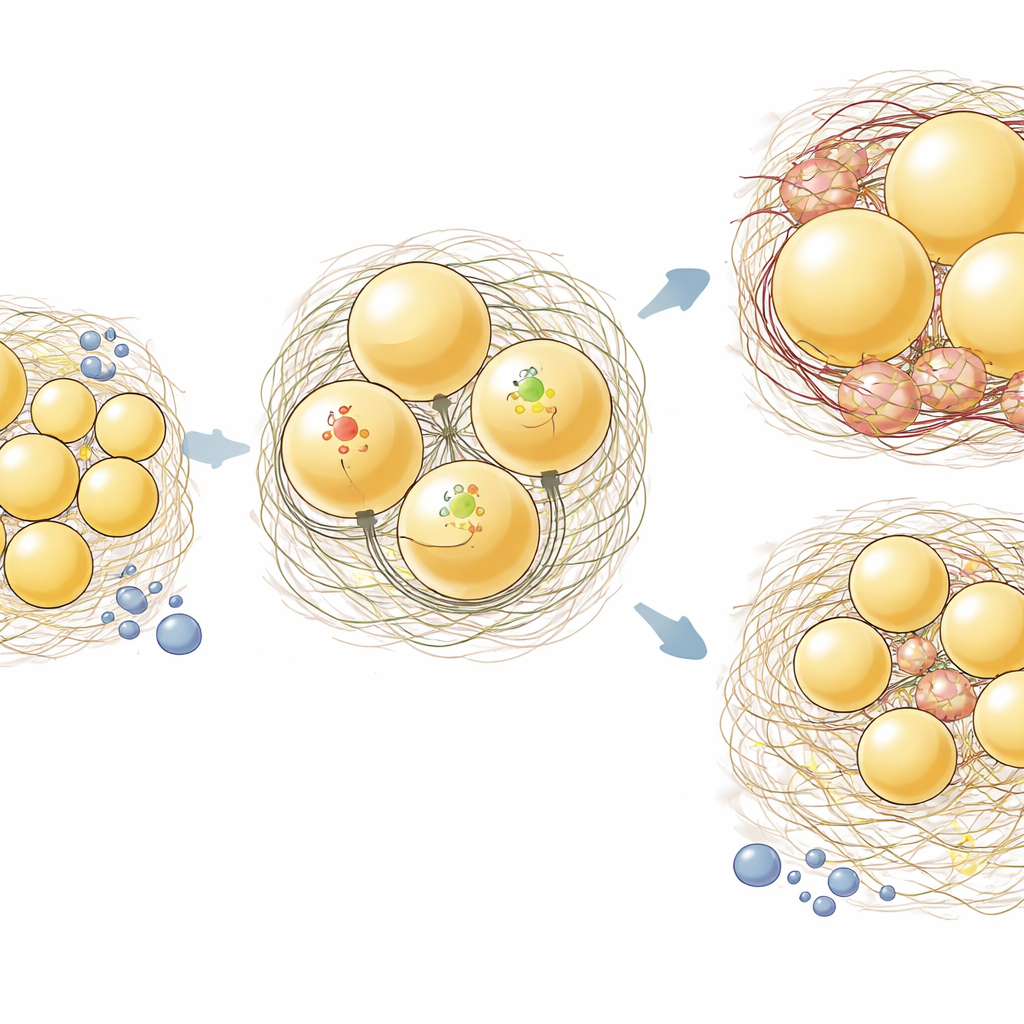
Von lokalen Fettveränderungen zum Stress des ganzen Körpers
Da Fettgewebe über Hormone und entzündliche Signale mit dem übrigen Körper kommuniziert, untersuchte das Team anschließend Blut- und Harnwerte. Wie erwartet störte fettreiche Ernährung bei Kontrollmäusen mehrere Blutmarker, darunter Glukose und Mineralstoffwerte, die mit frühem Nierendruck in Verbindung stehen. Bei den aKO-Mäusen wurden einige dieser Störungen abgeschwächt: anorganisches Phosphat und Kalzium verschoben sich wieder in Richtung Normalwerte, und mehrere Harnmarker deuteten auf weniger nierenbezogenen Stress hin. Die Daten zeigten noch keinen klaren strukturellen Schutz in der Niere selbst, deuten jedoch auf eine Ereigniskette hin, in der Hsp47-getriebenes Remodeling und Entzündung im ingWAT überproportional zu metabolischen und mineralischen Ungleichgewichten des ganzen Körpers beitragen.
Was das für die Behandlung von Adipositas bedeuten könnte
Insgesamt macht die Studie Hsp47 als wichtigen Verstärker ungesunder Veränderungen im Fettgerüst unter fettreicher Ernährung aus, besonders im subkutanen ingWAT. Wenn Hsp47 aktiv ist, wird das Kollagen um Fettzellen dichter und wahrscheinlich steifer, Fettzellen vergrößern sich und entzündliche Gene werden aktiviert, was den Körper in systemische Probleme schubst. Wird Hsp47 hingegen nur in Fettzellen entfernt, werden diese Prozesse gedämpft, ohne offensichtliche Probleme unter Normaldiätbedingungen. Da es bereits experimentelle kleinmolekulare Hemmstoffe von Hsp47 gibt, legen diese Befunde eine vielversprechende Strategie nahe: eine selektive Abschwächung der Hsp47-Aktivität könnte schädliches Remodeling und Entzündung des Fettgewebes bei Adipositas mildern, während die alltägliche Fettfunktion weitgehend erhalten bliebe.
Zitation: Ito, S., Kamei, R., Kasai, A. et al. Collagen-specific molecular chaperone Hsp47 in inguinal white adipose tissue promotes high-fat diet-induced inflammatory gene expression in male mice. Sci Rep 16, 14301 (2026). https://doi.org/10.1038/s41598-026-45003-4
Schlüsselwörter: Adipositas, Fettgewebe, Kollagen, Entzündung, metabolische Erkrankung