Clear Sky Science · fr
Chaperonne moléculaire spécifique du collagène Hsp47 dans le tissu adipeux blanc inguinal favorise l’expression des gènes inflammatoires induite par un régime riche en graisses chez la souris mâle
Pourquoi l’armature cachée du tissu graisseux compte
L’obésité est souvent décrite comme un « excès de graisse », mais ce qui se passe à l’intérieur de notre tissu adipeux est bien plus complexe. Les adipocytes vivent dans une armature protéique souple, et lorsqu’on suit un régime riche en graisses sur le long terme, cette armature peut se rigidifier, s’enflammer et finir par endommager l’organisme. Cette étude se concentre sur une molécule moins connue, Hsp47, qui participe à la construction de cette armature en guidant la production de collagène. En étudiant des souris soumises à un régime riche en graisses, les chercheurs ont posé une question simple aux implications majeures : réduire l’expression de Hsp47 dans les cellules adipeuses protège-t-il l’organisme des dommages induits par le régime ?
Un examen plus attentif des dépôts graisseux
Toute la graisse corporelle n’est pas identique. Les chercheurs se sont focalisés sur deux dépôts majeurs chez la souris mâle : la graisse sous-cutanée sous la peau de l’aine (tissu adipeux blanc inguinal, ou ingWAT) et la graisse viscérale plus profonde entourant les organes (tissu adipeux blanc épididymaire, ou epiWAT). Des travaux antérieurs montraient qu’un régime riche en graisses augmente l’expression des gènes de collagène et d’autres composants de l’armature dans la graisse, suggérant que le remodelage structurel est central dans l’obésité. Hsp47 est une protéine d’aide intracellulaire qui veille au bon repliement du collagène avant sa sécrétion. On sait qu’elle favorise la fibrose d’organes comme le foie, mais son rôle à long terme dans différents dépôts graisseux sous surrégime alimentaire chronique restait obscure. 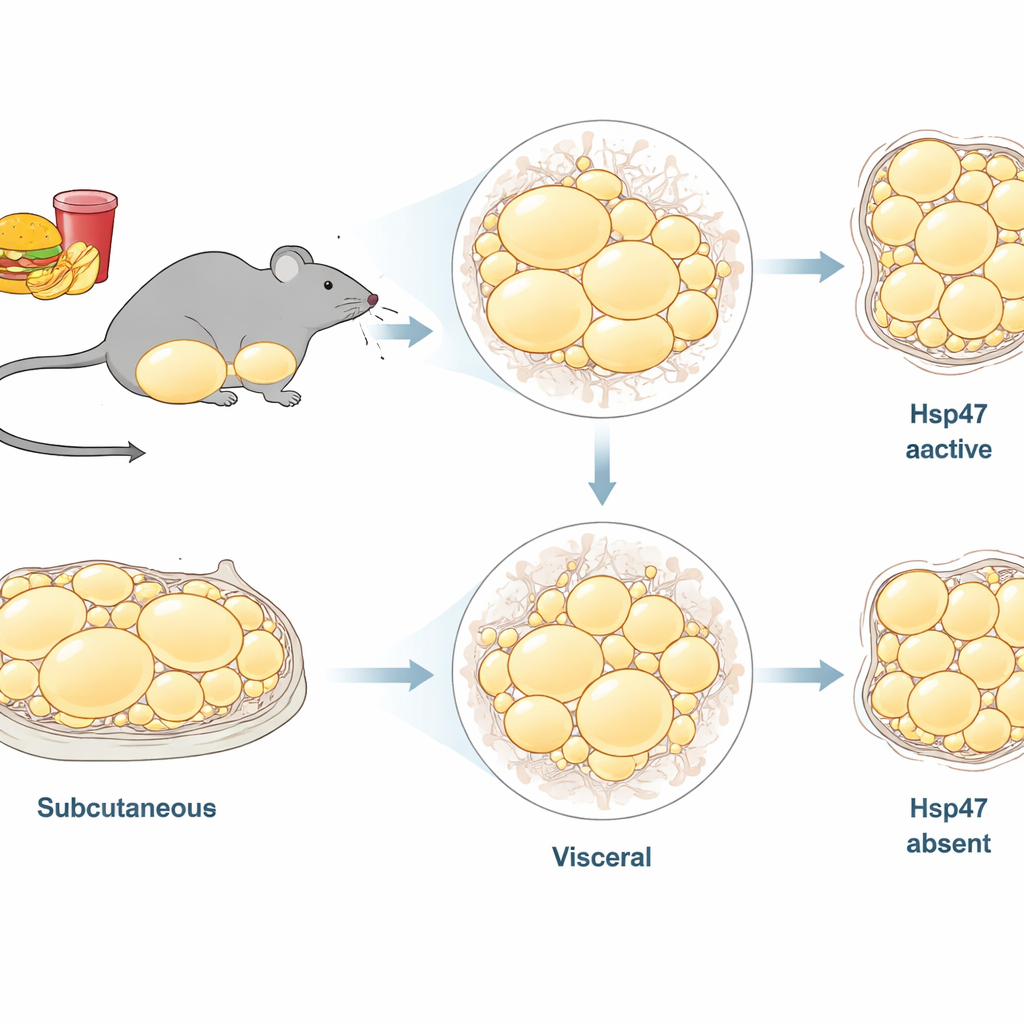
Éteindre Hsp47 dans les cellules graisseuses
Pour tester le rôle de Hsp47, l’équipe a créé des souris permettant de supprimer Hsp47 uniquement dans les adipocytes matures, en laissant les autres tissus intacts. Ces souris à suppression spécifique dans les adipocytes (aKO) et leurs congénères normaux (flox) ont reçu soit une alimentation standard soit un régime riche en graisses pendant 12 semaines, une durée suffisante pour déclencher une inflammation précoce et des modifications du collagène. Sous le régime riche en graisses, les niveaux de Hsp47 augmentaient spécifiquement dans les tissus adipeux, mais pas dans le rein ou le poumon. Fait important, la suppression de Hsp47 dans les cellules adipeuses n’a pas provoqué de signes de stress intracellulaire dans ces cellules, suggérant que le tissu adipeux peut tolérer une réduction du support du collagène, contrairement à des tissus riches en collagène comme le cartilage ou l’os.
Où Hsp47 fait le plus de dégâts
Les résultats les plus frappants sont apparus dans l’ingWAT sous-cutanée. Chez les souris témoins, un régime riche en graisses a provoqué l’hypertrophie des adipocytes dans les deux dépôts. Chez les souris aKO, toutefois, les cellules de l’ingWAT ont résisté à cette expansion, alors que l’epiWAT a continué de croître. Lorsque les chercheurs ont coloré des coupes tissulaires pour visualiser le collagène, ils ont constaté que l’alimentation riche en graisses n’avait pas encore entraîné un important dépôt global de collagène, mais que, dans l’ingWAT, les animaux aKO présentaient une zone positive au collagène plus réduite que les témoins. Les analyses d’expression génique ont renforcé ce schéma spécifique au dépôt : dans l’ingWAT, la perte de Hsp47 a modestement réduit les gènes de collagène et clairement abaissé les gènes inflammatoires et liés à la matrice tels que l’interleukine-6, le facteur de nécrose tumorale, Ccl2 et la fibronectine. En revanche, dans l’epiWAT, la suppression de Hsp47 n’a eu que peu d’effet sur ces transcrits. 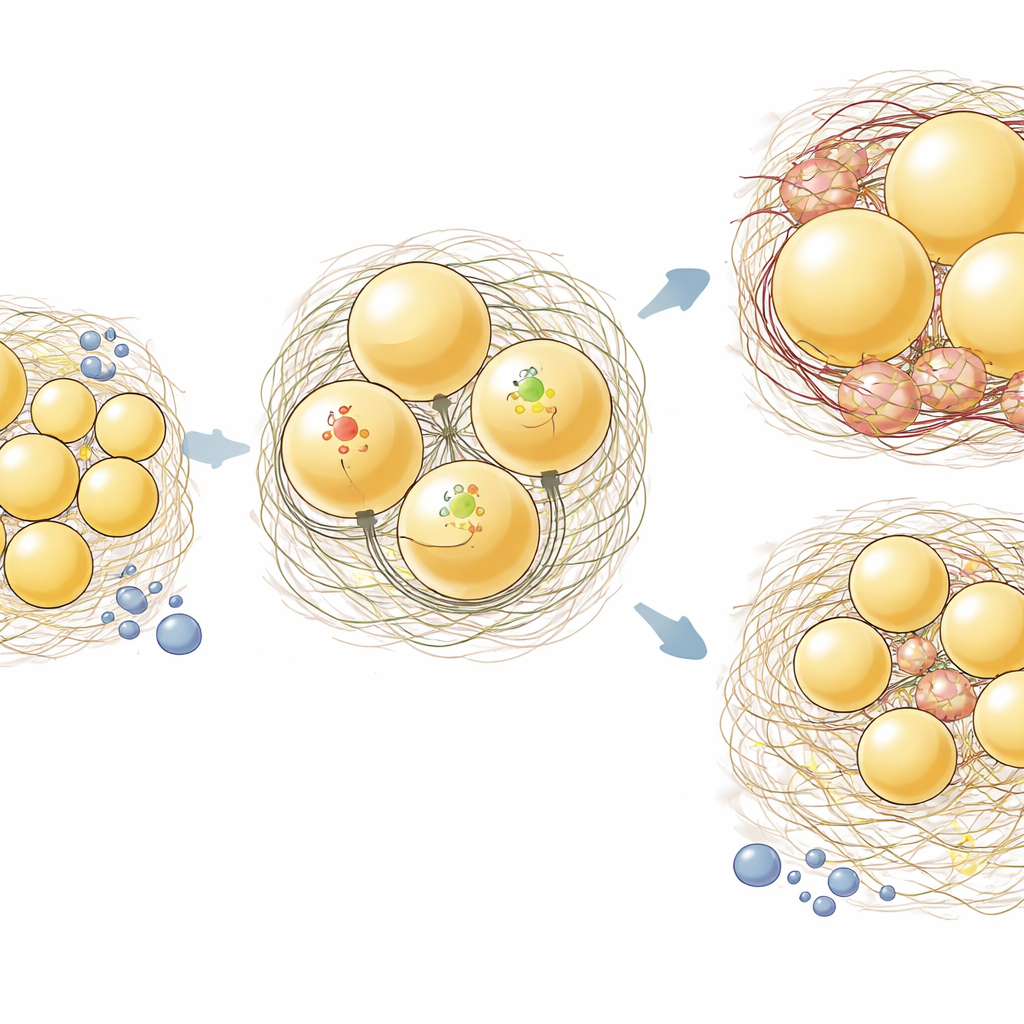
Des changements locaux dans la graisse au stress de tout l’organisme
Parce que le tissu adipeux communique avec le reste de l’organisme via des hormones et des signaux inflammatoires, l’équipe a ensuite examiné la chimie sanguine et urinaire. Comme prévu, le régime riche en graisses chez les témoins a perturbé plusieurs marqueurs sanguins, y compris la glycémie et des minéraux liés à une tension rénale précoce. Chez les souris aKO, certaines de ces perturbations ont été atténuées : les taux de phosphate inorganique et de calcium se sont rapprochés de la normale, et plusieurs marqueurs urinaires suggéraient un stress rénal moindre. Les données ne montraient pas encore de protection structurale évidente au niveau du rein lui-même, mais elles indiquent une chaîne d’événements dans laquelle le remodelage et l’inflammation pilotés par Hsp47 dans l’ingWAT contribuent de manière disproportionnée au déséquilibre métabolique et mineral de l’ensemble de l’organisme.
Ce que cela pourrait signifier pour le traitement de l’obésité
Dans l’ensemble, l’étude révèle Hsp47 comme un amplificateur clé des changements néfastes de l’armature adipeuse sous un régime riche en graisses, en particulier dans l’ingWAT sous-cutanée. Lorsque Hsp47 est actif, le collagène entourant les cellules graisseuses devient plus abondant et probablement plus rigide, les adipocytes grossissent et les gènes inflammatoires s’activent, poussant l’organisme vers des troubles systémiques. Lorsque Hsp47 est supprimé uniquement dans les adipocytes, ces processus sont atténués, sans problèmes évidents sous un régime normal. Comme des petites molécules bloquant Hsp47 existent déjà sous forme expérimentale, ces résultats suggèrent une stratégie prometteuse : moduler sélectivement l’activité de Hsp47 pourrait réduire le remodelage et l’inflammation nocifs du tissu adipeux dans l’obésité tout en préservant largement les fonctions quotidiennes de la graisse.
Citation: Ito, S., Kamei, R., Kasai, A. et al. Collagen-specific molecular chaperone Hsp47 in inguinal white adipose tissue promotes high-fat diet-induced inflammatory gene expression in male mice. Sci Rep 16, 14301 (2026). https://doi.org/10.1038/s41598-026-45003-4
Mots-clés: obésité, tissu adipeux, collagène, inflammation, maladie métabolique