Clear Sky Science · it
La chaperone molecolare specifica per il collagene Hsp47 nel tessuto adiposo bianco inguinale promuove l’espressione di geni infiammatori indotta da una dieta ad alto contenuto di grassi nei topi maschi
Perché conta l’impalcatura nascosta del tessuto adiposo
L’obesità viene spesso descritta come «grasso in eccesso», ma ciò che avviene all’interno del tessuto adiposo è molto più complesso. Le cellule adipose vivono all’interno di un’impalcatura proteica flessibile e, quando seguiamo una dieta ricca di grassi a lungo termine, questa impalcatura può irrigidirsi, infiammarsi e alla fine danneggiare l’organismo. Questo studio si concentra su una molecola meno nota, Hsp47, che aiuta a costruire quell’impalcatura guidando la produzione di collagene. Studiando topi sottoposti a dieta ricca di grassi, i ricercatori si sono posti una domanda semplice ma dalle grandi implicazioni: ridurre l’espressione di Hsp47 nelle cellule adipose protegge l’organismo dai danni indotti dalla dieta?
Uno sguardo più attento ai depositi di grasso
Non tutto il grasso corporeo è uguale. I ricercatori si sono concentrati su due principali depositi di grasso nei topi maschi: il grasso sottocutaneo sotto la pelle nell’area inguinale (tessuto adiposo bianco inguinale, o ingWAT) e il grasso addominale più profondo che circonda gli organi (tessuto adiposo bianco epididimale, o epiWAT). Lavori precedenti avevano mostrato che una dieta ricca di grassi aumenta l’espressione di geni per il collagene e altri componenti dell’impalcatura nel tessuto adiposo, suggerendo che il rimodellamento strutturale è centrale nell’obesità. Hsp47 è una proteina chaperone intracellulare che garantisce il corretto ripiegamento del collagene prima della sua secrezione. È nota per promuovere la formazione di cicatrici in organi come il fegato, ma il suo ruolo a lungo termine nei diversi depositi di grasso durante una condizione cronica di sovralimentazione non era chiaro. 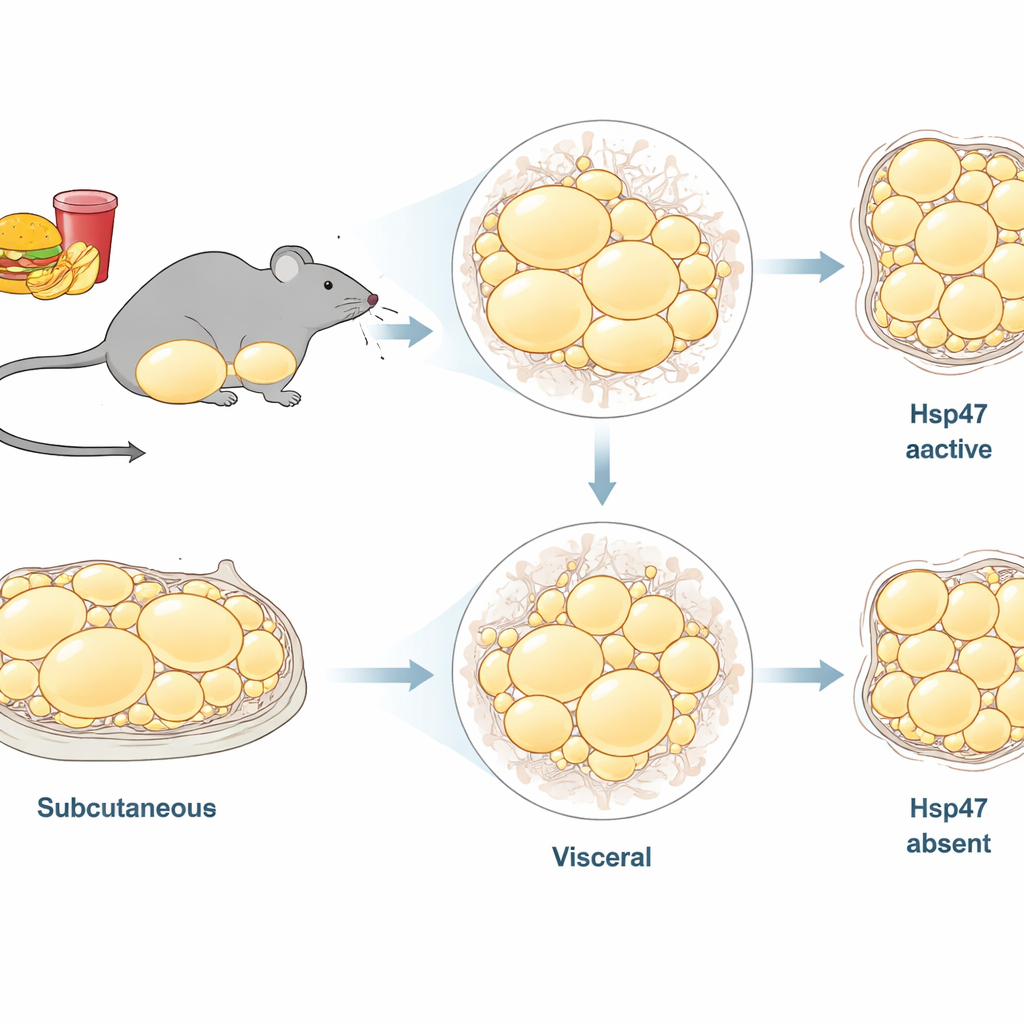
Spegnere Hsp47 nelle cellule adipose
Per testare il ruolo di Hsp47, il gruppo ha ingegnerizzato topi in cui Hsp47 poteva essere rimosso soltanto dalle cellule adipose mature, lasciando intatti gli altri tessuti. Questi topi con delezione specifica negli adipociti (aKO) e i loro fratelli normali (flox) sono stati nutriti con una dieta standard o con una dieta ricca di grassi per 12 settimane, tempo sufficiente a scatenare fasi iniziali di infiammazione e cambiamenti nel collagene. Con la dieta ricca di grassi, i livelli di Hsp47 aumentavano specificamente nei tessuti adiposi, ma non nel rene o nel polmone. È importante che l’eliminazione di Hsp47 nelle cellule adipose non abbia causato segni di stress all’interno di quelle cellule, suggerendo che il tessuto adiposo può tollerare una ridotta assistenza al collagene, diversamente da tessuti ricchi di collagene come cartilagine o osso.
Dove Hsp47 fa più danno
I risultati più marcati sono comparsi nell’ingWAT sottocutaneo. Nei topi normali, una dieta ricca di grassi rendeva gli adipociti in entrambi i depositi più grandi (ipertrofia). Nei topi aKO, invece, le cellule dell’ingWAT resistevano a questa espansione, mentre l’epiWAT continuava ad aumentare di volume. Analisi istologiche per visualizzare il collagene mostrarono che l’alimentazione ricca di grassi non aveva ancora provocato un massiccio accumulo di collagene in generale, ma nell’ingWAT gli animali aKO avevano un’area positiva per il collagene inferiore rispetto ai controlli. Le analisi dell’espressione genica hanno confermato questo pattern specifico del deposito: nell’ingWAT, la perdita di Hsp47 riduceva moderatamente i geni del collagene e diminuiva in modo chiaro geni infiammatori e legati alla matrice come interleuchina-6, fattore di necrosi tumorale, Ccl2 e fibronectina. Nell’epiWAT, invece, la delezione di Hsp47 aveva scarsa influenza su questi trascritti. 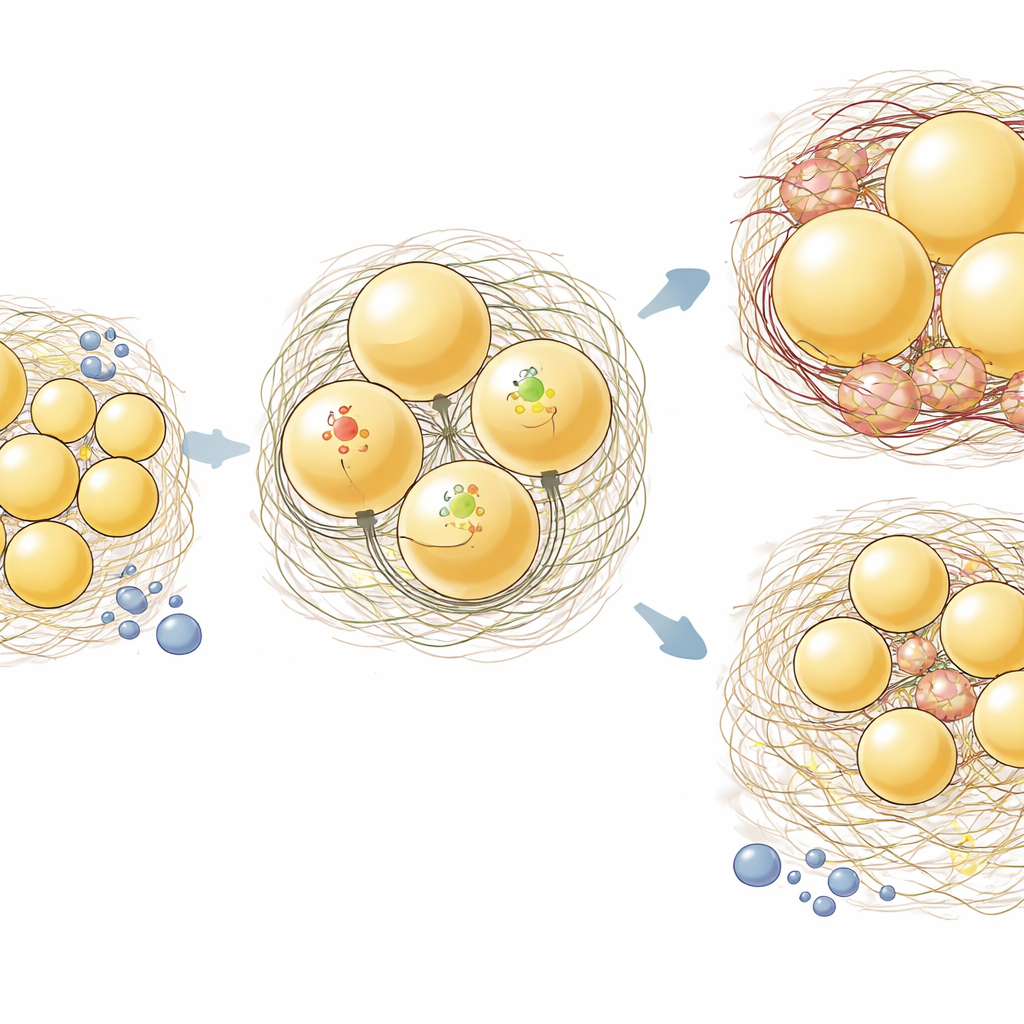
Dai cambi locali nel grasso allo stress sistemico
Poiché il tessuto adiposo comunica con il resto dell’organismo tramite ormoni e segnali infiammatori, il gruppo ha quindi esaminato parametri ematici e urinari. Come previsto, l’alimentazione ricca di grassi nei controlli alterava diversi marker nel sangue, inclusi glucosio e livelli di minerali associati a un precoce stress renale. Nei topi aKO alcune di queste alterazioni risultavano attenuate: livelli di fosfato inorganico e calcio si avvicinavano ai valori normali e diversi marker urinari suggerivano un minore stress legato al rene. I dati non mostravano ancora una chiara protezione strutturale nel rene stesso, ma indicano una catena di eventi nella quale il rimodellamento e l’infiammazione guidati da Hsp47 nell’ingWAT contribuiscono in modo sproporzionato allo squilibrio metabolico e minerale dell’intero organismo.
Cosa potrebbe significare per il trattamento dell’obesità
Nel complesso, lo studio identifica Hsp47 come un amplificatore chiave dei cambiamenti nocivi nell’impalcatura adiposa indotti da una dieta ricca di grassi, in particolare nell’ingWAT sottocutaneo. Con Hsp47 attivo, il collagene intorno agli adipociti diventa più abbondante e probabilmente più rigido, gli adipociti si ingrandiscono e si attivano geni infiammatori, spingendo l’organismo verso problemi sistemici. Quando Hsp47 viene rimosso solo dalle cellule adipose, questi processi risultano attenuati, senza problemi evidenti nelle condizioni di dieta normale. Poiché esistono già in forma sperimentale piccole molecole in grado di inibire Hsp47, questi risultati suggeriscono una strategia promettente: ridurre selettivamente l’attività di Hsp47 potrebbe mitigare il rimodellamento dannoso del tessuto adiposo e l’infiammazione nell’obesità, preservando in larga misura la funzione normale del grasso.
Citazione: Ito, S., Kamei, R., Kasai, A. et al. Collagen-specific molecular chaperone Hsp47 in inguinal white adipose tissue promotes high-fat diet-induced inflammatory gene expression in male mice. Sci Rep 16, 14301 (2026). https://doi.org/10.1038/s41598-026-45003-4
Parole chiave: obesità, tessuto adiposo, collagene, infiammazione, malattia metabolica