Clear Sky Science · zh
单细胞与整体转录组分析揭示与程序性细胞死亡特征相关的肝内胆管癌免疫亚型
这项肝癌研究的重要性
肝内胆管癌起源于肝脏内的小胆管,常进展迅速且常在无法手术的晚期被发现。临床上观察到部分患者生存期更长或对新型免疫治疗反应更好,但很难预测谁能获益。本研究利用先进的基因组学分型与单细胞分析,阐明不同形式的“程序性”细胞死亡与免疫系统在这些肿瘤中的相互作用,并构建了一个实用评分,有望帮助个体化治疗与临床决策。
逐细胞揭示肝肿瘤内部
研究者从公共数据库和一个大型临床队列收集了数百个肿瘤样本的基因表达数据,包括群体组织与单细胞数据。研究聚焦于与21类程序性细胞死亡相关的2,701个基因——细胞在受损或异常时自我毁灭的内在途径。通过将肿瘤组织与邻近非癌肝组织比较,缩减为87个在癌变中异常表达且可能与患者生存相关的基因。这些基因参与已知的癌症通路和如细胞凋亡、坏死性凋亡等细胞死亡形式,并在肝胆管肿瘤中呈现出特定的突变和染色体改变模式。 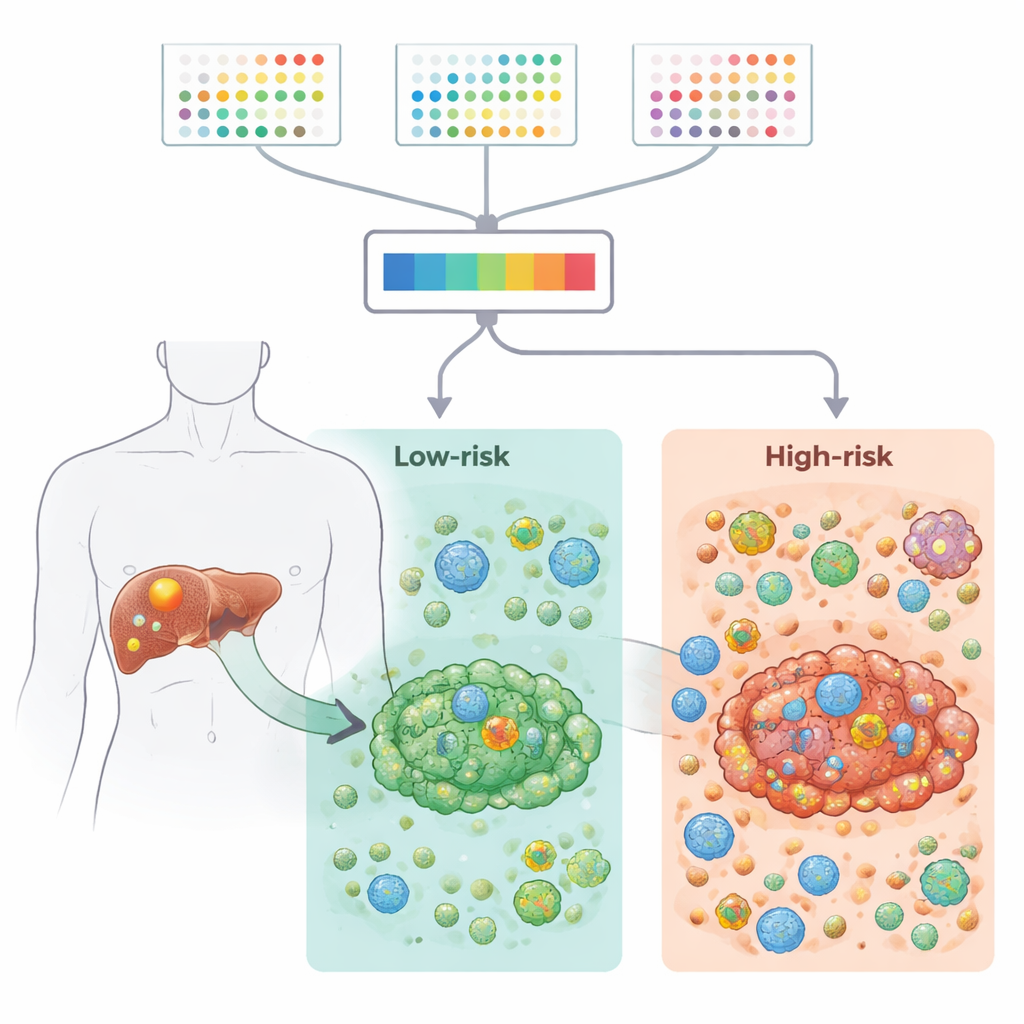
由九个关键基因构建的风险评分
为将复杂信息转化为临床可用的工具,团队测试了117种机器学习方法与生存模型的组合。表现最佳的方法将逐步Cox回归与随机生存森林结合,最终提炼出九个基因。每位患者根据这些基因在肿瘤中表达的高低获得一个风险评分。在多个独立患者队列中,这一九基因特征能可靠地将患者分为高危与低危两组并显示出显著不同的生存期。高风险肿瘤富集于应激与炎症相关通路,而低风险肿瘤则显示更活跃的代谢和解毒通路,提示两组在基本生物学特征上存在差异。
肿瘤内的免疫“社区”
随后研究聚焦肿瘤微环境——围绕并浸润肿瘤的免疫细胞、支持细胞与基质。利用多种计算工具,作者发现高风险肿瘤具有更高的免疫与基质评分、更强的炎症信号以及更多免疫抑制特征,包括增加的调节性T细胞,这类细胞可削弱抗肿瘤反应。单细胞RNA测序确认这些调节性T细胞和成纤维细胞在高风险肿瘤中更为丰富,并且参与密集的细胞间通信网络。相比之下,低风险肿瘤具有更强的胶原相关信号和更平衡、较少抑制性的环境。综上,九基因模式与局部免疫环境对肿瘤是“友好”还是“敌对”密切相关。 
指导免疫治疗与药物选择
鉴于免疫治疗在癌症治疗中的重要性,研究者基于相同的九个基因构建了一个单独的“PCD评分”以预测对免疫检查点抑制剂的反应。在三组使用此类药物(来自具有可用数据的其他癌种)的独立患者队列中,较高的PCD评分始终与更好的治疗反应相关,表明该评分捕捉到了使免疫治疗更可能有效的肿瘤环境特征。团队还利用药物敏感性数据库和计算对接模拟预测不同风险组可能更敏感的药物。高风险患者似乎对某些靶向药物更敏感,包括干扰TGF-β和mTOR信号通路的药物,提示可采用组合策略以克服免疫抑制。
从复杂生物学到实用工具
为帮助将这些发现转化到临床,作者构建了一个列线图——将基因风险评分与常规临床信息如分期与血管侵袭相结合的可视化风险计算器。该工具能在其主要患者队列中准确预测一、三和四年的生存。尽管这项工作仍需在更大规模、治疗定义明确的肝内胆管癌前瞻性队列中验证,但它为如何利用与细胞死亡相关基因模式对肿瘤进行分型、理解其免疫生态并指导治疗提供了蓝图。对患者而言,长期的承诺是基于肿瘤独特的基因与免疫指纹获得更精确的预后判断与更匹配的治疗方案。
引用: Zhang, T., Dou, D., Liu, Q. et al. Single-cell and bulk transcriptomic analyses uncover immune subtypes associated with programmed cell death features in intrahepatic cholangiocarcinoma. Sci Rep 16, 13678 (2026). https://doi.org/10.1038/s41598-026-44332-8
关键词: 肝内胆管癌, 程序性细胞死亡, 肿瘤免疫微环境, 单细胞RNA测序, 免疫治疗反应