Clear Sky Science · pl
Analizy transkryptomiczne pojedynczych komórek i materiału zbiorczego ujawniają podtypy immunologiczne powiązane z cechami programowanej śmierci komórkowej w wewnątrzwątrobowym rakowiaku dróg żółciowych
Dlaczego to badanie raka wątroby ma znaczenie
Wewnątrzwątrobowy rak dróg żółciowych to szybko rosnący nowotwór wywodzący się z małych przewodów żółciowych w obrębie wątroby, często rozpoznawany zbyt późno, by móc wykonać zabieg operacyjny. Lekarze obserwują, że niektórzy pacjenci żyją znacznie dłużej albo lepiej reagują na nowe immunoterapie niż inni, lecz trudno jest przewidzieć, kto skorzysta. W tym badaniu zastosowano zaawansowane profilowanie genetyczne i analizę pojedynczych komórek, aby pokazać, jak różne formy „programowanej” śmierci komórkowej współdziałają z układem odpornościowym w tych guzach, oraz opracowano praktyczny wynik (score), który może pomóc dopasować leczenie i wspierać decyzje kliniczne.
Zajrzeć do wnętrza guzów wątroby komórka po komórce
Naukowcy zgromadzili rozległe zbiory danych aktywności genów z setek próbek nowotworowych, obejmujące zarówno materiał zbiorczy, jak i pojedyncze komórki, pochodzące z zasobów publicznych oraz dużej kohorty klinicznej. Skoncentrowali się na 2701 genach związanych z 21 typami programowanej śmierci komórkowej — wbudowanymi mechanizmami, dzięki którym komórki mogą samodestrukować się, gdy są uszkodzone lub nieprawidłowe. Porównując tkankę guza z przyległą, niezłośliwą wątrobą, zawęzili tę listę do 87 genów, które były zarówno zaburzone w raku, jak i potencjalnie istotne dla przeżycia pacjentów. Geny te brały udział w znanych ścieżkach nowotworowych i formach śmierci komórkowej, takich jak apoptoza i nekroptoza, i wykazywały charakterystyczne wzorce mutacji oraz zmian chromosomalnych w guzach dróg żółciowych wątroby. 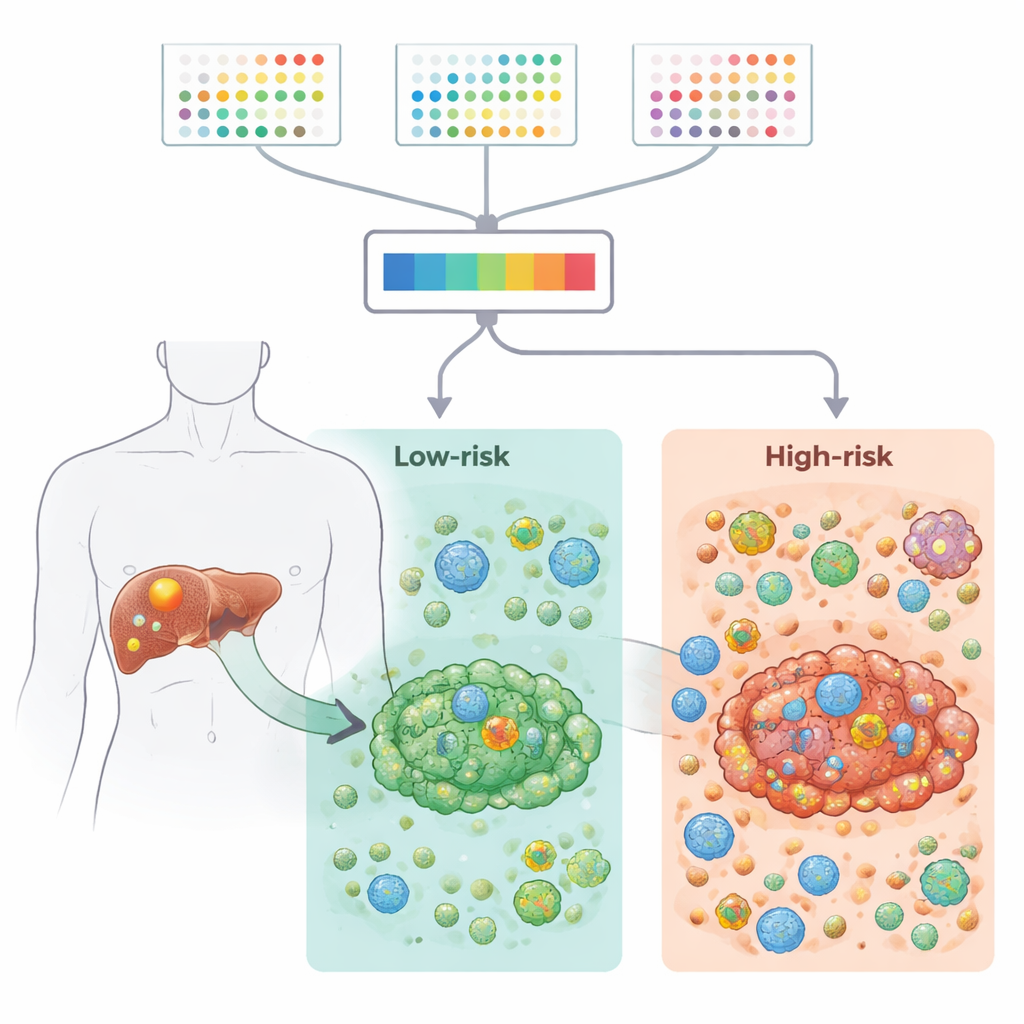
Budowanie wskaźnika ryzyka z dziewięciu kluczowych genów
Aby przekształcić te złożone informacje w użyteczne klinicznie narzędzie, zespół przetestował 117 kombinacji metod uczenia maszynowego i modeli przeżycia. Najlepiej sprawdziło się podejście łączące krokową regresję Coxa z losowymi lasami przeżycia (random survival forests), które sprowadziło informacje do dziewięciu genów. Każdy pacjent otrzymał wynik ryzyka oparty na tym, jak silnie te geny były włączone lub wyłączone w jego guzie. W kilku niezależnych grupach pacjentów podpis dziewięciu genów wiarygodnie dzielił pacjentów na grupy o wysokim i niskim ryzyku z wyraźnie różnymi czasami przeżycia. Guzy o wysokim ryzyku były wzbogacone w szlaki związane ze stresem i zapaleniem, podczas gdy guzy o niskim ryzyku wykazywały silniejszą aktywność szlaków metabolicznych i detoksykacyjnych, co sugeruje zasadnicze różnice biologiczne między tymi dwiema grupami.
Sąsiedztwa immunologiczne wewnątrz guza
Badanie następnie przyjrzało się mikrośrodowisku guza — mieszaninie komórek odpornościowych, komórek podporowych i tkanki łącznej, które otaczają i infiltrują nowotwór. Używając kilku narzędzi obliczeniowych, autorzy wykazali, że guzy o wysokim ryzyku miały wyższe wyniki odpornościowe i zrębuszu (stromalne), silniejsze sygnały zapalne oraz więcej cech immunosupresyjnych, w tym zwiększoną liczbę komórek regulatorowych T (Treg), które mogą tłumić odpowiedź przeciwnowotworową. Sekwencjonowanie RNA pojedynczych komórek potwierdziło, że te Tregi i fibroblasty były bardziej liczne w guzach wysokiego ryzyka i uczestniczyły w gęstych sieciach komunikacji międzykomórkowej. W przeciwieństwie do tego, guzy niskiego ryzyka wykazywały silniejsze sygnalizowanie związane z kolagenem i bardziej zrównoważone, mniej tłumiące środowisko. Razem te obserwacje sugerują, że wzorzec dziewięciu genów jest ściśle powiązany z tym, jak „przyjazne” lub „wrogie” jest lokalne środowisko immunologiczne względem guza. 
Wytyczne dotyczące immunoterapii i doboru leków
Z uwagi na rosnącą rolę immunoterapii w onkologii, badacze stworzyli odrębny „PCD score” oparty na tych samych dziewięciu genach, by przewidzieć odpowiedź na blokadę punktów kontrolnych układu odpornościowego. W trzech niezależnych kohortach pacjentów leczonych takimi lekami (pochodzących z innych typów nowotworów z dostępnymi danymi) wyższe wartości PCD score konsekwentnie wiązały się z lepszą odpowiedzią, co sugeruje, że wynik odzwierciedla cechy środowiska guza sprzyjające skuteczności immunoterapii. Zespół wykorzystał także bazy danych wrażliwości na leki i symulacje dokowania komputerowego, aby przewidzieć, które leki mogą być skuteczniejsze w różnych grupach ryzyka. Pacjenci o wysokim ryzyku wydawali się bardziej wrażliwi na pewne leki celowane, w tym inhibitory szlaków TGF-beta i mTOR, co wskazuje potencjalne strategie kombinacyjne mające przełamać immunosupresję.
Od złożonej biologii do praktycznych narzędzi
Aby ułatwić przeniesienie tych wyników do praktyki klinicznej, autorzy zbudowali nomogram — wizualny kalkulator ryzyka — łączący genowy wynik ryzyka z rutynowymi informacjami klinicznymi, takimi jak stadium choroby i inwazja naczyń. To narzędzie dokładnie przewidywało przeżycie w ciągu jednego, trzech i czterech lat w głównej kohorcie pacjentów. Chociaż wyniki wymagają jeszcze prospektywnego przetestowania w większych, zdefiniowanych pod względem leczenia grupach pacjentów z wewnątrzwątrobowym rakiem dróg żółciowych, badanie dostarcza schematu pokazującego, jak wzorce genów powiązanych ze śmiercią komórkową można wykorzystać do klasyfikacji guzów, zrozumienia ich ekosystemów immunologicznych i ukierunkowania terapii. Dla pacjentów długoterminowa obietnica to bardziej precyzyjne prognozy i lepiej dopasowane leczenie oparte na unikalnym genetycznym i immunologicznym odcisku ich guza.
Cytowanie: Zhang, T., Dou, D., Liu, Q. et al. Single-cell and bulk transcriptomic analyses uncover immune subtypes associated with programmed cell death features in intrahepatic cholangiocarcinoma. Sci Rep 16, 13678 (2026). https://doi.org/10.1038/s41598-026-44332-8
Słowa kluczowe: wewnątrzwątrobowy rak dróg żółciowych, programowana śmierć komórki, mikrosrodowisko immunologiczne guza, sekwencjonowanie RNA pojedynczych komórek, odpowiedź na immunoterapię