Clear Sky Science · fr
Analyses transcriptomiques en cellules uniques et en masse révèlent des sous-types immunitaires associés aux caractéristiques de la mort cellulaire programmée dans le cholangiocarcinome intra-hépatique
Pourquoi cette étude sur le cancer du foie est importante
Le cholangiocarcinome intra-hépatique est un cancer en forte progression qui prend naissance dans les petits canaux biliaires du foie et est souvent diagnostiqué trop tard pour envisager une chirurgie. Les cliniciens observent que certains patients vivent beaucoup plus longtemps ou répondent mieux aux nouvelles immunothérapies que d’autres, mais il a été difficile de prédire qui bénéficiera de ces traitements. Cette étude utilise des profils génétiques avancés et l’analyse unicellulaire pour montrer comment différentes formes de mort cellulaire « programmée » et le système immunitaire interagissent dans ces tumeurs, et elle élabore un score pratique susceptible d’aider à personnaliser les traitements et orienter les décisions cliniques.
Examiner les tumeurs hépatiques cellule par cellule
Les chercheurs ont rassemblé de grands jeux de données d’expression génique issus de centaines d’échantillons tumoraux, comprenant à la fois des tissus en masse et des cellules uniques, provenant de ressources publiques et d’une large cohorte clinique. Ils se sont concentrés sur 2 701 gènes associés à 21 types de mort cellulaire programmée — les mécanismes intrinsèques par lesquels les cellules peuvent s’autodétruire lorsqu’elles sont endommagées ou anormales. En comparant le tissu tumoral au foie non cancéreux adjacent, ils ont réduit cette liste à 87 gènes à la fois dérégulés dans le cancer et potentiellement importants pour la survie des patients. Ces gènes participaient à des voies connues du cancer et à des formes de mort cellulaire telles que l’apoptose et la nécroptose, et présentaient aussi des profils caractéristiques de mutations et d’altérations chromosomiques dans les tumeurs des canaux biliaires hépatiques. 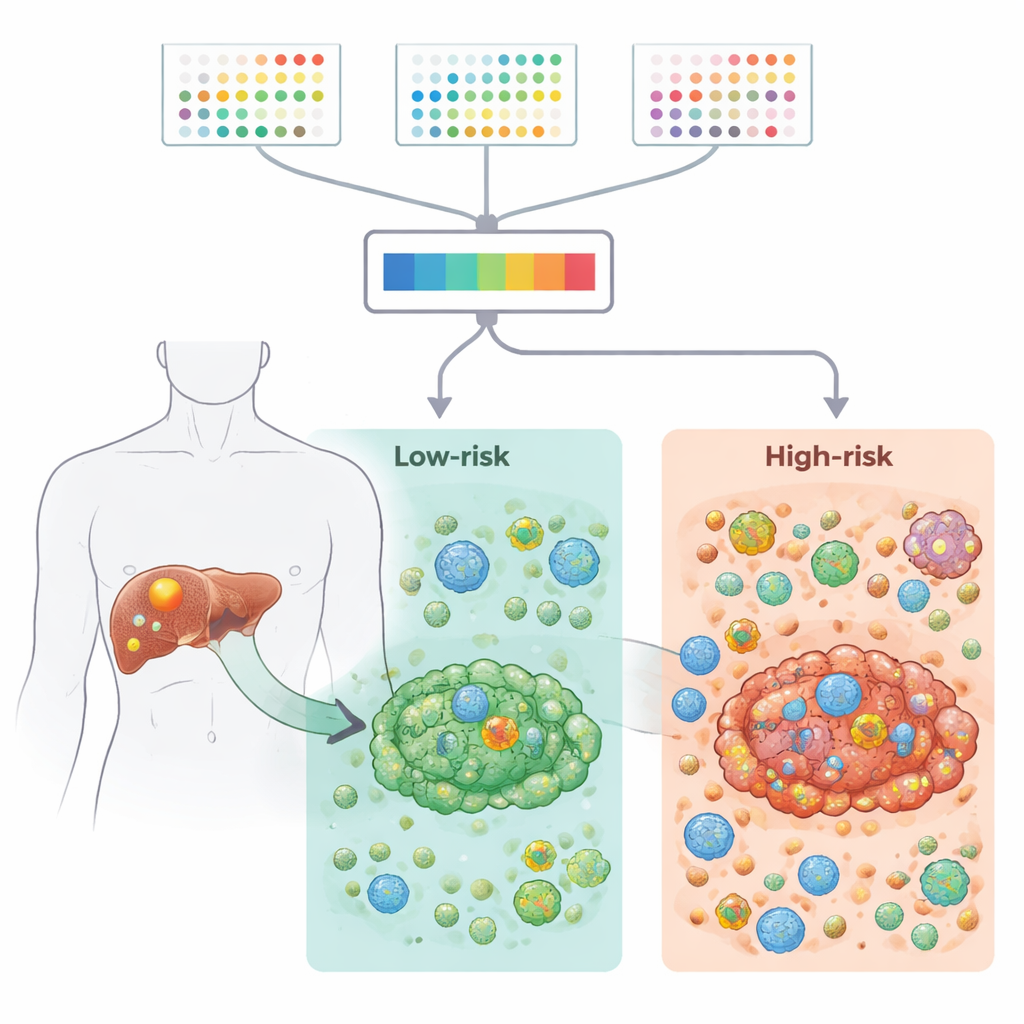
Construire un score de risque à partir de neuf gènes clés
Pour transformer cette information complexe en un outil cliniquement utile, l’équipe a testé 117 combinaisons de méthodes d’apprentissage automatique et de modèles de survie. L’approche la plus performante, qui combinait une régression de Cox par étapes et des forêts aléatoires de survie, a réduit l’information à neuf gènes. Chaque patient recevait un score de risque basé sur l’intensité d’expression de ces gènes dans sa tumeur. Dans plusieurs cohorts indépendantes, ce signature à neuf gènes a séparé de manière fiable les patients en groupes à haut et faible risque présentant des survies nettement différentes. Les tumeurs à haut risque étaient enrichies en voies liées au stress et à l’inflammation, tandis que les tumeurs à faible risque présentaient des voies métaboliques et de détoxification plus actives, suggérant des différences biologiques fondamentales entre les deux groupes.
Quartiers immunitaires à l’intérieur de la tumeur
L’étude a ensuite zoomé sur le microenvironnement tumoral — le mélange de cellules immunitaires, cellules de soutien et tissu conjonctif qui entoure et infiltre la tumeur. À l’aide de plusieurs outils informatiques, les auteurs ont montré que les tumeurs à haut risque présentaient des scores immunitaires et stromaux plus élevés, des signaux inflammatoires plus forts et davantage de caractéristiques immunosuppressives, notamment une augmentation des cellules T régulatrices capables d’atténuer les réponses anti-tumorales. Le séquençage ARN unicellulaire a confirmé que ces cellules T régulatrices et les fibroblastes étaient plus abondants dans les tumeurs à haut risque et participaient à des réseaux d’interactions cellule–cellule denses. En revanche, les tumeurs à faible risque présentaient une signalisation liée au collagène plus marquée et un environnement plus équilibré, moins suppressif. Ensemble, ces résultats suggèrent que le profil à neuf gènes est étroitement lié au degré de « convivialité » ou d’« hostilité » du voisinage immunitaire local vis‑à‑vis de la tumeur. 
Orienter le choix des immunothérapies et des médicaments
Conscients que l’immunothérapie devient centrale dans la prise en charge du cancer, les chercheurs ont calculé un « score PCD » distinct à partir des mêmes neuf gènes pour prédire la réponse aux inhibiteurs de points de contrôle immunitaire. Dans trois cohortes indépendantes de patients traités par ces médicaments (issues d’autres types de cancer avec des données disponibles), des scores PCD plus élevés étaient systématiquement associés à de meilleures réponses, ce qui suggère que le score capture des caractéristiques de l’environnement tumoral favorables à l’efficacité de l’immunothérapie. L’équipe a également utilisé des bases de données de sensibilité aux médicaments et des simulations de docking informatique pour prédire quels traitements pourraient être plus efficaces selon les groupes de risque. Les patients à haut risque semblaient plus sensibles à certains agents ciblés, notamment des inhibiteurs des voies TGF‑beta et mTOR, offrant des stratégies de combinaison potentielles pour surmonter l’immunosuppression.
De la biologie complexe aux outils pratiques
Pour faciliter la traduction clinique de ces résultats, les auteurs ont construit un nomogramme — un calculateur visuel de risque — qui combine le score de risque basé sur les gènes avec des informations cliniques courantes comme le stade et l’envahissement vasculaire. Cet outil a prédit avec précision la survie à un, trois et quatre ans dans leur cohorte principale. Bien que ces travaux nécessitent encore des validations prospectives dans des cohortes plus larges et définies par le traitement chez des patients atteints de cholangiocarcinome intra‑hépatique, ils fournissent une feuille de route sur la manière dont les profils de gènes liés à la mort cellulaire peuvent servir à classifier les tumeurs, comprendre leurs écosystèmes immunitaires et guider la thérapie. Pour les patients, la promesse à long terme est d’obtenir des pronostics plus précis et des traitements mieux adaptés, fondés sur l’empreinte génétique et immunitaire unique de leur tumeur.
Citation: Zhang, T., Dou, D., Liu, Q. et al. Single-cell and bulk transcriptomic analyses uncover immune subtypes associated with programmed cell death features in intrahepatic cholangiocarcinoma. Sci Rep 16, 13678 (2026). https://doi.org/10.1038/s41598-026-44332-8
Mots-clés: cholangiocarcinome intra-hépatique, mort cellulaire programmée, microenvironnement immunitaire tumoral, séquençage ARN unicellulaire, réponse à l’immunothérapie