Clear Sky Science · ru
Анализы транскриптомов на уровне одиночных клеток и тканей выявляют иммунные подтипы, связанные с признаками программируемой клеточной гибели при внутрипечёночной холангиокарциноме
Почему это исследование рака печени важно
Внутрипечёночная холангиокарцинома — быстро прогрессирующий рак, возникающий из мелких желчных протоков внутри печени, который часто выявляют слишком поздно для хирургического вмешательства. Врачи заметили, что некоторые пациенты живут значительно дольше или лучше отвечают на новые иммунотерапевтические методы лечения, однако предсказать, кто получит пользу, было трудно. В этом исследовании использованы современные подходы картирования генетической активности и анализ одиночных клеток, чтобы показать, как разные варианты «программируемой» клеточной гибели взаимодействуют с иммунной системой в этих опухолях, и создан практичный скор, который может помочь персонализировать лечение и направлять клинические решения.
Исследование опухолей печени поклеточно
Исследователи собрали крупные наборы данных активности генов из сотен образцов опухолей, включая как гомогенные ткани, так и одиночные клетки, из общедоступных ресурсов и крупной клинической когорты. Они сосредоточились на 2701 гене, связанных с 21 типом программируемой клеточной гибели — встроенными путями, которыми клетки могут самоуничтожаться при повреждении или патологии. Сопоставляя опухолевую ткань с прилежащей непоражённой печенью, они сузили список до 87 генов, которые были нарушены при раке и могли иметь значение для выживания пациентов. Эти гены участвовали в известных онкопутях и формах клеточной гибели, таких как апоптоз и некроптоз, а также демонстрировали характерные паттерны мутаций и хромосомных изменений при опухолях желчных протоков печени. 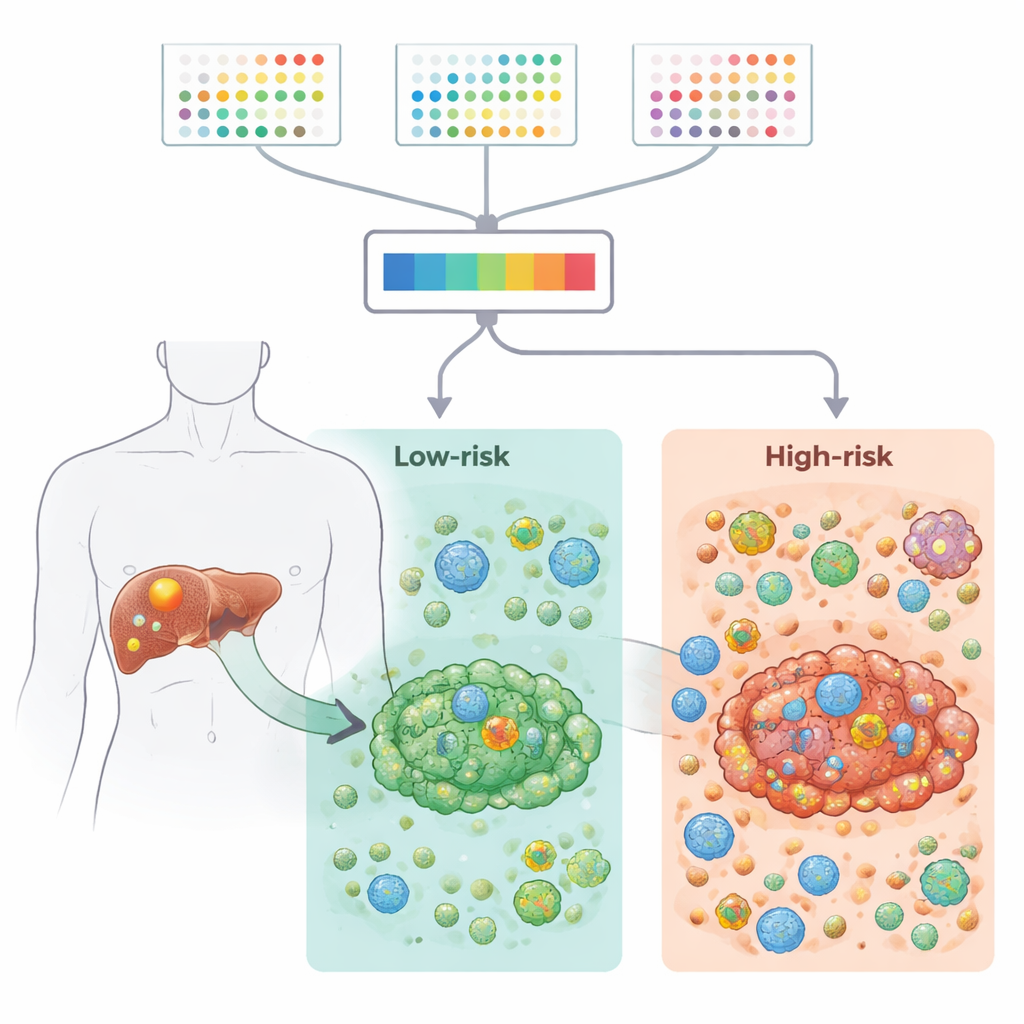
Построение риск‑индекса на основе девяти ключевых генов
Чтобы превратить эту сложную информацию в клинически применимый инструмент, команда протестировала 117 комбинаций методов машинного обучения и моделей выживаемости. Наилучшим оказалась комбинация пошаговой регрессии Кокса и случайных лесов выживаемости, которая сократила набор до девяти генов. Каждому пациенту присваивался риск‑балл на основе того, насколько сильно эти гены были включены или выключены в опухоли. В нескольких независимых когортах пациентов этот девятегенный сигнатурный профиль надёжно разделял людей на группы высокого и низкого риска с явно различающимся временем выживания. Опухоли высокого риска были обогащены путями, связанными со стрессом и воспалением, в то время как опухоли низкого риска демонстрировали более активные метаболические и детоксикационные механизмы, что указывает на фундаментальные биологические различия между группами.
Иммунные «окрестности» внутри опухоли
Далее исследование углубилось в микросреду опухоли — смешение иммунных клеток, клеток‑стромы и соединительной ткани, которое окружает и инфильтрирует опухоль. С помощью нескольких вычислительных инструментов авторы показали, что опухоли высокого риска имеют более высокие иммунные и стромальные показатели, усиленные воспалительные сигналы и больше иммуноподавляющих признаков, включая увеличение регуляторных Т‑клеток, которые могут ослаблять противоопухолевый ответ. Секвенирование РНК одиночных клеток подтвердило, что эти регуляторные Т‑клетки и фибробласты более многочисленны в опухолях высокого риска и участвуют в плотных сетях клеточно‑клеточной коммуникации. Напротив, в опухолях низкого риска отмечались более выраженные коллаген‑связанные сигнальные пути и более сбалансированная, менее подавляющая среда. В совокупности эти результаты указывают, что девятигенный паттерн тесно связан с тем, насколько «дружелюбной» или «враждебной» является локальная иммунная среда по отношению к опухоли. 
Ориентирование в выборе иммунотерапии и лекарств
Понимая, что иммунотерапия становится центральным элементом лечения рака, исследователи создали отдельный «PCD‑скор» на основе тех же девяти генов для предсказания ответа на блокаду иммунных контрольных точек. В трёх независимых когортках пациентов, лечившихся такими препаратами (в других типах рака, где были доступны данные), более высокие PCD‑значения последовательно ассоциировались с лучшим ответом, что подразумевает: скор отражает свойства опухолевой среды, повышающие вероятность эффективности иммунотерапии. Команда также использовала базы данных чувствительности к препаратам и компьютерное докинг‑моделирование, чтобы спрогнозировать, какие лекарства могут работать лучше в разных группах риска. Пациенты высокого риска казались более чувствительными к определённым таргетным агентам, включая препараты, влияющие на TGF‑бета и mTOR‑сигналинг, что может дать основу для комбинированных стратегий преодоления иммунного подавления.
От сложной биологии к практическим инструментам
Чтобы помочь перенести эти находки в клинику, авторы создали номограмму — визуальный калькулятор риска, который объединяет генетический риск‑скор с обычной клинической информацией, такой как стадия заболевания и сосудистая инвазия. Этот инструмент точно прогнозировал выживаемость на один, три и четыре года в основной когорте пациентов. Хотя работа требует дальнейшей проспективной проверки в больших группах пациентов с чётко определёнными режимами лечения при внутрипечёночной холангиокарциноме, она предлагает план действий: как паттерны генов, связанных с клеточной гибелью, можно использовать для классификации опухолей, понимания их иммунных экосистем и выбора терапии. Для пациентов долгосрочная перспектива — более точные прогнозы и лучше подобранные лечение на основе уникального генетического и иммунного «отпечатка» их опухоли.
Цитирование: Zhang, T., Dou, D., Liu, Q. et al. Single-cell and bulk transcriptomic analyses uncover immune subtypes associated with programmed cell death features in intrahepatic cholangiocarcinoma. Sci Rep 16, 13678 (2026). https://doi.org/10.1038/s41598-026-44332-8
Ключевые слова: внутрипечёночная холангиокарцинома, программируемая клеточная гибель, опухолевая иммунная микросреда, секвенирование РНК одиночных клеток, ответ на иммунотерапию