Clear Sky Science · zh
介导Mycobacterium smegmatis胆固醇转运的调控机制:LtmA
本研究为何重要
结核病仍然是全球最致命的传染病之一,部分原因在于其致病菌——结核分枝杆菌——极擅长在我们免疫细胞内存活。它的一项关键伎俩是吞噬宿主的胆固醇并用来强化自身防御。本研究借助一种安全的近缘模型菌Mycobacterium smegmatis,揭示了单一调控蛋白如何开关式地控制胆固醇摄取——为在体内“饿死”这些微生物提供了新的线索。
能吃掉我们胆固醇的细菌
当结核菌被称为巨噬细胞的免疫细胞吞噬后,并不像许多其他微生物那样被摧毁。相反,它们定居在细胞内的一个区室中,并重塑周围膜以吸引胆固醇。这种脂质分子不仅是细菌细胞壁的构件,还在长期感染期间、其他营养物质匮乏时,成为重要的碳和能量来源。细菌包膜中的专门运输系统,包括称为Mce4的复合体,像分子门一样将胆固醇从宿主环境拉入微生物内部。
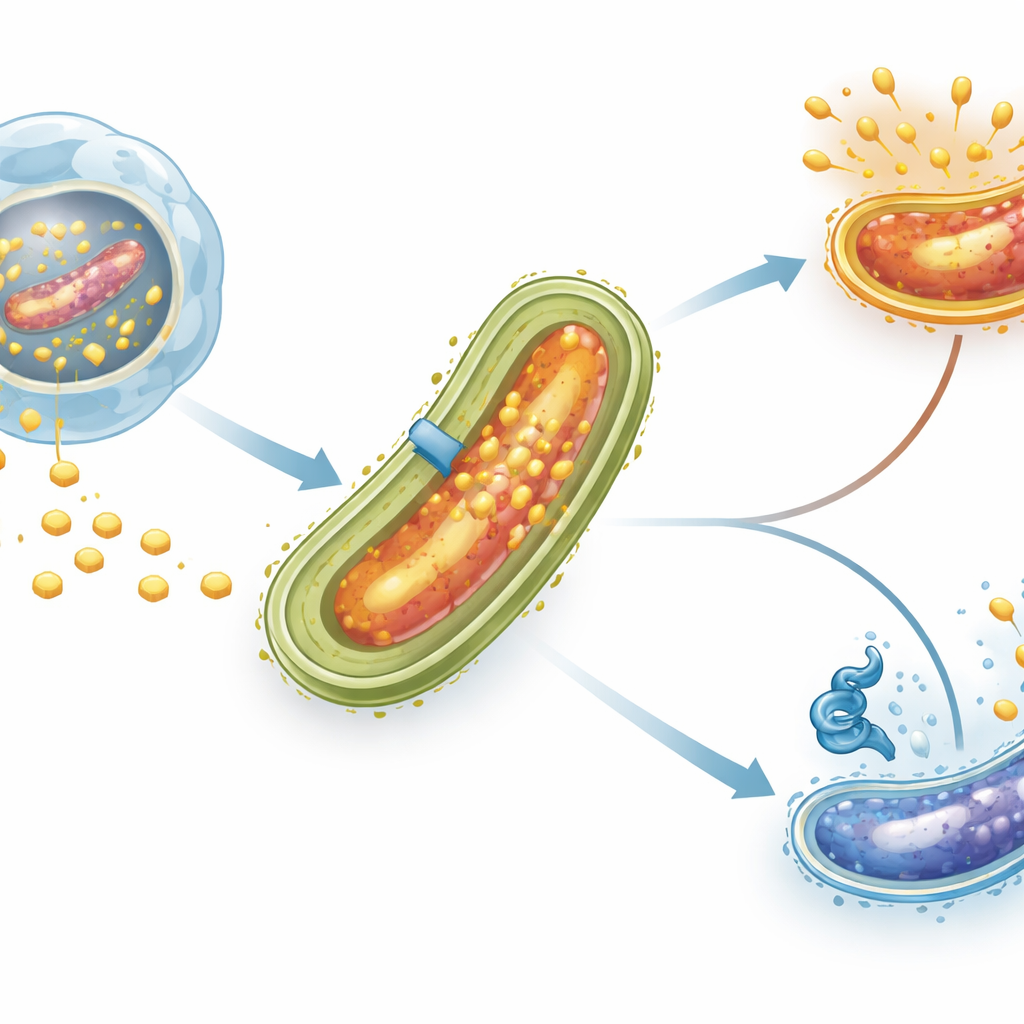
控制胆固醇进入的“交通灯”
研究者聚焦于一种名为LtmA的调控蛋白,此前已知它影响许多与脂质相关的基因。像LtmA这样的蛋白在细菌DNA上充当“交通灯”,决定哪些基因应被激活、哪些应被抑制。通过计算分析,团队在mce4基因簇上游识别出一段可能被LtmA识别的短DNA序列。随后他们在体外纯化了LtmA,并进行了电泳迁移率变动实验,这种技术本质上检测蛋白是否会物理结合到某段DNA片段上。结果显示,LtmA对正常的mce4调控区结合牢固且具有特异性,但对关键碱基被替换的版本则不结合,从而证实该调控因子直接识别mce4启动子。
调高或调低胆固醇水龙头
为了解该结合在活细菌中的意义,团队构建了LtmA表达被下调(敲减)或过表达的菌株。他们测量了mce4基因的活性,发现互为镜像的模式:当LtmA水平偏低时,mce4转运基因的转录量上升数倍;而当LtmA丰富时,这些基因被显著抑制。功能性检测支持这一结论。在胆固醇摄取实验中,LtmA减少的细菌摄入胆固醇更快且更多,而过表达LtmA的细菌摄入则较慢且较少。换言之,LtmA充当了对胆固醇进口机制的刹车。
只有在有胆固醇时才能生长
当科学家在明确的碳源上培养不同菌株时,这一调控刹车的后果变得清晰。以葡萄糖为食时,各菌株——无论LtmA水平偏低、正常或过多——生长表现相当,代谢活性相近。但当胆固醇是唯一碳源时,情况则相反。过量LtmA的菌株(因此mce4转运活性较低)生长不良且代谢活性低。LtmA减少的菌株,其Mce4“门”更开放,生长更强劲并更积极代谢胆固醇。这表明LtmA通过限制宿主来源营养物的进入量,特异性地限制了依赖胆固醇条件下的生长。
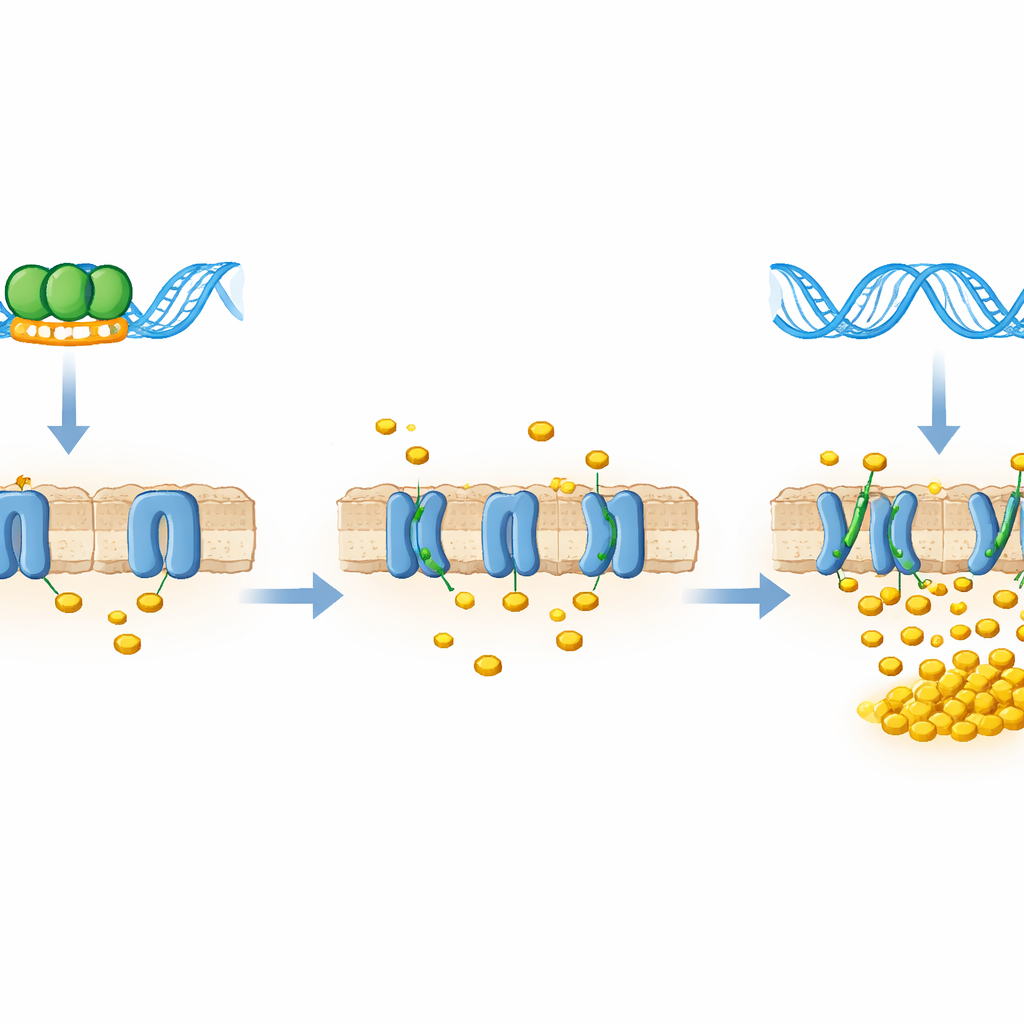
对抗结核病的潜在意义
综合来看,研究结果显示LtmA是mce4胆固醇转运子的直接抑制因子:当LtmA结合于mce4调控区时,胆固醇的分子门保持部分关闭;当LtmA被减少或缺失时,这些门打开,细菌就能大量摄取胆固醇并“进食”。尽管该研究在无致病性的模型物种中完成,LtmA与结核分枝杆菌中的一类蛋白高度相关,提示类似的开关可能影响病原体在感染过程中如何利用宿主胆固醇。如果属实,干扰该调控节点或其所控的转运子的小分子药物,未来或可帮助在巨噬细胞内切断结核菌的营养来源,为全球控制这一长期困扰的疾病提供新的策略。
引用: Feng, YW., Yin, BC., Li, HB. et al. Regulatory mechanism of cholesterol transport via LtmA in Mycobacterium smegmatis. Sci Rep 16, 14235 (2026). https://doi.org/10.1038/s41598-026-43871-4
关键词: 结核病, 胆固醇摄取, 细菌调控因子, 分枝杆菌, 宿主–病原体相互作用