Clear Sky Science · pl
Mechanizm regulacji transportu cholesterolu przez LtmA w Mycobacterium smegmatis
Dlaczego to badanie ma znaczenie
Gruźlica pozostaje jedną z najgroźniejszych chorób zakaźnych na świecie, częściowo dlatego, że jej wywołujący ją gatunek, Mycobacterium tuberculosis, doskonale radzi sobie z przetrwaniem wewnątrz naszych komórek odpornościowych. Jednym z jego kluczowych trików jest wykorzystywanie cholesterolu gospodarza jako pożywienia i wzmacnianie za jego pomocą własnych mechanizmów obronnych. Wykorzystując bezpieczny model bliski bakteriom gruźlicy — Mycobacterium smegmatis — to badanie ujawnia, jak pojedynczy białkowy regulator potrafi włączać lub wyłączać pobieranie cholesterolu, dając wskazówki do nowych sposobów „głodzenia” tych mikroorganizmów w organizmie.
Bakteria, która pożywia się naszym cholesterolem
Kiedy bakterie wywołujące gruźlicę zostają pochłonięte przez komórki odpornościowe zwane makrofagami, nie są niszczone tak jak wiele innych drobnoustrojów. Zamiast tego osiedlają się w specjalnym przedziale wewnątrz komórki i przebudowują otaczającą membranę tak, aby przyciągała cholesterol. Ta tłuszczowa cząsteczka nie jest tylko elementem budulcowym ściany komórkowej bakterii; staje się też istotnym źródłem węgla i energii, zwłaszcza podczas przewlekłych zakażeń, gdy inne składniki odżywcze są ograniczone. Specjalizowane systemy transporterów w otoczce bakteryjnej, w tym kompleks zwany Mce4, działają jak molekularne drzwi, które wyciągają cholesterol ze środowiska gospodarza do wnętrza mikroba.
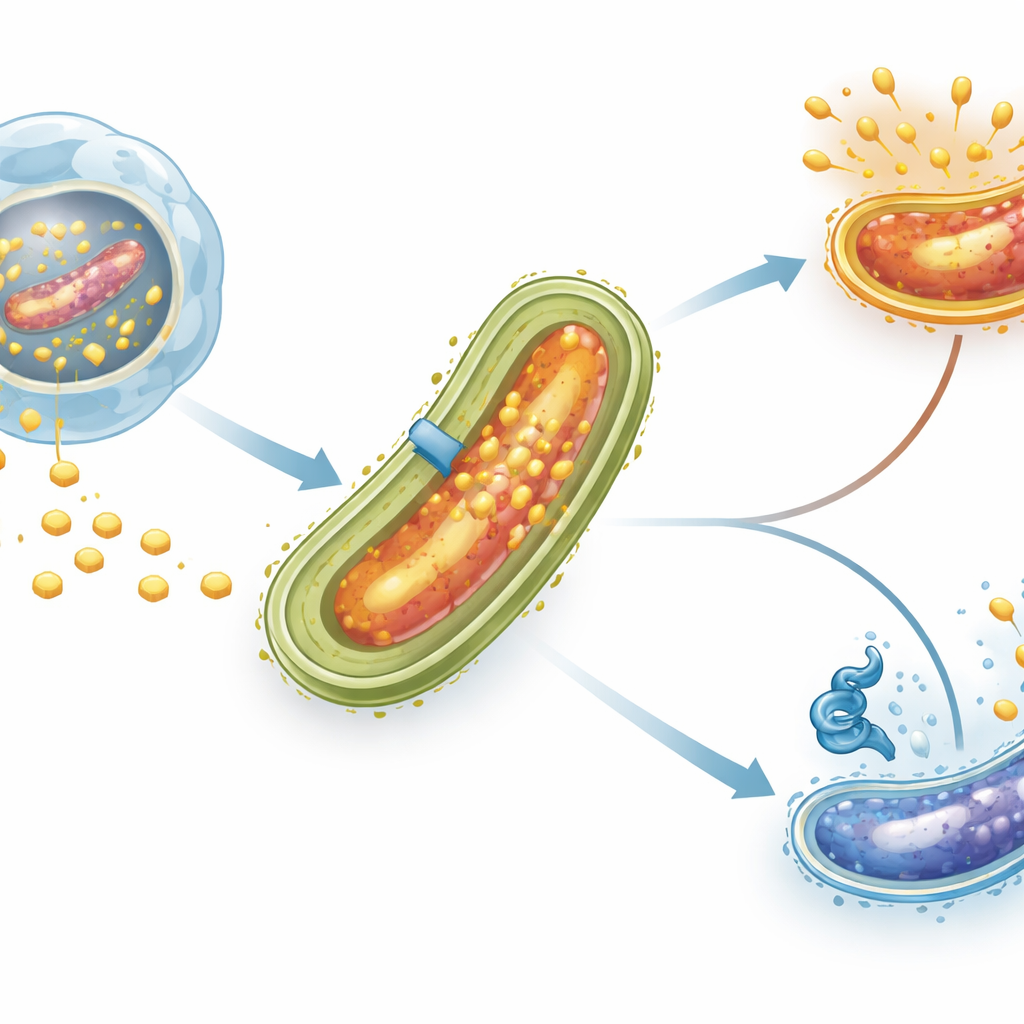
Sygnalizacja świetlna dla wejścia cholesterolu
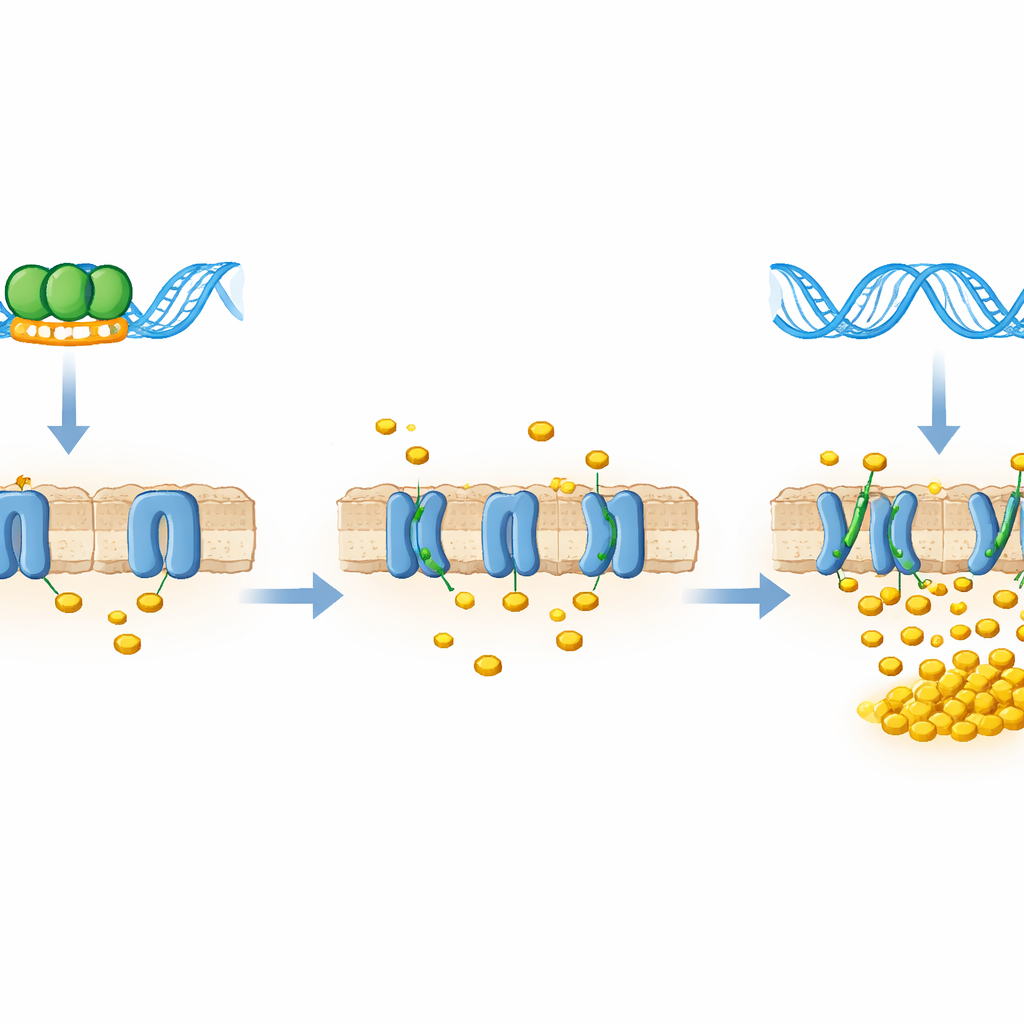
Naukowcy skupili się na białku regulatorowym nazwanym LtmA, wcześniej znanym z wpływu na wiele genów związanych z lipidami. Białka takie jak LtmA pełnią rolę „świateł drogowych” na DNA bakterii, decydując, które geny mają być aktywne, a które przyhamowane. Za pomocą analiz komputerowych zespół zidentyfikował krótką sekwencję DNA przed klastrem genów mce4, wyglądającą na prawdopodobne miejsce dokowania dla LtmA. Następnie oczyścili LtmA w laboratorium i przeprowadzili test zwany elektroforetycznym testem przesunięcia ruchliwości (EMSA), który w istocie sprawdza, czy białko fizycznie wiąże się z fragmentem DNA. LtmA wiązał się silnie i specyficznie z prawidłowym regionem kontrolnym mce4, ale nie z wersją, w której zmieniono kluczowe nukleotydy, co potwierdza, że regulator bezpośrednio rozpoznaje promotor mce4.
Regulacja dopływu cholesterolu — przykręcanie i odkręcanie
Aby ustalić, co to wiązanie oznacza dla żywej bakterii, zespół skonstruował szczepy produkujące mniej LtmA (obniżenie ekspresji) lub nadmiar LtmA (nadekspresja). Zmierzyli aktywność genów mce4 i zaobserwowali lustrzany wzór: gdy poziomy LtmA były niskie, transkrypty genów transportera mce4 wzrastały wielokrotnie; kiedy LtmA było obfite, te same geny były silnie represjonowane. Testy funkcjonalne potwierdziły ten obraz. W teście wychwytu cholesterolu bakterie z obniżonym LtmA pobierały cholesterol szybciej i w większych ilościach niż komórki normalne, podczas gdy szczepy z nadmiarem LtmA były pod tym względem opóźnione. LtmA pełni zatem funkcję hamulca dla mechanizmu importu cholesterolu.
Wzrost tylko, gdy w menu jest cholesterol
Konsekwencje tego regulatoryjnego hamulca stały się jasne, gdy naukowcy hodowali różne szczepy na zdefiniowanych źródłach węgla. Gdy źródłem była glukoza, wszystkie szczepy — czy to z niedoborem LtmA, normalne, czy przeciążone tym białkiem — rosły równie dobrze i wykazywały podobną aktywność metaboliczną. Jednak gdy jedynym źródłem węgla był cholesterol, sytuacja się odwróciła. Szczepy z nadmiarem LtmA, a zatem z mniej aktywnymi transporterami mce4, rosły słabo i miały niską aktywność metaboliczną. Szczepy z obniżonym LtmA, których „drzwi” Mce4 były bardziej otwarte, rosły bardziej energicznie i metabolizowały cholesterol wydajniej. To dowodzi, że LtmA specyficznie ogranicza wzrost w warunkach zależnych od cholesterolu, kontrolując, ile tego składnika gospodarza może wejść do komórki.
Znaczenie dla walki z gruźlicą
Podsumowując, wyniki ukazują LtmA jako bezpośredniego represora transportera cholesterolu mce4: gdy LtmA jest związane z regionem kontrolnym mce4, molekularne drzwi dla cholesterolu pozostają częściowo zamknięte; gdy LtmA jest zmniejszone lub nieobecne, te drzwi otwierają się i bakteria może się posilić. Chociaż praca została przeprowadzona na niepatogennym gatunku modelowym, LtmA jest blisko spokrewnione z białkiem występującym w Mycobacterium tuberculosis, co sugeruje, że podobny mechanizm może wpływać na to, jak patogen wykorzystuje cholesterol gospodarza podczas zakażenia. Jeśli tak jest, leki zakłócające ten węzeł regulacyjny — lub sam transporter, który on kontroluje — mogłyby w przyszłości pomóc w „zagłodzeniu” bakterii gruźlicy wewnątrz makrofagów, dodając nowy wymiar do globalnych wysiłków na rzecz kontroli tej przewlekłej choroby.
Cytowanie: Feng, YW., Yin, BC., Li, HB. et al. Regulatory mechanism of cholesterol transport via LtmA in Mycobacterium smegmatis. Sci Rep 16, 14235 (2026). https://doi.org/10.1038/s41598-026-43871-4
Słowa kluczowe: gruźlica, wchłanianie cholesterolu, regulatory bakteryjne, mikobakterie, interakcja gospodarza z patogenem