Clear Sky Science · nl
Reguleringsmechanisme van cholesteroltransport via LtmA in Mycobacterium smegmatis
Waarom deze studie ertoe doet
Tuberculose blijft een van de dodelijkste infectieziekten ter wereld, mede omdat de veroorzakende bacterie, Mycobacterium tuberculosis, zo goed kan overleven in onze immuuncellen. Een van haar belangrijkste trucs is het benutten van ons cholesterol om haar eigen verdedigingen te versterken. Deze studie, uitgevoerd met een veilige modelverwant van de tuberculeuse bacterie genaamd Mycobacterium smegmatis, onthult hoe een enkel regulerend eiwit de opname van cholesterol aan- of uitzet—wat aanwijzingen geeft voor nieuwe manieren om deze microben in het lichaam uit te hongeren.
De bacterie die ons cholesterol opeet
Wanneer tuberculosebacteriën worden opgenomen door immuuncellen genaamd macrofagen, worden ze niet vernietigd zoals veel andere microben. In plaats daarvan vestigen ze zich in een compartiment binnen de cel en herschikken ze het omringende membraan om cholesterol aan te trekken. Dit vette molecuul is niet alleen een bouwsteen voor de bacteriële celwand; het dient ook als een belangrijke bron van koolstof en energie, vooral tijdens langdurige infecties wanneer andere voedingsstoffen schaars zijn. Gespecialiseerde transportsystemen in de bacteriële envelop, waaronder het zogenaamde Mce4-complex, functioneren als moleculaire deuren die cholesterol uit de gastheeromgeving in de microbe trekken.
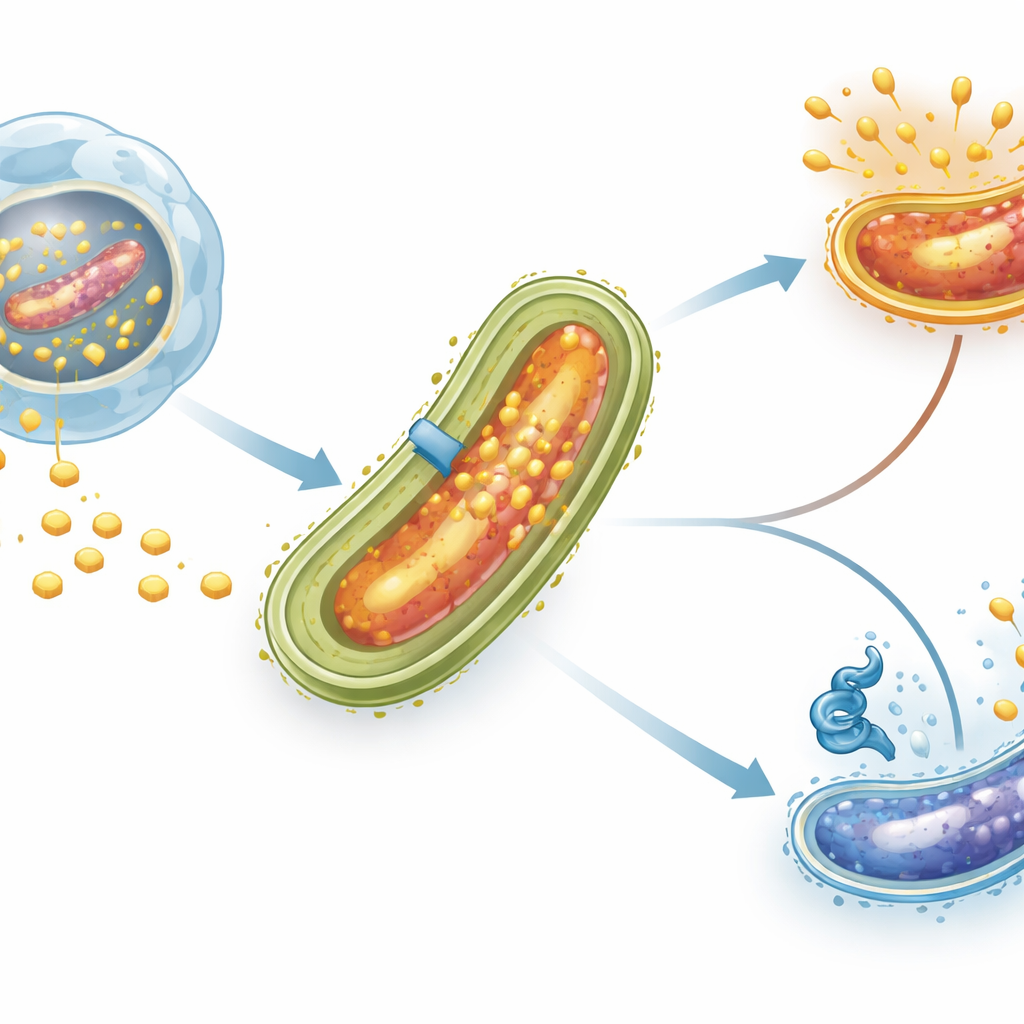
Een stoplicht voor cholesteroltoegang
De onderzoekers richtten zich op een regulerend eiwit genaamd LtmA, dat eerder bekendstond om zijn invloed op veel vetgerelateerde genen. Eiwitten zoals LtmA werken als “stoplichten” op het bacteriële DNA en bepalen welke genen actief moeten zijn en welke gepauzeerd. Met computervaardigheden identificeerde het team een korte DNA-sequentie voor de mce4-gencluster die er als een waarschijnlijke aanhechtingsplaats voor LtmA uitzag. Vervolgens zuiverden ze LtmA in het laboratorium en voerden een techniek uit die een elektroforetische mobiliteitsverschuivingsassay heet, die in wezen test of een eiwit fysiek aan een DNA-fragment bindt. LtmA bond sterk en specifiek aan de normale mce4-controle-regio, maar niet aan een versie waarvan cruciale basen waren veranderd, wat bevestigt dat deze regulator direct de mce4-promoter herkent.
Het cholesterolkraantje harder of zachter zetten
Om te begrijpen wat deze binding voor de levende bacterie betekent, maakten de onderzoekers stammen die ofwel minder LtmA produceerden (knockdown) of juist extra LtmA (overexpressie). Ze maten de activiteit van de mce4-genen en vonden een spiegelbeeldig patroon: wanneer LtmA-niveaus laag waren, stegen de transcriptielevels van de mce4-transporter-genen meerdere malen; wanneer LtmA overvloedig aanwezig was, werden diezelfde genen sterk geremd. Functionele tests bevestigden dit beeld. In een cholesterolopname-assay namen bacteriën met verminderd LtmA cholesterol sneller en in grotere hoeveelheden op dan normale cellen, terwijl die met teveel LtmA achterbleven. LtmA fungeert met andere woorden als een rem op het cholesterolimportmechanisme.
Groei alleen wanneer cholesterol op het menu staat
De gevolgen van deze regulatorische rem werden duidelijk toen de wetenschappers de verschillende bacteriestammen op gedefinieerde koolstofbronnen lieten groeien. Wanneer glucose als voedsel diende, groeiden alle stammen—ongeacht of ze weinig LtmA hadden, normaal waren of er te veel van produceerden—even goed en toonden ze vergelijkbare metabolische activiteit. Maar wanneer cholesterol de enige koolstofbron was, keerde het beeld zich om. Stammen met extra LtmA, en dus minder actieve mce4-transporters, groeiden slecht en vertoonden lage metabolische activiteit. Stammen met verminderde LtmA, waarvan de Mce4-deuren meer openstonden, groeiden robuuster en metaboliseerden cholesterol krachtiger. Dit laat zien dat LtmA specifiek de groei beperkt onder cholesterolafhankelijke omstandigheden door te beperken hoeveel van deze gastheer-afgeleide voedingsstof de cel kan binnenkomen.
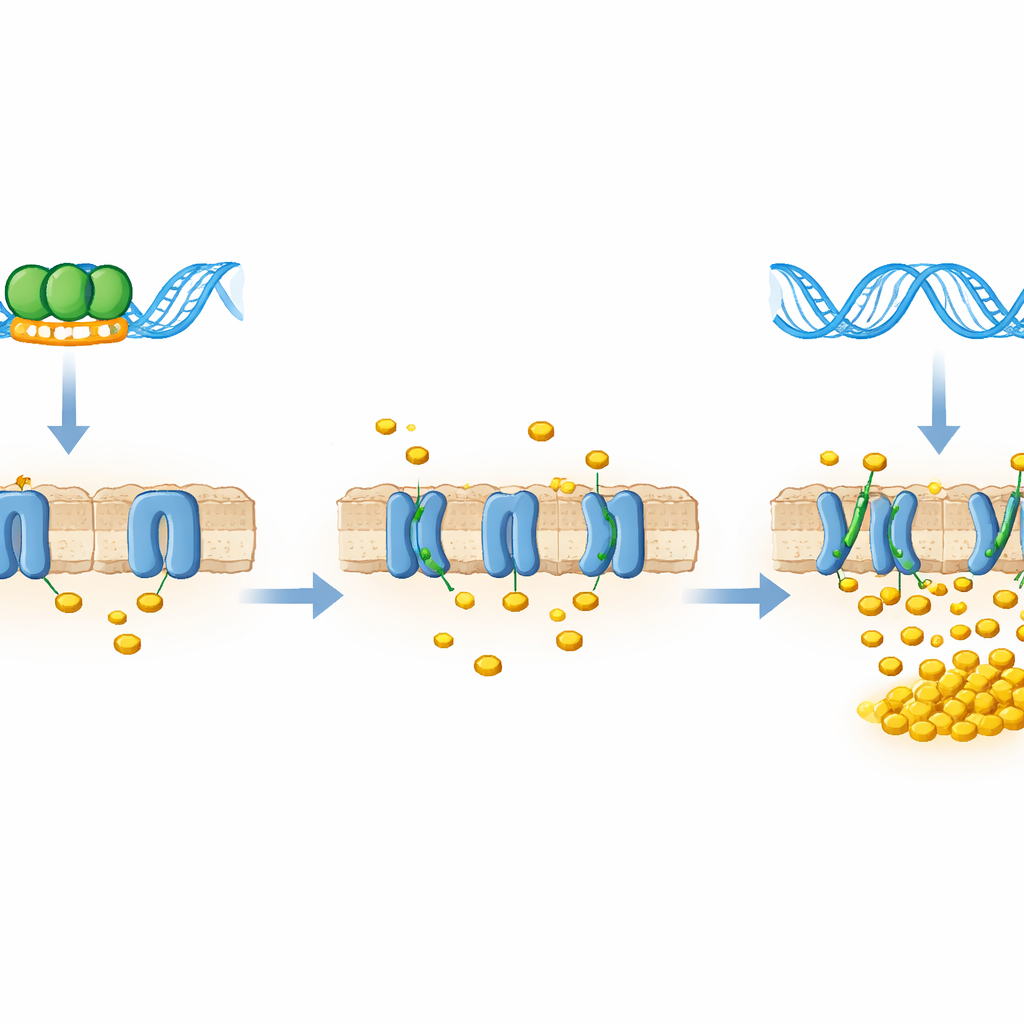
Wat dit betekent voor de strijd tegen tuberculose
Samengevat onthullen de bevindingen LtmA als een directe remmer van de mce4-cholesteroltransporter: wanneer LtmA gebonden is aan de mce4-controllocus, blijven de moleculaire deuren voor cholesterol gedeeltelijk gesloten; wanneer LtmA verminderd of afwezig is, gaan die deuren open en kan de bacterie zich tegoed doen. Hoewel het werk is uitgevoerd in een niet-pathogene modelsoort, is LtmA nauw verwant aan een eiwit in Mycobacterium tuberculosis, wat suggereert dat een vergelijkbare schakel kan bepalen hoe de verwekker tijdens infectie gastheercholesterol exploiteert. Als dat klopt, zouden geneesmiddelen die deze regulatorische knoop verstoren—of de transporter die zij beheerst—op termijn kunnen helpen tuberculosebacteriën in macrofagen uit te hongeren, wat een nieuwe invalshoek toevoegt aan de wereldwijde inspanning om deze hardnekkige ziekte te bestrijden.
Bronvermelding: Feng, YW., Yin, BC., Li, HB. et al. Regulatory mechanism of cholesterol transport via LtmA in Mycobacterium smegmatis. Sci Rep 16, 14235 (2026). https://doi.org/10.1038/s41598-026-43871-4
Trefwoorden: tuberculose, cholesterolopname, bacteriële regulatoren, mycobacteriën, gastheer–pathogeen interactie