Clear Sky Science · sv
Regleringsmekanism för kolesteroltransport via LtmA i Mycobacterium smegmatis
Varför denna studie är viktig
Tuberkulos är fortfarande en av världens dödligaste infektionssjukdomar, delvis därför att dess orsaksbakterie, Mycobacterium tuberculosis, är så skicklig på att överleva inne i våra immunceller. Ett av dess viktigaste knep är att livnära sig på vårt kolesterol och använda det för att stärka sina egna försvar. Denna studie, som använder en säker modellkusin till tuberkelbakterien kallad Mycobacterium smegmatis, avslöjar hur ett enda reglerande protein hjälper till att slå på eller av kolesterolupptaget — vilket ger ledtrådar till nya sätt att svälta ut dessa mikrober inne i kroppen.
Bakterien som äter vårt kolesterol
När tuberkulosbakterier tas upp av immunceller kallade makrofager blir de inte förstörda som många andra mikrober. I stället etablerar de sig i ett utrymme inne i cellen och omformar den omgivande membranen för att locka till sig kolesterol. Denna fettsyraliknande molekyl är inte bara en byggsten för bakteriecellväggen; den blir också en viktig källa till kol och energi, särskilt under långvariga infektioner när andra näringsämnen är knappare. Specialiserade transportsystem i bakteriers hölje, inklusive ett som kallas Mce4-komplexet, fungerar som molekylära dörrar som drar kolesterol från värdmiljön in i mikroben.
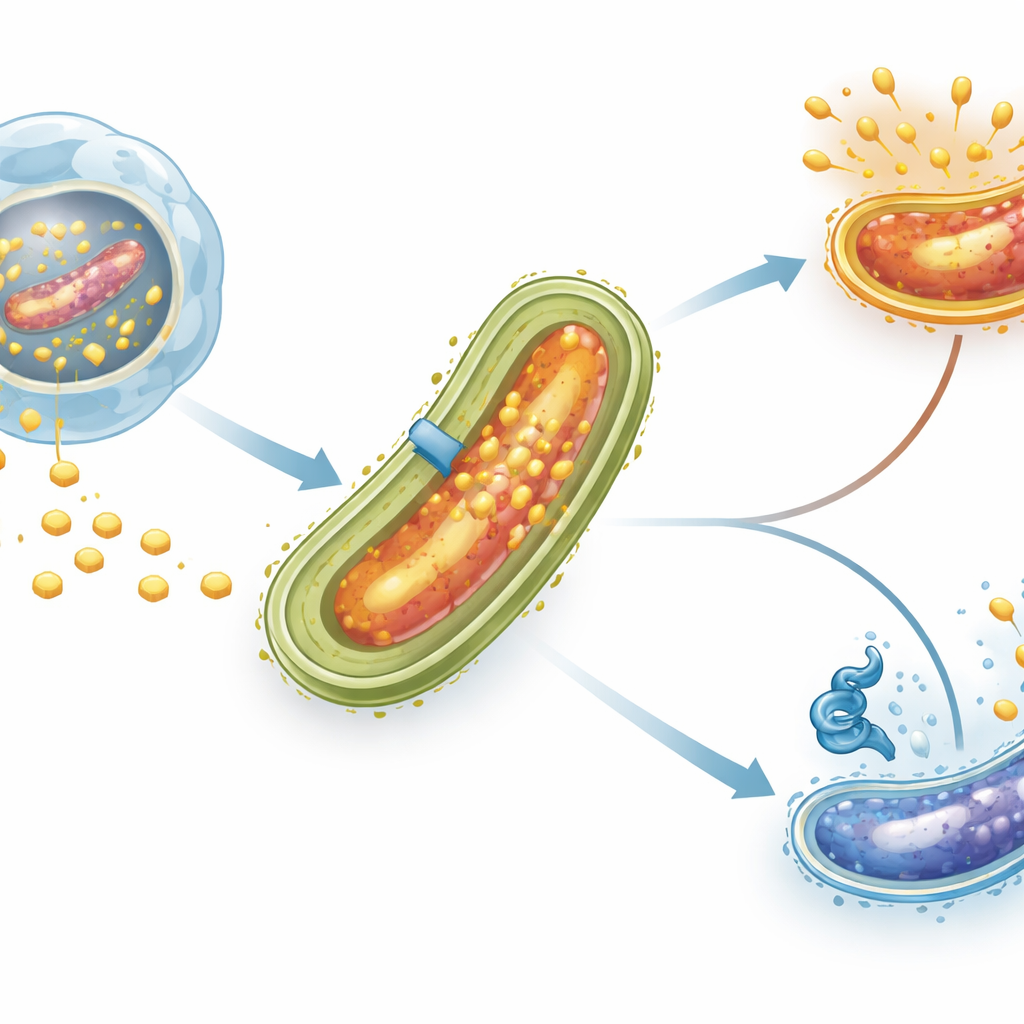
Ett trafikljus för kolesterolinträde
Forskarna fokuserade på ett reglerande protein som heter LtmA, tidigare känt för att påverka många lipidrelaterade gener. Proteiner som LtmA fungerar som "trafikljus" på bakteriens DNA och bestämmer vilka gener som ska vara aktiva och vilka som ska pausas. Med datoranalys identifierade teamet en kort DNA-sekvens framför mce4-genklustret som såg ut att vara en trolig bindningsplats för LtmA. De renade sedan LtmA i laboratoriet och utförde en teknik som kallas elektroforetisk mobilitetsförskjutningsanalys, vilken i praktiken testar om ett protein fysiskt binder till ett DNA-fragment. LtmA band tätt och specifikt till den normala mce4-kontrollregionen men inte till en variant där nyckelbaser var ändrade, vilket bekräftar att denna regulator direkt känner igen mce4-promotorn.
Att vrida upp eller ner kolesterolkranen
För att se vad denna bindning betyder för den levande bakterien konstruerade teamet stammar som antingen producerade mindre LtmA (nermodulering) eller extra LtmA (överuttryck). De mätte aktiviteten hos mce4-generna och fann ett spegelvänt mönster: när LtmA-nivåerna var låga ökade mängden mce4-transkript flera gånger; när LtmA var rikligt förekommande undertrycktes samma gener kraftigt. Funktionella tester stödde denna bild. I ett kolesterolupptagstest drog bakterier med reducerat LtmA in kolesterol snabbare och i större mängd än normala celler, medan de med överskott av LtmA halkade efter. LtmA fungerar med andra ord som en broms på kolesterolimportmaskineriet.
Tillväxt bara när kolesterol finns på menyn
Konsekvenserna av denna reglerande broms blev tydliga när forskarna odlade de olika bakteriestammarna på definierade kolkällor. När glukos fungerade som näring växte alla stammar — oavsett om de hade lite LtmA, normal eller mycket av det — lika bra och visade liknande metabolisk aktivitet. Men när kolesterol var den enda kolkällan vände bilden. Stammar med extra LtmA, och därmed mindre aktiva mce4-transportörer, växte dåligt och visade låg metabol aktivitet. Stammar med minskat LtmA, vars Mce4-dörrar var mer öppna, växte mer kraftigt och omsatte kolesterol mer intensivt. Detta visar att LtmA specifikt begränsar tillväxt under kolesterolberoende förhållanden genom att begränsa hur mycket av detta värdproducerade näringsämne som kan komma in i cellen.
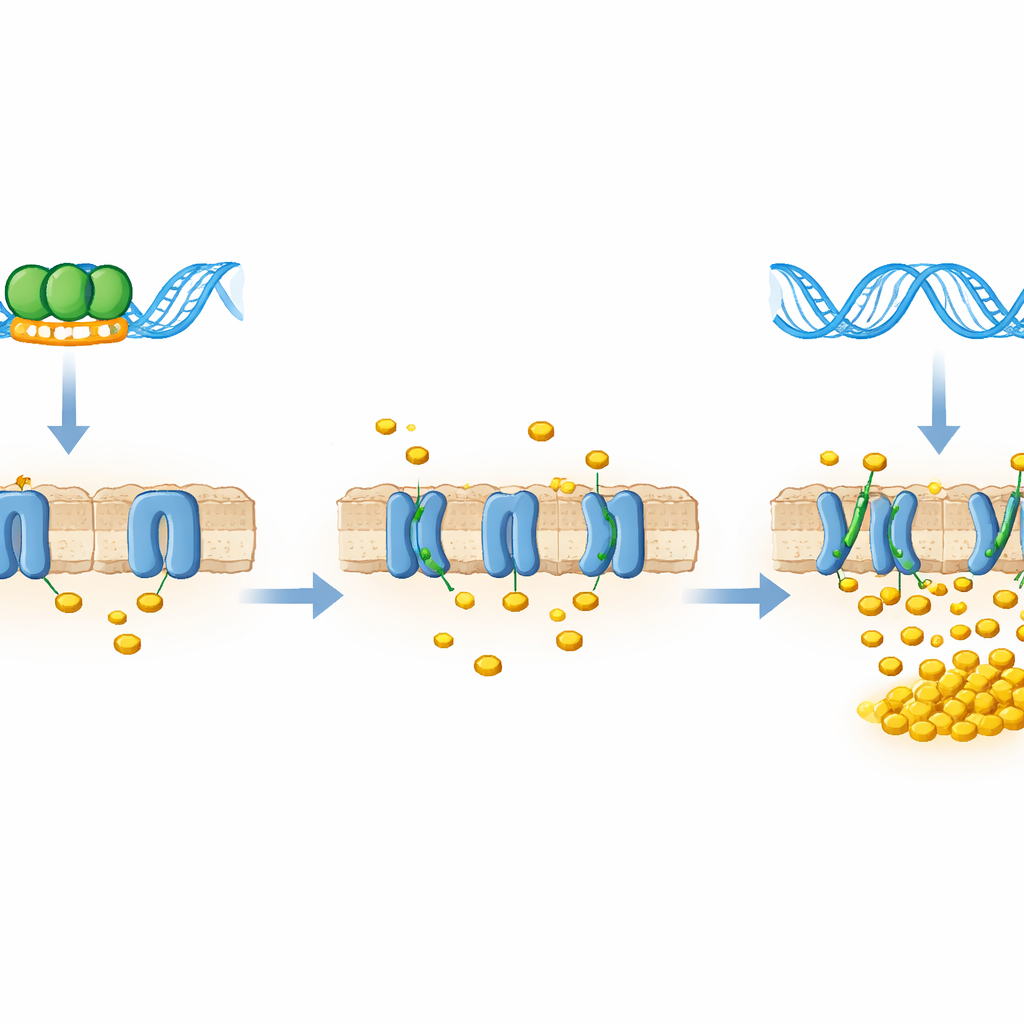
Vad detta betyder för kampen mot tuberkulos
Sammantaget visar fynden att LtmA är en direkt repressor av mce4-kolesteroltransportören: när LtmA är bundet till mce4-kontrollregionen förblir de molekylära dörrarna för kolesterol delvis stängda; när LtmA är reducerat eller frånvarande öppnas dessa dörrar och bakterien kan kalasa. Även om arbetet utfördes i en icke-patogen modellarart är LtmA nära besläktat med ett protein i Mycobacterium tuberculosis, vilket antyder att en liknande kontrollväxling kan påverka hur patogenen utnyttjar värdkolesterol under infektion. Om så är fallet kan läkemedel som stör denna regleringsnod — eller transportören den styr — en dag hjälpa till att svälta tuberkelbakterier inne i makrofager och ge en ny infallsvinkel i det globala arbetet för att kontrollera denna långlivade sjukdom.
Citering: Feng, YW., Yin, BC., Li, HB. et al. Regulatory mechanism of cholesterol transport via LtmA in Mycobacterium smegmatis. Sci Rep 16, 14235 (2026). https://doi.org/10.1038/s41598-026-43871-4
Nyckelord: tuberkulos, kolesterolupptag, bakteriella regulatorer, mykobakterier, värd–patogen-interaktion