Clear Sky Science · es
Mecanismo regulador del transporte de colesterol mediante LtmA en Mycobacterium smegmatis
Por qué importa este estudio
La tuberculosis sigue siendo una de las enfermedades infecciosas más mortales del mundo, en parte porque su bacteria causante, Mycobacterium tuberculosis, es muy eficaz para sobrevivir dentro de nuestras células inmunitarias. Una de sus estrategias clave es alimentarse de nuestro colesterol y usarlo para reforzar sus propias defensas. Este estudio, realizado con un primo seguro de la bacteria de la tuberculosis llamado Mycobacterium smegmatis, desvela cómo una única proteína reguladora ayuda a encender o apagar la captación de colesterol, ofreciendo pistas para nuevas maneras de privar de alimento a estos microbios dentro del organismo.
La bacteria que se come nuestro colesterol
Cuando las bacterias de la tuberculosis son engullidas por células inmunitarias llamadas macrófagos, no se destruyen como muchas otras. En cambio, se establecen en un compartimento dentro de la célula y remodelan la membrana circundante para atraer colesterol. Esta molécula grasa no es solo un componente de la pared celular bacteriana; también se convierte en una fuente importante de carbono y energía, especialmente durante infecciones prolongadas cuando otros nutrientes escasean. Sistemas transportadores especializados en el envoltorio bacteriano, incluido uno llamado complejo Mce4, actúan como puertas moleculares que extraen colesterol del entorno del huésped hacia el microbio.
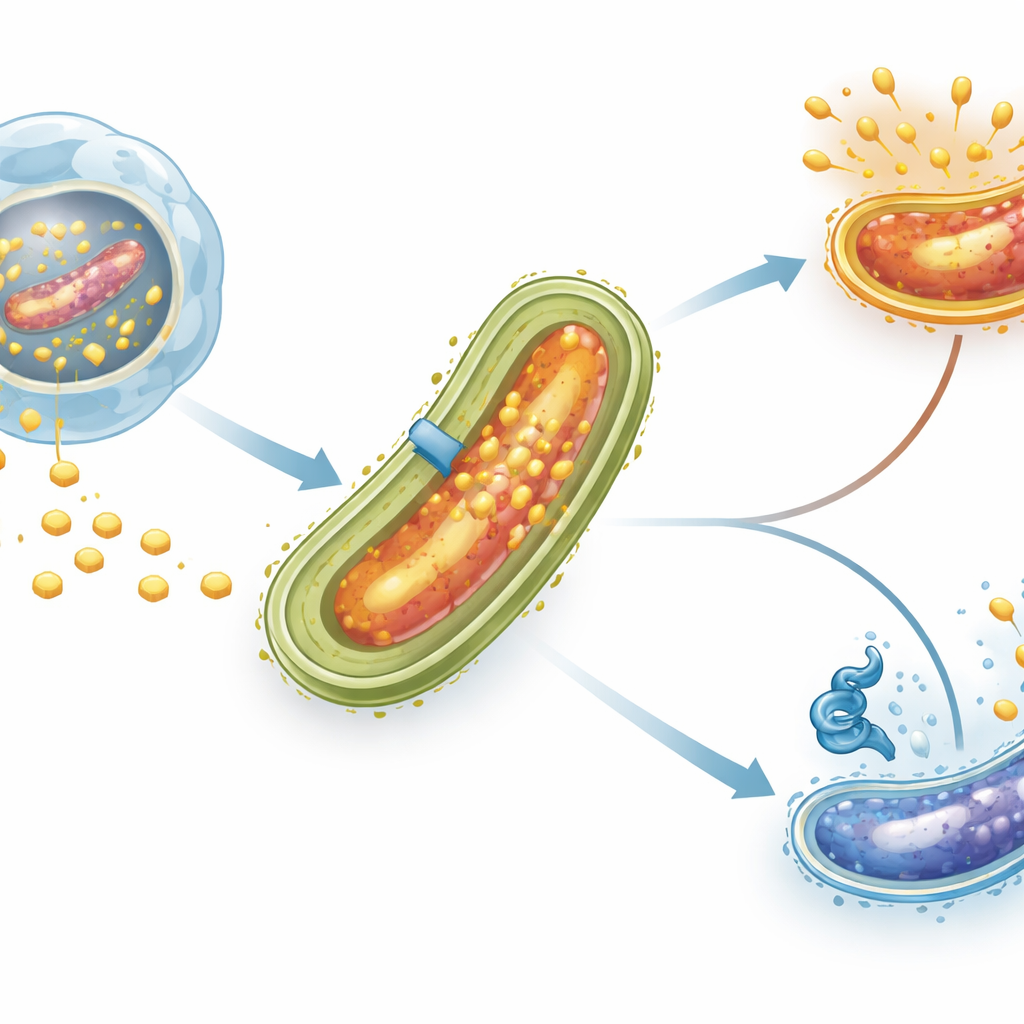
Un semáforo para la entrada de colesterol
Los investigadores se centraron en una proteína reguladora llamada LtmA, conocida previamente por influir en muchos genes relacionados con los lípidos. Proteínas como LtmA actúan como “semáforos” en el ADN bacteriano, decidiendo qué genes deben estar activos y cuáles en pausa. Mediante análisis computacionales, el equipo identificó una corta secuencia de ADN delante del grupo de genes mce4 que parecía un posible sitio de unión para LtmA. A continuación, purificaron LtmA en el laboratorio y realizaron una técnica llamada ensayo de movilidad electroforética (EMSA), que esencialmente prueba si una proteína se une físicamente a un fragmento de ADN. LtmA se unió con fuerza y de forma específica a la región de control normal de mce4, pero no a una versión con bases clave alteradas, confirmando que este regulador reconoce directamente el promotor de mce4.
Regular el grifo del colesterol
Para saber qué representa esa unión en la bacteria viva, el equipo diseñó cepas que producían menos LtmA (inhibición) o LtmA en exceso (sobreexpresión). Midieron la actividad de los genes mce4 y encontraron un patrón en espejo: cuando los niveles de LtmA eran bajos, los transcritos de los genes transportadores mce4 aumentaron varios pliegos; cuando LtmA era abundante, esos mismos genes se reprimieron de manera notable. Pruebas funcionales apoyaron este panorama. En un ensayo de captación de colesterol, las bacterias con LtmA reducido tomaron colesterol más rápido y en mayor cantidad que las células normales, mientras que las que tenían exceso de LtmA lo hicieron con menor eficacia. LtmA, en otras palabras, actúa como un freno sobre la maquinaria de importación de colesterol.
Crecimiento solo cuando el colesterol está en el menú
Las consecuencias de este freno regulador se hicieron evidentes cuando los científicos cultivaron las distintas cepas bacterianas con fuentes de carbono definidas. Cuando la glucosa sirvió de alimento, todas las cepas—con poco LtmA, normales o con exceso—crecieron igual de bien y mostraron actividad metabólica similar. Pero cuando el colesterol fue la única fuente de carbono, la situación cambió. Las cepas con LtmA extra, y por tanto con transportadores mce4 menos activos, crecieron pobremente y mostraron baja actividad metabólica. Las cepas con LtmA disminuido, cuyas puertas Mce4 estaban más abiertas, crecieron con mayor robustez y metabolizaron el colesterol con más vigor. Esto demuestra que LtmA limita específicamente el crecimiento en condiciones dependientes del colesterol al restringir la entrada de este nutriente derivado del huésped.
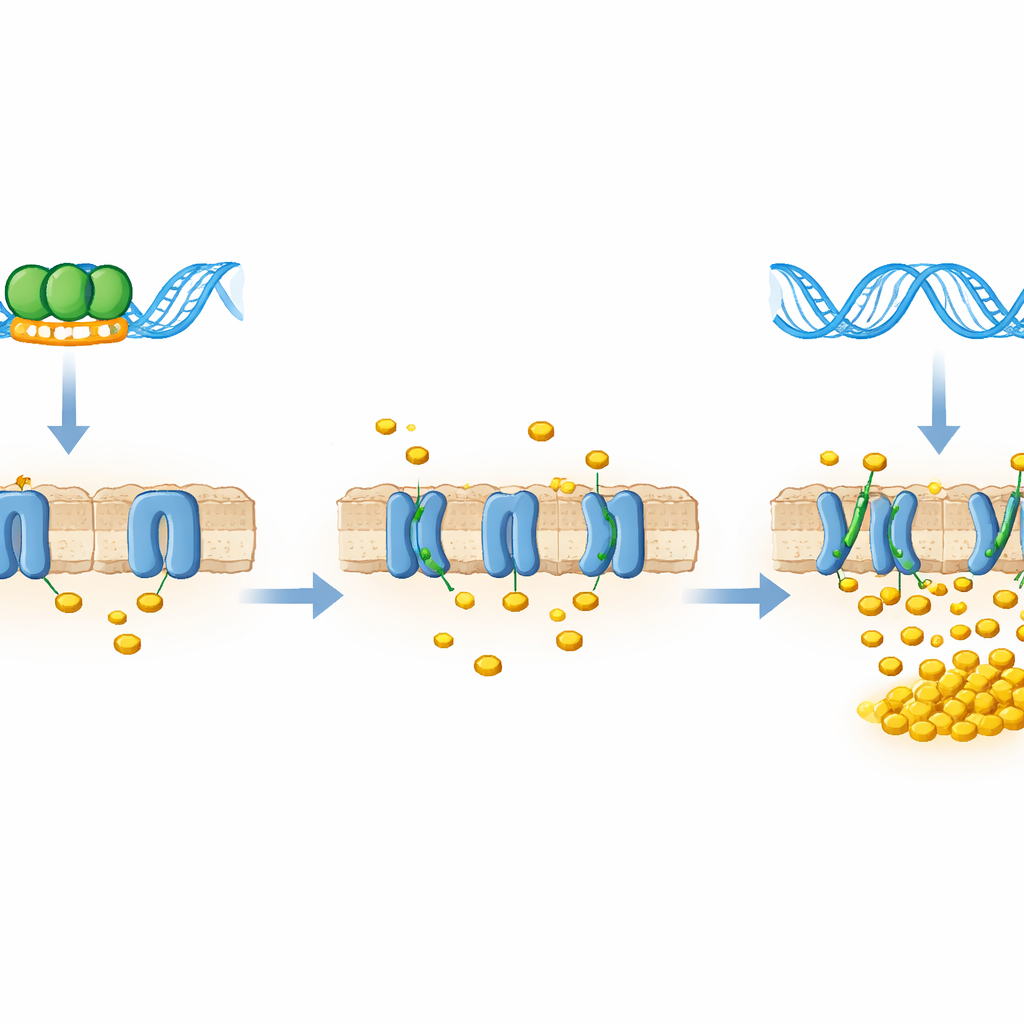
Qué significa esto para combatir la tuberculosis
En conjunto, los hallazgos revelan a LtmA como un represor directo del transportador de colesterol mce4: cuando LtmA está unido a la región de control de mce4, las puertas moleculares para el colesterol permanecen parcialmente cerradas; cuando LtmA se reduce o falta, esas puertas se abren y la bacteria puede alimentarse. Aunque el trabajo se realizó en una especie modelo no patógena, LtmA es muy similar a una proteína de Mycobacterium tuberculosis, lo que sugiere que un interruptor de control parecido podría influir en cómo el patógeno explota el colesterol del huésped durante la infección. Si es así, fármacos que interfieran con este nodo regulador—o con el transportador que controla—podrían algún día ayudar a privar de alimento a las bacterias de la tuberculosis dentro de los macrófagos, añadiendo un nuevo ángulo al esfuerzo global por controlar esta persistente enfermedad.
Cita: Feng, YW., Yin, BC., Li, HB. et al. Regulatory mechanism of cholesterol transport via LtmA in Mycobacterium smegmatis. Sci Rep 16, 14235 (2026). https://doi.org/10.1038/s41598-026-43871-4
Palabras clave: tuberculosis, captación de colesterol, reguladores bacterianos, micobacterias, interacción huésped–patógeno