Clear Sky Science · fr
Mécanisme de régulation du transport du cholestérol via LtmA chez Mycobacterium smegmatis
Pourquoi cette étude est importante
La tuberculose reste l’une des maladies infectieuses les plus mortelles au monde, en partie parce que la bactérie responsable, Mycobacterium tuberculosis, sait très bien survivre à l’intérieur de nos cellules immunitaires. L’un de ses principaux tours consiste à se nourrir de notre cholestérol et à l’utiliser pour renforcer ses propres défenses. Cette étude, réalisée à l’aide d’un cousin non pathogène de la bactérie de la tuberculose appelé Mycobacterium smegmatis, met au jour comment une seule protéine régulatrice permet d’allumer ou d’éteindre l’entrée du cholestérol — offrant des pistes pour de nouvelles façons d’affamer ces microbes à l’intérieur de l’organisme.
La bactérie qui mange notre cholestérol
Quand les bacilles de la tuberculose sont phagocytés par des cellules immunitaires appelées macrophages, ils ne sont pas détruits comme le sont de nombreux autres microbes. Au lieu de cela, ils s’installent dans un compartiment intracellulaire et remodèlent la membrane qui l’entoure pour attirer le cholestérol. Cette molécule lipidique n’est pas seulement un élément de construction de la paroi bactérienne ; elle devient aussi une source majeure de carbone et d’énergie, notamment lors d’infections persistantes où d’autres nutriments se font rares. Des systèmes de transport spécialisés dans l’enveloppe bactérienne, dont un complexe nommé Mce4, agissent comme des portes moléculaires qui extraient le cholestérol de l’environnement de l’hôte vers le microbe.
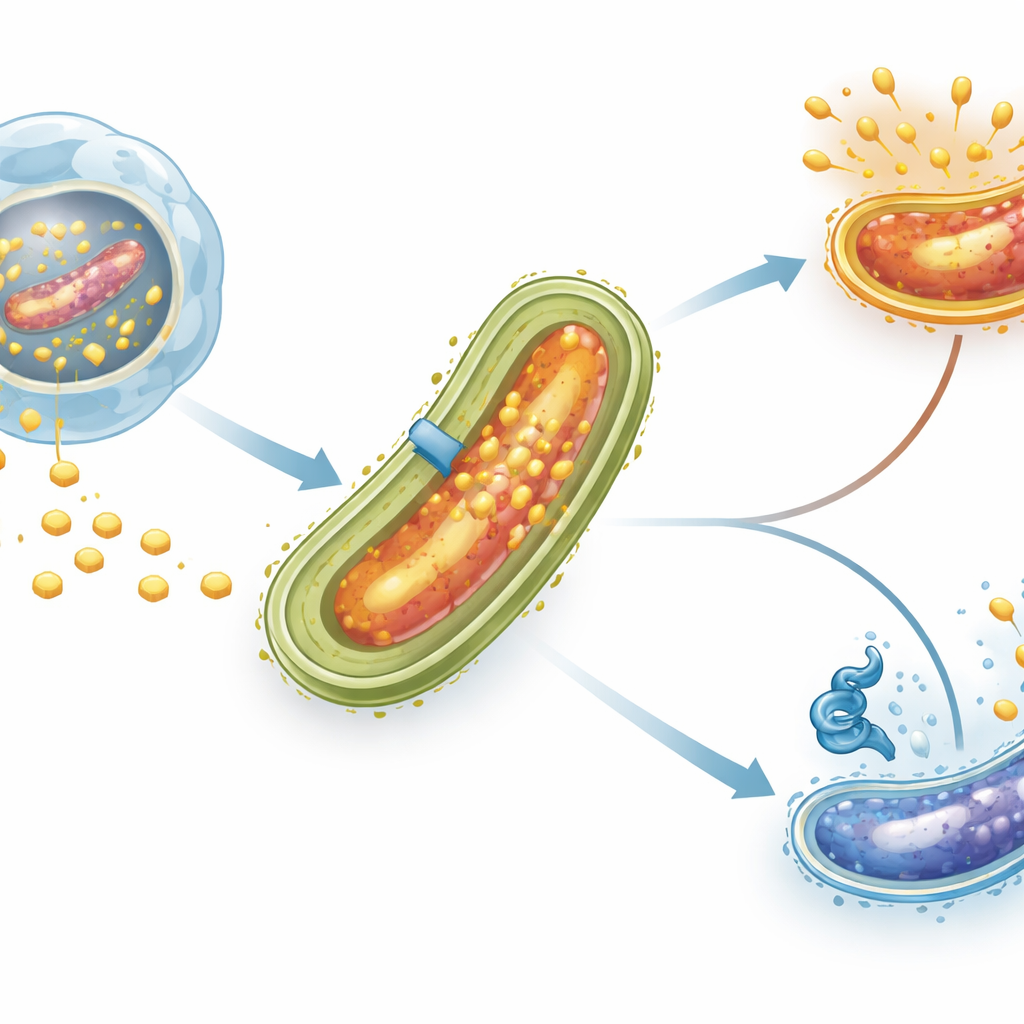
Un feu de signalisation pour l’entrée du cholestérol
Les chercheurs se sont intéressés à une protéine régulatrice nommée LtmA, déjà connue pour influer sur de nombreux gènes liés aux lipides. Des protéines comme LtmA agissent comme des « feux de circulation » sur l’ADN bactérien, décidant quels gènes doivent être actifs et lesquels doivent être mis en pause. Grâce à une analyse informatique, l’équipe a identifié une courte séquence d’ADN en amont du groupe de gènes mce4 qui ressemblait à un site d’ancrage probable pour LtmA. Ils ont ensuite purifié LtmA en laboratoire et réalisé une technique appelée test de mobilité électrophorétique, qui vérifie essentiellement si une protéine se lie physiquement à un fragment d’ADN. LtmA se lia fermement et spécifiquement à la région de contrôle normale du mce4 mais pas à une version dont les bases clés avaient été altérées, confirmant que ce régulateur reconnaît directement le promoteur de mce4.
Régler le robinet du cholestérol
Pour comprendre la signification de cette liaison pour la bactérie vivante, l’équipe a conçu des souches produisant soit moins de LtmA (extinction partielle), soit un excès de LtmA (surexpression). Ils ont mesuré l’activité des gènes mce4 et observé un schéma en miroir : quand les niveaux de LtmA étaient faibles, les transcrits des gènes transporteurs mce4 augmentaient de plusieurs fois ; quand LtmA était abondant, ces mêmes gènes étaient fortement réprimés. Des tests fonctionnels confirment ce tableau. Dans un essai d’absorption du cholestérol, les bactéries à LtmA réduit ont capté le cholestérol plus rapidement et en plus grande quantité que les cellules normales, tandis que celles avec un excès de LtmA étaient à la traîne. Autrement dit, LtmA agit comme un frein sur la machinerie d’importation du cholestérol.
Croissance seulement quand le cholestérol est au menu
Les conséquences de ce frein régulateur sont apparues lorsque les scientifiques ont cultivé les différentes souches bactériennes sur des sources de carbone définies. Lorsque le glucose servait d’aliment, toutes les souches — à LtmA réduit, normales ou en excès — se développaient de la même manière et montraient une activité métabolique comparable. Mais lorsque le cholestérol était la seule source de carbone, la situation s’est inversée. Les souches avec un excès de LtmA, et donc des transporteurs mce4 moins actifs, croissaient peu et présentaient une faible activité métabolique. Les souches avec LtmA diminué, dont les portes Mce4 étaient plus ouvertes, se développaient de manière plus robuste et métabolisaient le cholestérol plus vigoureusement. Cela montre que LtmA limite spécifiquement la croissance dans des conditions dépendantes du cholestérol en restreignant la quantité de ce nutriment dérivé de l’hôte pouvant pénétrer dans la cellule.
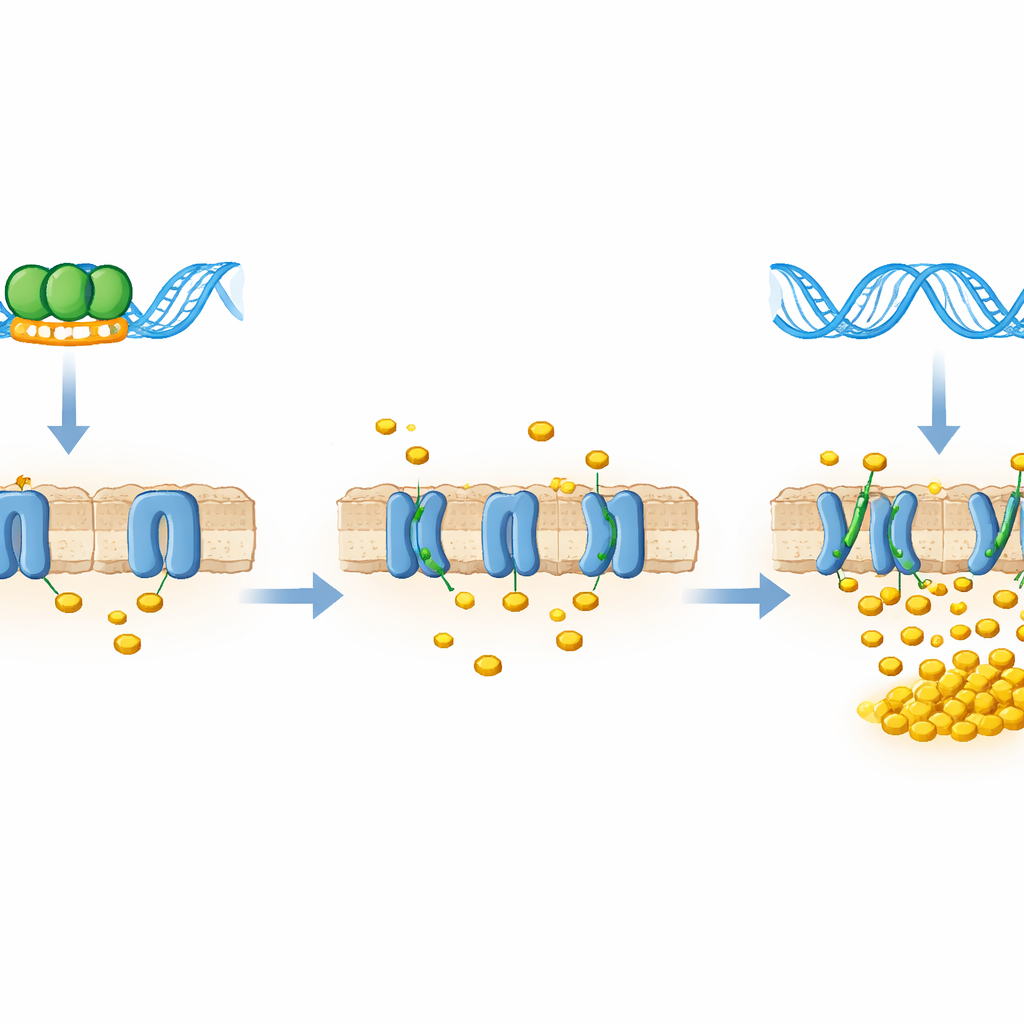
Ce que cela signifie pour la lutte contre la tuberculose
Pris ensemble, les résultats révèlent LtmA comme un répresseur direct du transporteur de cholestérol mce4 : lorsque LtmA est lié à la région de contrôle de mce4, les portes moléculaires du cholestérol restent partiellement fermées ; quand LtmA est réduit ou absent, ces portes s’ouvrent et la bactérie peut se nourrir. Bien que les travaux aient été réalisés sur une espèce modèle non pathogène, LtmA est étroitement apparenté à une protéine de Mycobacterium tuberculosis, ce qui suggère qu’un interrupteur de contrôle similaire pourrait influencer la façon dont le pathogène exploite le cholestérol de l’hôte pendant l’infection. Si tel est le cas, des médicaments qui perturbent ce nœud régulateur — ou le transporteur qu’il contrôle — pourraient un jour aider à affamer les bactéries de la tuberculose à l’intérieur des macrophages, ajoutant un nouvel angle aux efforts mondiaux pour contrôler cette maladie persistante.
Citation: Feng, YW., Yin, BC., Li, HB. et al. Regulatory mechanism of cholesterol transport via LtmA in Mycobacterium smegmatis. Sci Rep 16, 14235 (2026). https://doi.org/10.1038/s41598-026-43871-4
Mots-clés: tuberculose, absorption du cholestérol, régulateurs bactériens, mycobactéries, interaction hôte–pathogène