Clear Sky Science · de
Regulatorischer Mechanismus des Cholesterintransports über LtmA in Mycobacterium smegmatis
Warum diese Studie wichtig ist
Tuberkulose bleibt eine der tödlichsten Infektionskrankheiten der Welt, teilweise weil ihr Erreger, Mycobacterium tuberculosis, so gut darin ist, in unseren Immunzellen zu überleben. Ein zentrales Täuschungsmanöver besteht darin, sich von unserem Cholesterin zu ernähren und es zur Verstärkung eigener Abwehrmechanismen zu verwenden. Diese Studie, durchgeführt an einem harmlosen Modellverwandten des Tuberkulose-Erregers namens Mycobacterium smegmatis, zeigt, wie ein einzelnes Regulationsprotein die Cholesterinaufnahme an- und abschaltet – und liefert damit Hinweise auf neue Wege, diese Mikroben im Körper auszuhungern.
Das Bakterium, das unser Cholesterin nutzt
Wenn Tuberkulose-Bakterien von Immunzellen, den Makrophagen, aufgenommen werden, werden sie nicht wie viele andere Mikroben zerstört. Stattdessen nisten sie sich in einem Kompartiment innerhalb der Zelle ein und verändern die umliegende Membran, um Cholesterin anzuziehen. Dieses fettartige Molekül ist nicht nur ein Baustein der bakteriellen Zellwand; es wird besonders während langwieriger Infektionen, wenn andere Nährstoffe knapp sind, zu einer wichtigen Quelle für Kohlenstoff und Energie. Spezialisierte Transportsysteme in der bakteriellen Hülle, darunter der sogenannte Mce4-Komplex, fungieren wie molekulare Türen, die Cholesterin aus der Wirtsumgebung in das Mikroorganismus hineinziehen.
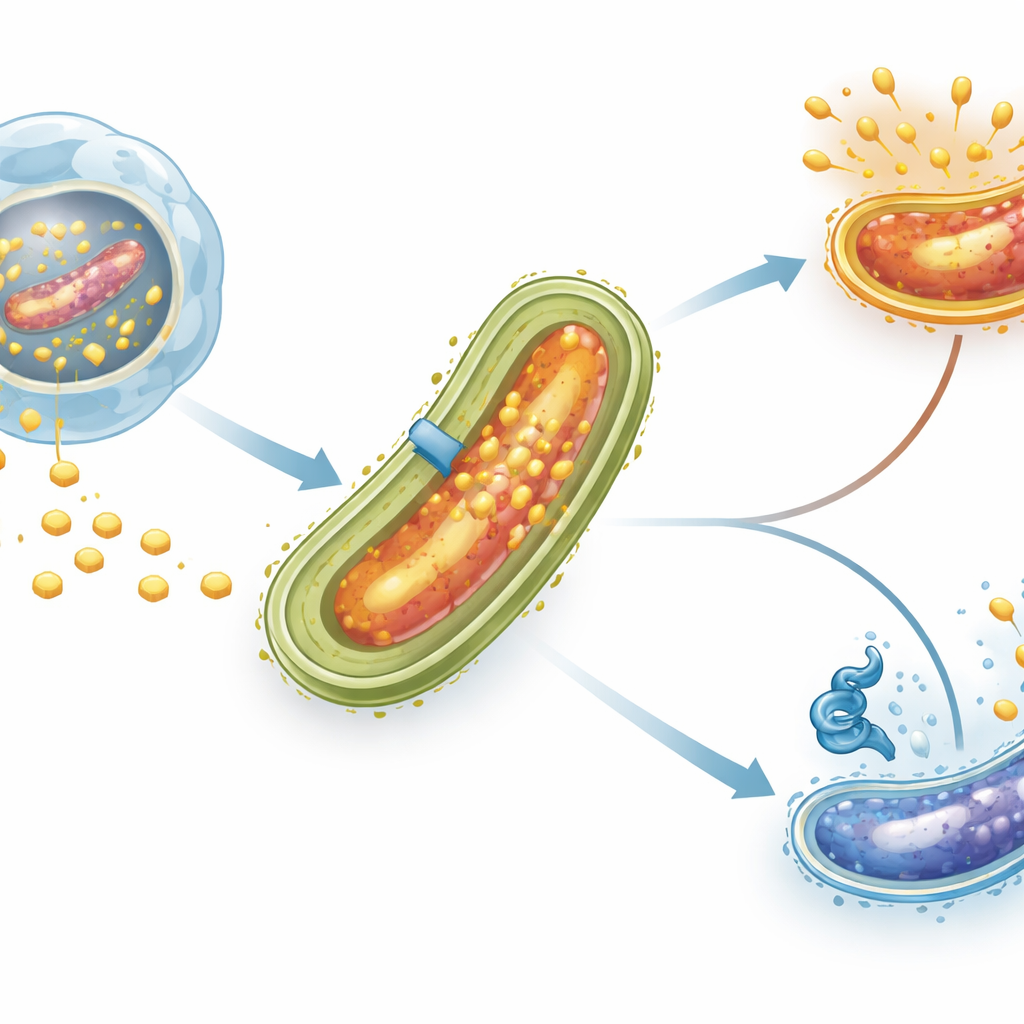
Ein Ampelsystem für den Cholesterinzutritt
Die Forscher konzentrierten sich auf ein Regulationsprotein namens LtmA, das zuvor dafür bekannt war, zahlreiche lipidbezogene Gene zu beeinflussen. Proteine wie LtmA wirken wie „Ampeln“ auf der bakteriellen DNA und entscheiden, welche Gene aktiviert und welche pausiert werden. Mithilfe von Computeranalysen identifizierte das Team eine kurze DNA-Sequenz vor dem mce4-Gencluster, die wie eine wahrscheinliche Andockstelle für LtmA aussah. Anschließend reinigten sie LtmA im Labor und führten eine Elektrophoretische Mobilitätsverschiebungs-Assay (EMSA) durch, ein Verfahren, das im Wesentlichen prüft, ob ein Protein ein DNA-Fragment physisch bindet. LtmA band sich fest und spezifisch an die normale mce4-Kontrollregion, aber nicht an eine Version, deren Schlüsselbasen verändert worden waren, was bestätigte, dass dieser Regulator den mce4-Promotor direkt erkennt.
Den Cholesterinhahn auf- oder zudrehen
Um zu sehen, was diese Bindung für das lebende Bakterium bedeutet, erzeugte das Team Stämme, die entweder weniger LtmA produzierten (Herunterregulierung) oder zusätzliches LtmA herstellten (Überexpression). Sie maßen die Aktivität der mce4-Gene und fanden ein spiegelbildliches Muster: Bei niedrigen LtmA-Spiegeln stiegen die Transkripte der mce4-Transportergene um das Mehrfache; bei hohem LtmA-Gehalt wurden dieselben Gene stark reprimiert. Funktionelle Tests stützten dieses Bild. In einem Cholesterinaufnahme-Assay nahmen Bakterien mit reduziertem LtmA Cholesterin schneller und in größeren Mengen auf als normale Zellen, während solche mit überschüssigem LtmA zurückblieben. LtmA wirkt demnach wie eine Bremse für die Cholesterinimport-Maschinerie.
Wachstum nur, wenn Cholesterin auf dem Speiseplan steht
Die Folgen dieser regulatorischen Bremse wurden deutlich, als die Wissenschaftler die verschiedenen bakteriellen Stämme auf definierten Kohlenstoffquellen kultivierten. Wenn Glukose als Nahrungsquelle diente, wuchsen alle Stämme – ob LtmA-vermindert, normal oder übermäßig vorhanden – gleichermaßen gut und zeigten ähnliche Stoffwechselaktivität. Wenn jedoch Cholesterin die einzige Kohlenstoffquelle war, kehrte sich das Bild um. Stämme mit zusätzlichem LtmA und damit weniger aktiven mce4-Transportern wuchsen schlecht und zeigten eine geringe Stoffwechselaktivität. Stämme mit verringertem LtmA, deren Mce4-Türen weiter geöffnet waren, wuchsen robuster und bauten Cholesterin kräftiger ab. Das zeigt, dass LtmA das Wachstum unter cholesterinabhängigen Bedingungen gezielt einschränkt, indem es begrenzt, wie viel dieses wirtseigenen Nährstoffs in die Zelle gelangt.
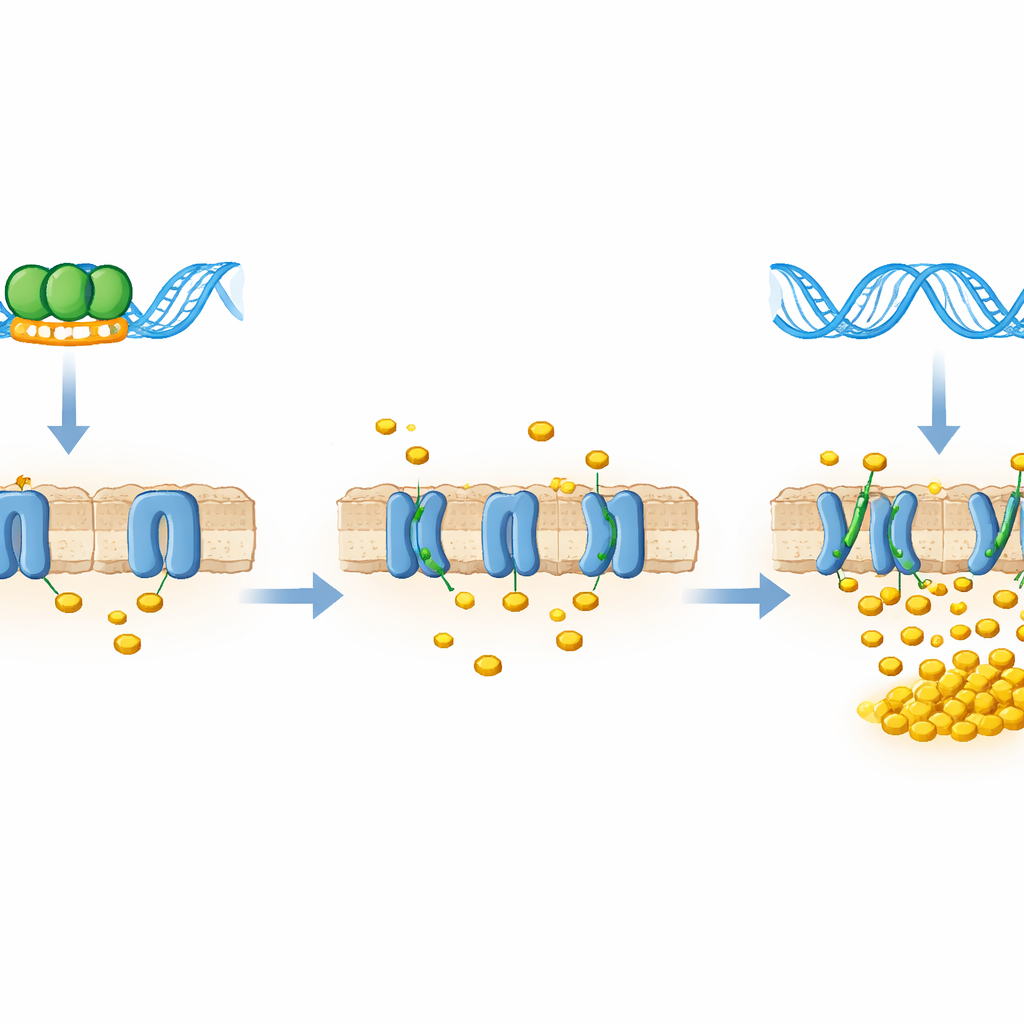
Was das für den Kampf gegen Tuberkulose bedeutet
Zusammengefasst zeigen die Ergebnisse, dass LtmA ein direkter Repressor des mce4-Cholesterintransporters ist: Wenn LtmA an die mce4-Kontrollregion gebunden ist, bleiben die molekularen Türen für Cholesterin teilweise geschlossen; ist LtmA reduziert oder fehlt es, öffnen sich diese Türen und das Bakterium kann sich ernähren. Obwohl die Arbeit an einer nicht-pathogenen Modellart durchgeführt wurde, ist LtmA eng verwandt mit einem Protein in Mycobacterium tuberculosis, was nahelegt, dass ein ähnlicher Schaltmechanismus beeinflusst, wie der Erreger während der Infektion Wirtscholesterin ausnutzt. Falls dem so ist, könnten Wirkstoffe, die diesen regulatorischen Knoten – oder den von ihm kontrollierten Transporter – stören, eines Tages dazu beitragen, Tuberkulosebakterien in Makrophagen auszuhungern und damit einen neuen Ansatz zur Bekämpfung dieser hartnäckigen Krankheit bieten.
Zitation: Feng, YW., Yin, BC., Li, HB. et al. Regulatory mechanism of cholesterol transport via LtmA in Mycobacterium smegmatis. Sci Rep 16, 14235 (2026). https://doi.org/10.1038/s41598-026-43871-4
Schlüsselwörter: Tuberkulose, Cholesterinaufnahme, bakterielle Regulatoren, Mykobakterien, Wirt–Pathogen-Interaktion