Clear Sky Science · zh
糖尿病相关脂质自噬中关键基因 CCR1 与 EGR2 的鉴定与验证
为何脂肪和糖会压垮我们的细胞
通常我们把 2 型糖尿病视为糖代谢的问题,但脂肪同样扮演着同等重要且紧密相关的角色。当机体被过量热量淹没时,脂滴会在肝脏和肌肉等器官内堆积。健康细胞可以通过分解这些储存的脂肪来“清理家园”,但在糖尿病中,这一清理系统失灵。本文总结的研究提出了一个既简单又有力的问题:哪些基因位于脂肪过载、细胞清理失常与血糖升高的交汇处——并可能成为新的预警标志或治疗靶点?
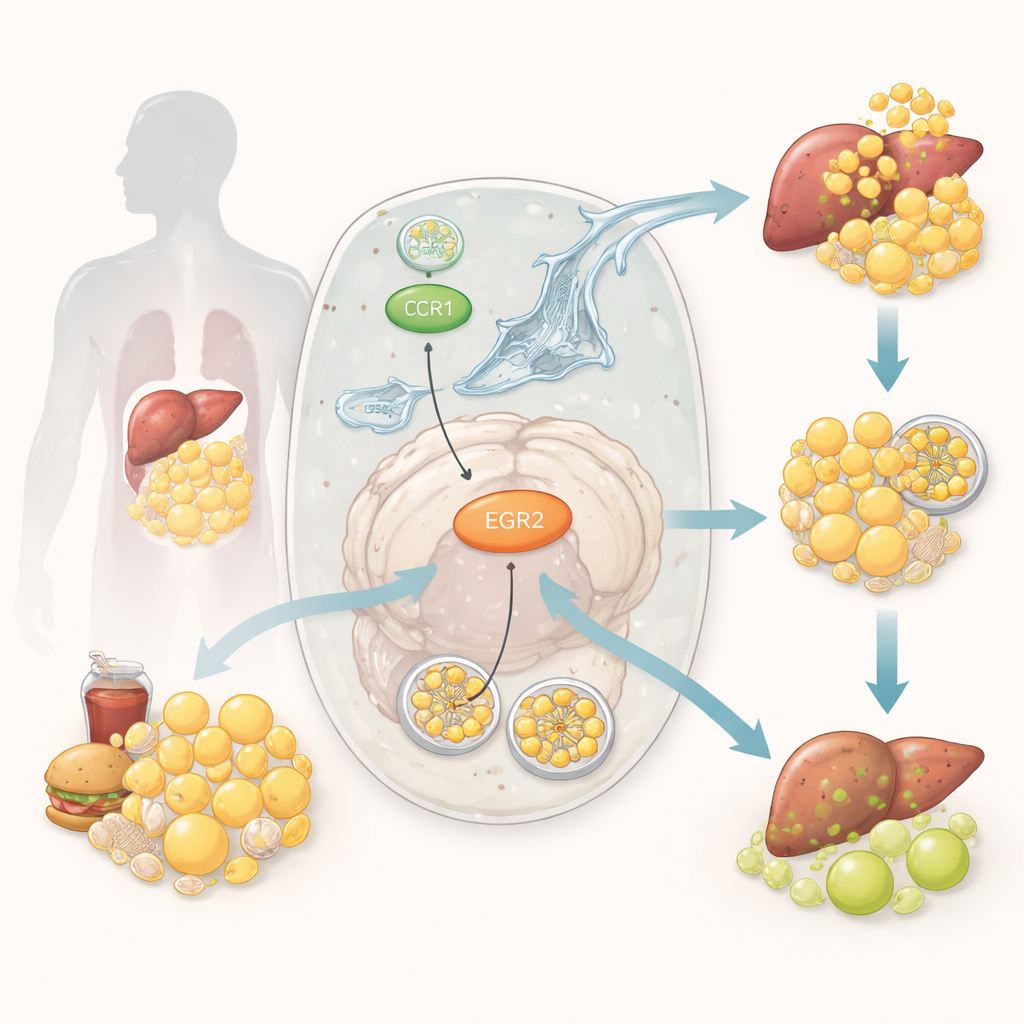
负责清理细胞内脂肪的机制
在细胞内部,一条专门的回收通路称为脂质自噬,帮助打包并消化微小的脂肪滴。可以把它想象为一辆细胞级的垃圾车,收集过剩脂肪并把它们运到处理中心,以便安全再利用。当脂质自噬运行良好时,脂肪储备保持平衡,细胞对胰岛素的反应正常;一旦被破坏,脂肪就在肝脏和肌肉等组织中堆积,助长炎症并削弱胰岛素的作用。尽管科学家已知错误的脂质处理和失调的细胞回收都参与糖尿病,但将这些过程连接起来的精确分子开关尚不清楚。
从人类数据中寻找关键开关
研究人员首先挖掘了公共数据库中来自糖尿病患者与非糖尿病者血液的基因表达数据。利用统计工具和网络分析,他们将数千个基因筛选到一小组,这些基因在糖尿病中活动有一致变化并且已与脂质代谢或细胞回收相关。接着他们应用了若干机器学习方法——这些技术允许计算机在复杂数据中找到稳健的模式——以精准识别哪些基因最好地区分糖尿病样本与非糖尿病样本。在这些独立方法的交叉验证中,两个基因反复脱颖而出,成为中心枢纽:CCR1 与 EGR2。两者在糖尿病样本中均更为活跃,且其表达水平往往同步升降。
在血液与肝脏中确认模式
为确保这些模式并非原始数据集的偶然现象,研究团队测试了来自有无 2 型糖尿病个体的新鲜血样。使用常规实验室检测,他们发现 CCR1 与 EGR2 蛋白在糖尿病者的血液中确实较高。随后,他们转向一种成熟的小鼠疾病模型,该模型会出现肥胖、脂肪肝和高血糖。在这些动物中,肝脏积累了大量脂滴,细胞回收通路的标志物显示出受阻的迹象。在相同肝脏中,CCR1 与 EGR2 水平明显升高,再次呼应了在人类血液中观察到的变化。综合来看,这些发现表明这两种基因与脂肪堆积、回收受损和血糖控制不良密切相关。
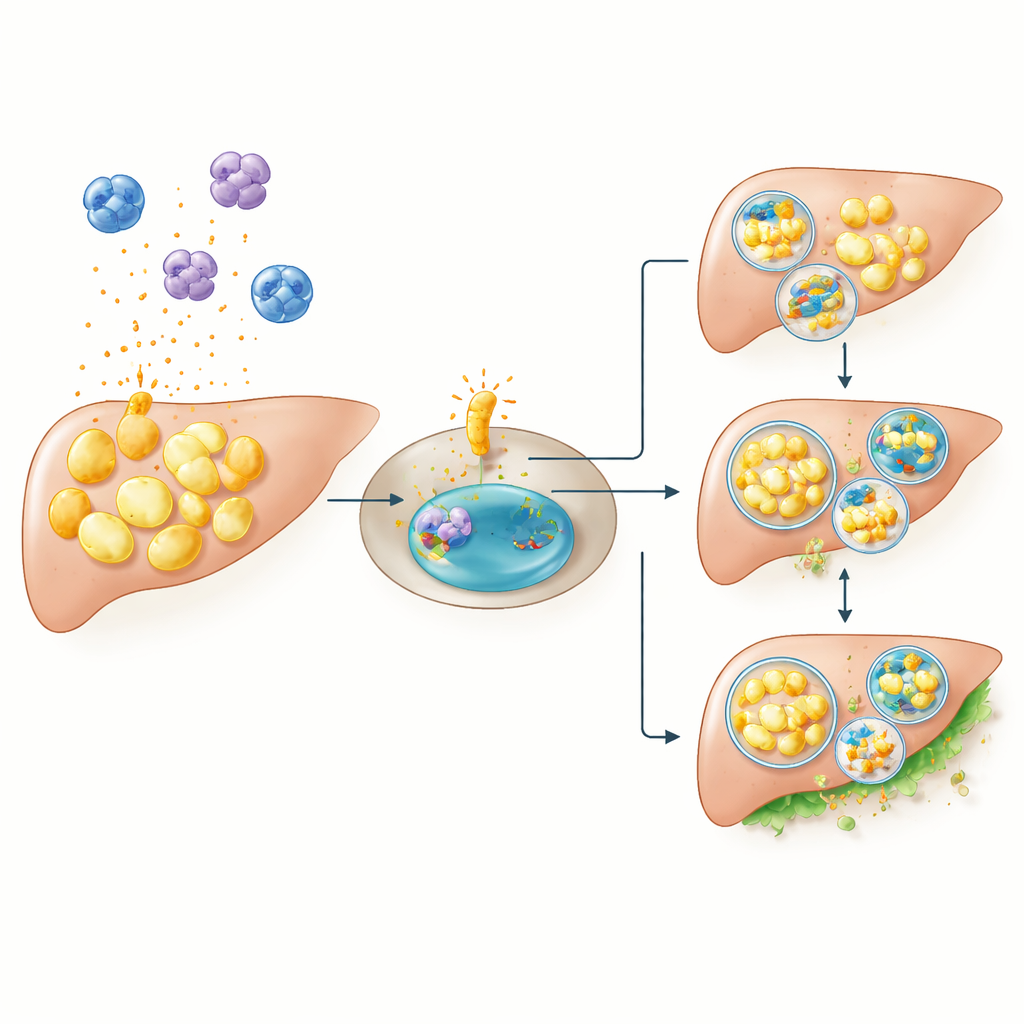
在小鼠中探究因果关系
仅凭相关性无法证明这些基因促成了糖尿病。为测试因果,研究人员构建了缺失 CCR1 的小鼠,并给予高脂饮食——这种应激通常会显著推高血糖。如预期,普通小鼠在高脂饮食下出现空腹和餐后血糖升高。与之形成鲜明对比的是,缺失 CCR1 的小鼠在相同高脂条件下大体保持受控:它们的血糖接近正常喂养的敲除动物水平。这提示 CCR1 并非维持日常葡萄糖平衡所必需,但在机体受到过量膳食脂肪挑战时成为关键因子,可能通过放大炎症并干扰细胞内的脂肪清除来发挥作用。
这对糖尿病患者意味着什么
通过结合大数据分析、人类血液测量与有针对性的小鼠实验,这项研究突出了 CCR1 与 EGR2 作为调节细胞在糖尿病中处理脂肪的潜在分子“旋钮”。这两基因水平升高与脂肪性、炎症性肝组织以及脂质自噬堵塞的迹象相关。重要的是,在小鼠中去除 CCR1 可削弱高脂饮食通常诱发的血糖升高,这指向一种可能的新治疗策略。尽管还需大量工作来阐明 CCR1 与 EGR2 在不同组织中如何具体调控脂肪回收,但它们已作为早期提示糖尿病的有前景生物标志物以及恢复细胞清除多余脂肪能力的药物起点脱颖而出。
引用: Liu, J., Zhang, X., Wang, Y. et al. Identification and verification of the key genes, CCR1 and EGR2, in diabetes-associated lipophagy. Sci Rep 16, 14274 (2026). https://doi.org/10.1038/s41598-026-43737-9
关键词: 2 型糖尿病, 脂质自噬, 脂肪肝, 炎症, 生物标志物