Clear Sky Science · it
Identificazione e verifica dei geni chiave, CCR1 ed EGR2, nella lipofagia associata al diabete
Perché grasso e zucchero possono sopraffare le nostre cellule
Il diabete di tipo 2 è spesso descritto come un problema dello zucchero, ma il grasso svolge un ruolo altrettanto importante e strettamente collegato. Quando il nostro organismo è sommerso da calorie in eccesso, goccioline di grasso si accumulano all’interno di organi come il fegato e i muscoli. Le cellule sane possono "fare pulizia" degradando questi grassi immagazzinati, ma nel diabete questo sistema di smaltimento vacilla. Lo studio qui riassunto pone una domanda semplice ma potente: quali geni si trovano all’incrocio tra sovraccarico di grasso, pulizia cellulare difettosa e aumento della glicemia — e potrebbero diventare nuovi segnali di allarme o bersagli terapeutici?
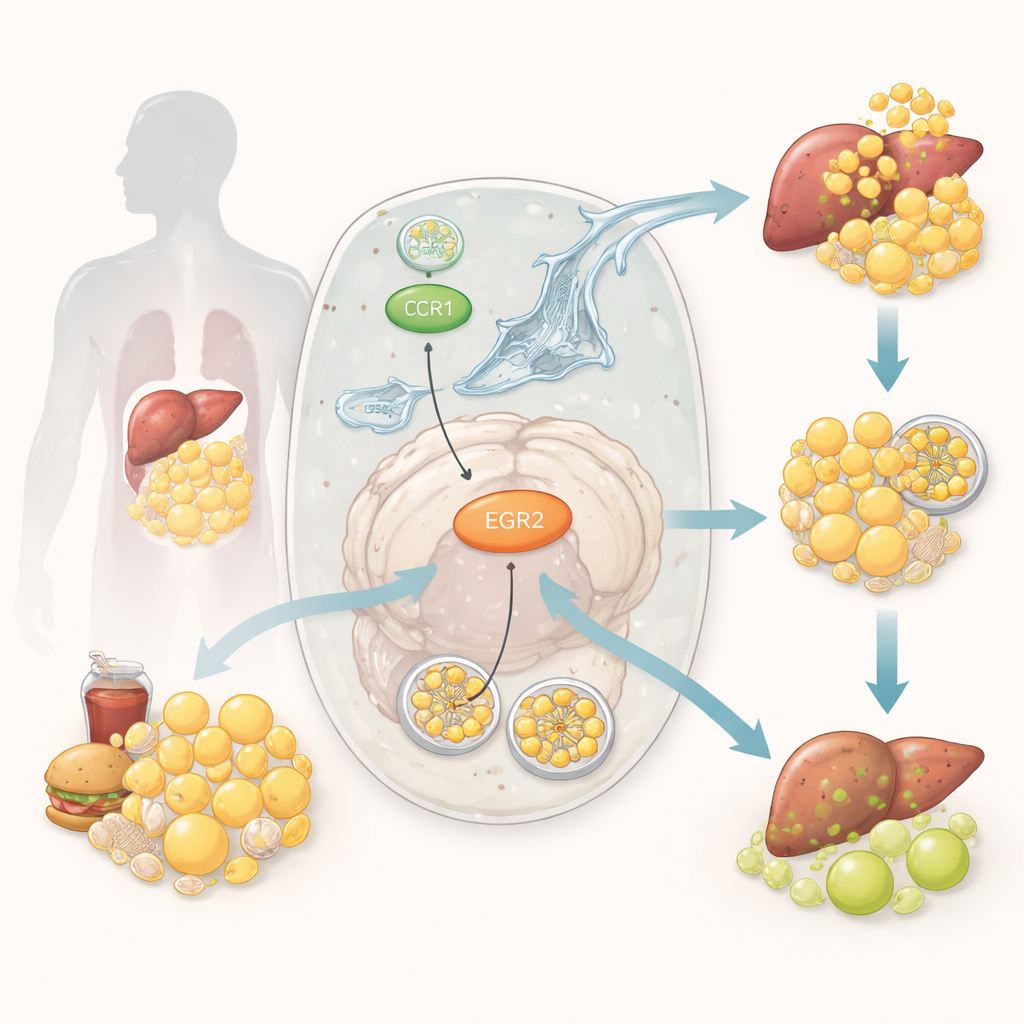
Una squadra di pulizia cellulare per il grasso
All’interno delle nostre cellule, un percorso di riciclo specializzato, chiamato lipofagia, aiuta a incapsulare e digerire piccole goccioline di grasso. Pensatelo come a un camion della spazzatura cellulare che raccoglie il grasso in eccesso e lo consegna a un centro di smaltimento affinché il contenuto possa essere riutilizzato in sicurezza. Quando la lipofagia funziona bene, le riserve di grasso restano in equilibrio e le cellule rispondono correttamente all’insulina. Quando è compromessa, il grasso si accumula nei tessuti come il fegato e il muscolo, alimentando l’infiammazione e rendendo più difficile l’azione dell’insulina. Sebbene gli scienziati sappiano che sia la cattiva gestione del grasso sia il riciclo cellulare alterato sono coinvolti nel diabete, gli interruttori molecolari precisi che collegano questi processi non erano chiari.
Caccia agli interruttori chiave nei dati umani
I ricercatori hanno iniziato esaminando grandi banche dati pubbliche di attività genica nel sangue di persone con e senza diabete. Utilizzando strumenti statistici e analisi di rete, hanno prima ridotto migliaia di geni a un piccolo gruppo la cui attività cambiava in modo coerente nel diabete e che erano già associati al metabolismo dei grassi o al riciclo cellulare. Hanno quindi applicato diversi metodi di apprendimento automatico — tecniche che permettono ai computer di trovare schemi robusti in dati complessi — per individuare quali geni distinguessero meglio i campioni diabetici da quelli non diabetici. Attraverso questi approcci indipendenti, due geni sono emersi ripetutamente come nodi centrali: CCR1 ed EGR2. Entrambi risultavano più attivi nei campioni diabetici e i loro livelli di espressione tendevano a variare in modo coordinato.
Confermare i modelli nel sangue e nel fegato
Per verificare che questi schemi non fossero semplici anomalie dei dataset iniziali, il team ha analizzato campioni di sangue freschi di persone con e senza diabete di tipo 2. Con un saggio di laboratorio standard, hanno riscontrato che sia le proteine CCR1 sia EGR2 erano effettivamente più alte nel sangue degli individui con diabete. Successivamente si sono rivolti a un modello murino ben consolidato della malattia, che sviluppa obesità, fegato grasso e iperglicemia. In questi animali il fegato presentava ampi depositi di grasso e i marker della via di riciclo cellulare mostravano segni di blocco. Negli stessi fegati, i livelli di CCR1 ed EGR2 erano chiaramente elevati, rispecchiando ancora una volta le modificazioni osservate nel sangue umano. Complessivamente, questi risultati suggeriscono che i due geni sono strettamente connessi alla combinazione di accumulo di grasso, riciclo compromesso e controllo glicemico alterato.
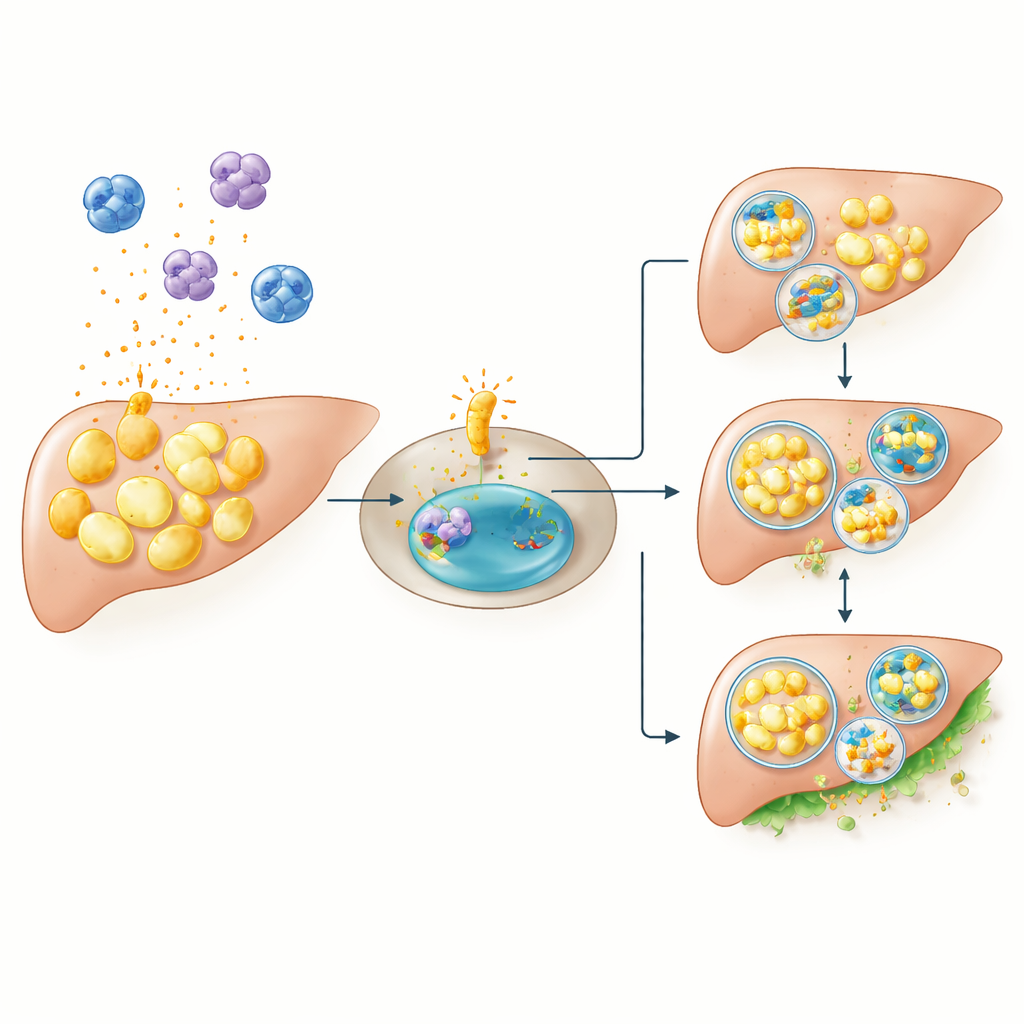
Mettere alla prova causa ed effetto nei topi
La sola correlazione non può provare che questi geni promuovano il diabete. Per testare causa ed effetto, i ricercatori hanno generato topi privi di CCR1 e li hanno esposti a una dieta ricca di grassi, uno stress che normalmente fa aumentare nettamente la glicemia. Come previsto, i topi normali alimentati con la dieta ricca hanno sviluppato elevati livelli di glucosio a digiuno e dopo i pasti. In netto contrasto, i topi senza CCR1 sono risultati in gran parte protetti: alle stesse condizioni ad alto contenuto di grassi, la loro glicemia è rimasta vicina a quella dei topi knock‑out normali. Ciò suggerisce che CCR1 non sia necessario per mantenere l’equilibrio glicemico quotidiano, ma diventi un attore critico quando l’organismo è sfidato dall’eccesso di grassi nella dieta, probabilmente amplificando l’infiammazione e interferendo con il corretto smaltimento del grasso all’interno delle cellule.
Cosa significa per le persone che convivono con il diabete
Combinando analisi di big data, misurazioni nel sangue umano ed esperimenti mirati nei topi, questo studio mette in luce CCR1 ed EGR2 come potenziali "manopole" molecolari che regolano il modo in cui le cellule gestiscono il grasso durante il diabete. Livelli più elevati di questi geni si associano a tessuto epatico grasso e infiammato e a segni che il sistema di lipofagia è intasato. È importante notare che la rimozione di CCR1 nei topi attenua l’aumento della glicemia normalmente indotto da una dieta ricca di grassi, indicando una possibile nuova strategia terapeutica. Pur restando molto lavoro da fare per chiarire esattamente come CCR1 ed EGR2 controllino il riciclo del grasso in tessuti diversi, essi emergono ora come promettenti biomarcatori per individuare il diabete precocemente e come punti di partenza per farmaci volti a ripristinare la capacità cellulare di eliminare l’eccesso di grasso.
Citazione: Liu, J., Zhang, X., Wang, Y. et al. Identification and verification of the key genes, CCR1 and EGR2, in diabetes-associated lipophagy. Sci Rep 16, 14274 (2026). https://doi.org/10.1038/s41598-026-43737-9
Parole chiave: diabete di tipo 2, lipofagia, fegato grasso, infiammazione, biomarcatori