Clear Sky Science · pt
Identificação e verificação dos genes-chave, CCR1 e EGR2, na lipofagia associada ao diabetes
Por que gordura e açúcar podem sobrecarregar nossas células
O diabetes tipo 2 costuma ser descrito como um problema de açúcar, mas a gordura tem um papel igualmente importante e intimamente ligado. Quando nossos corpos são inundados por calorias em excesso, gotículas de gordura se acumulam dentro de órgãos como o fígado e o músculo. Células saudáveis conseguem “limpar a casa” degradando essas gorduras armazenadas, mas no diabetes esse sistema de limpeza falha. O estudo resumido aqui faz uma pergunta simples, porém poderosa: quais genes estão no cruzamento entre sobrecarga de gordura, limpeza celular defeituosa e aumento da glicemia — e poderiam tornar‑se novos sinais de alerta ou alvos de tratamento?
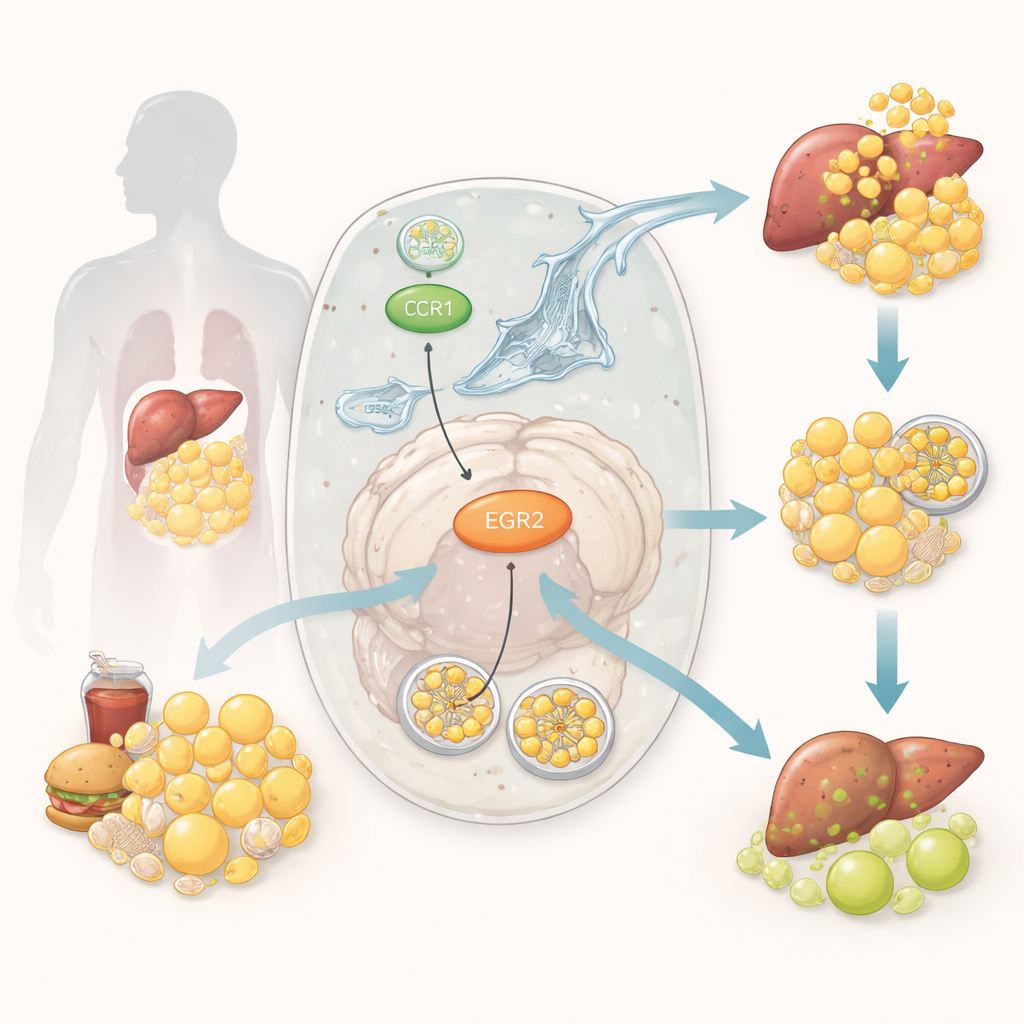
Uma equipe de limpeza celular para a gordura
Dentro de nossas células, uma via especializada de reciclagem, chamada lipofagia, ajuda a empacotar e digerir pequenas gotículas de gordura. Pense nela como um caminhão de lixo celular que coleta o excesso de gordura e o leva a um centro de descarte para que o conteúdo possa ser reutilizado com segurança. Quando a lipofagia funciona bem, as reservas de gordura permanecem equilibradas e as células respondem adequadamente à insulina. Quando fica comprometida, a gordura se acumula em tecidos como fígado e músculo, alimentando a inflamação e dificultando o trabalho da insulina. Embora os cientistas saibam que tanto o manejo defeituoso da gordura quanto a reciclagem celular alterada estão envolvidos no diabetes, os interruptores moleculares precisos que conectam esses processos têm sido pouco claros.
Caçando interruptores-chave em dados humanos
Os pesquisadores começaram garimpando grandes bancos de dados públicos de atividade gênica no sangue de pessoas com e sem diabetes. Usando ferramentas estatísticas e análise de redes, eles primeiro reduziram milhares de genes a um pequeno grupo cuja atividade mudava de forma consistente no diabetes e que já estavam ligados ao metabolismo de gorduras ou à reciclagem celular. Em seguida aplicaram vários métodos de aprendizado de máquina — técnicas que permitem aos computadores encontrar padrões robustos em dados complexos — para identificar quais genes melhor distinguiam amostras diabéticas das não diabéticas. Entre essas abordagens independentes, dois genes surgiram repetidamente como centros: CCR1 e EGR2. Ambos estavam mais ativos nas amostras diabéticas, e seus níveis de expressão tendiam a subir e descer em conjunto.
Confirmando padrões no sangue e no fígado
Para verificar se esses padrões não eram apenas peculiaridades dos conjuntos de dados originais, a equipe testou amostras de sangue novas de pessoas com e sem diabetes tipo 2. Usando um ensaio laboratorial padrão, descobriram que as proteínas CCR1 e EGR2 estavam de fato mais altas no sangue dos indivíduos com diabetes. Em seguida, recorreram a um modelo de camundongo bem estabelecido da doença que desenvolve obesidade, fígado gorduroso e hiperglicemia. Nesses animais, o fígado acumulou grandes depósitos de gordura, e marcadores da via de reciclagem celular mostraram sinais de bloqueio. Nos mesmos fígados, os níveis de CCR1 e EGR2 estavam claramente elevados, novamente ecoando as mudanças observadas no sangue humano. Em conjunto, esses achados sugerem que os dois genes estão intimamente ligados à combinação de acúmulo de gordura, reciclagem prejudicada e controle glicêmico deficiente.
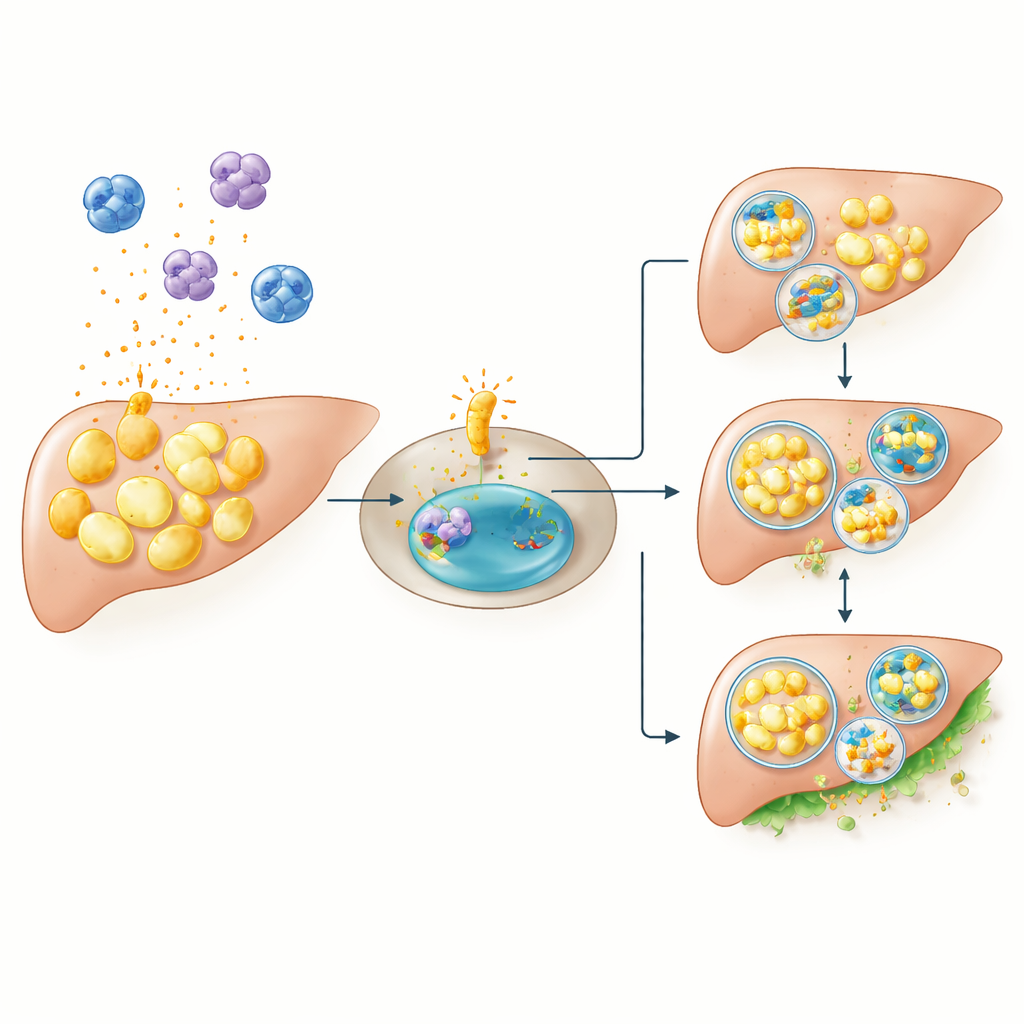
Investigando causa e efeito em camundongos
A correlação por si só não prova que esses genes impulsionam o diabetes. Para testar causalidade, os pesquisadores geraram camundongos sem CCR1 e os submeteram a uma dieta rica em gorduras, um estresse que normalmente eleva fortemente a glicemia. Como esperado, camundongos comuns na dieta rica desenvolveram níveis elevados de glicose em jejum e após as refeições. Em contraste marcante, camundongos sem CCR1 foram amplamente protegidos: sob as mesmas condições de alta gordura, sua glicemia permaneceu próxima à de animais com nulificação normalmente alimentados. Isso sugere que CCR1 não é necessário para manter o equilíbrio glicêmico cotidiano, mas torna‑se um jogador crítico quando o corpo é desafiado por excesso de gordura alimentar, provavelmente ao amplificar a inflamação e interferir na adequada eliminação de gordura dentro das células.
O que isso significa para pessoas que vivem com diabetes
Ao combinar análise de big data, medidas no sangue humano e experimentos direcionados em camundongos, este estudo destaca CCR1 e EGR2 como possíveis “botões” moleculares que ajustam como as células lidam com a gordura durante o diabetes. Níveis mais altos desses genes acompanham tecido hepático gorduroso e inflamado e sinais de que o sistema de lipofagia está entupido. Importante, a remoção de CCR1 em camundongos atenua a elevação da glicemia normalmente desencadeada por uma dieta rica em gordura, apontando para uma possível nova estratégia terapêutica. Embora ainda seja preciso muito trabalho para esclarecer exatamente como CCR1 e EGR2 controlam a reciclagem de gordura em diferentes tecidos, eles agora se destacam como biomarcadores promissores para sinalizar o diabetes mais cedo e como pontos de partida para fármacos destinados a restaurar a capacidade da célula de limpar o excesso de gordura.
Citação: Liu, J., Zhang, X., Wang, Y. et al. Identification and verification of the key genes, CCR1 and EGR2, in diabetes-associated lipophagy. Sci Rep 16, 14274 (2026). https://doi.org/10.1038/s41598-026-43737-9
Palavras-chave: diabetes tipo 2, lipofagia, fígado gorduroso, inflamação, biomarcadores