Clear Sky Science · nl
Identificatie en verificatie van de sleutelsgenen CCR1 en EGR2 bij diabetes‑geassocieerde lipofagie
Waarom vet en suiker onze cellen kunnen overweldigen
Type 2 diabetes wordt meestal beschreven als een probleem van suiker, maar vet speelt een even belangrijke en nauw verbonden rol. Wanneer ons lichaam wordt overspoeld met overtollige calorieën, hopen vetdruppels zich op in organen zoals de lever en spier. Gezonde cellen kunnen dit opruimen door opgeslagen vet af te breken, maar bij diabetes hapert dit schoonmaaksysteem. De hier samengevatte studie stelt een eenvoudige maar krachtige vraag: welke genen bevinden zich op het kruispunt tussen vetoverbelasting, foutief cellulair opruimen en stijgende bloedsuiker—en zouden ze nieuwe waarschuwingssignalen of behandelingsdoelen kunnen worden?
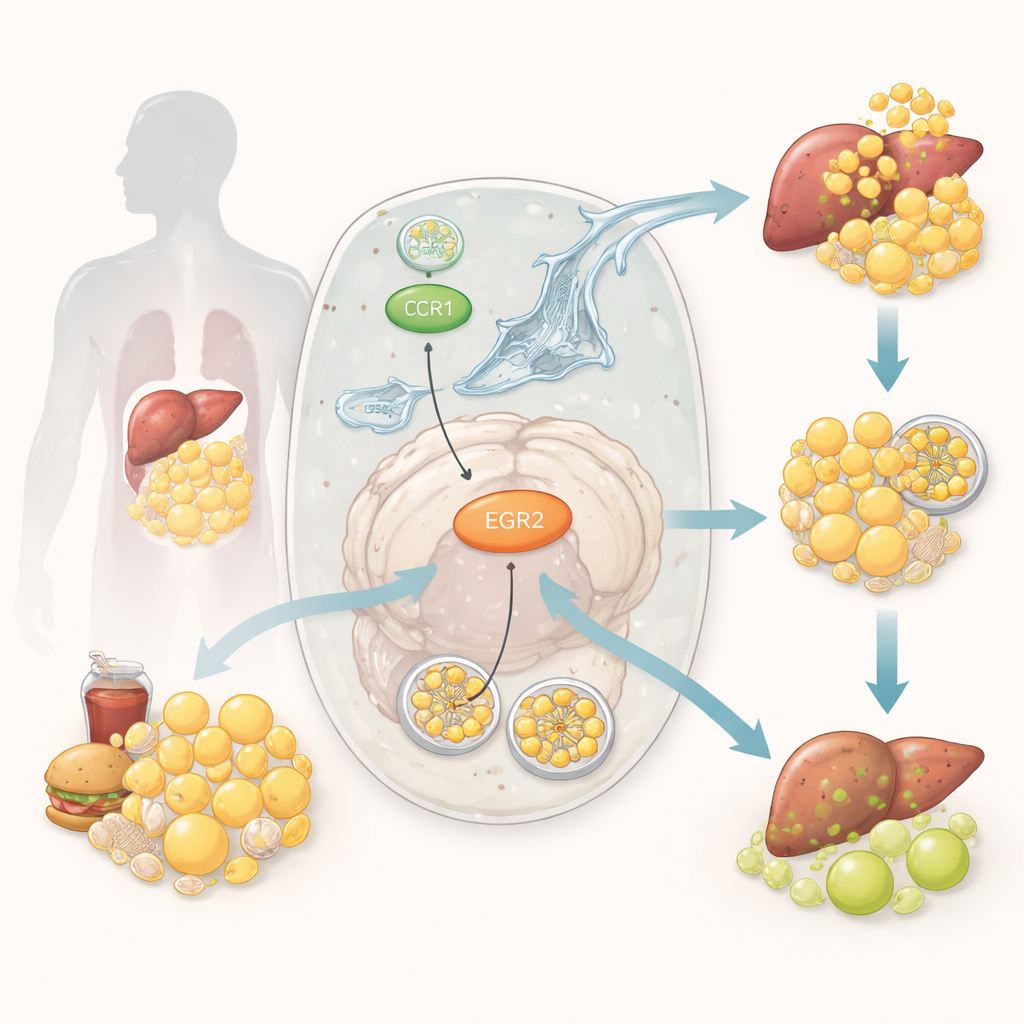
Een cellulair opruimteam voor vet
In onze cellen helpt een gespecialiseerde recycleroute, lipofagie genoemd, bij het verpakken en verteren van kleine vetdruppels. Zie het als een cellulair afvalophaaldienst die overtollig vet verzamelt en naar een verwerkingscentrum brengt zodat de inhoud veilig opnieuw gebruikt kan worden. Als lipofagie soepel verloopt, blijven vetvoorraden in balans en reageren cellen goed op insuline. Als het verstoord raakt, hoopt vet zich op in weefsels zoals lever en spier, wat ontsteking voedt en het voor insuline moeilijker maakt om zijn werk te doen. Hoewel wetenschappers weten dat zowel foutieve vetverwerking als gebrekkig cellulair recyclen bij diabetes betrokken zijn, waren de precieze moleculaire schakelaars die deze processen verbinden onduidelijk.
Op zoek naar sleutelknoppen in menselijke gegevens
De onderzoekers begonnen met het doorzoeken van grote openbare databases met genexpressiegegevens uit het bloed van mensen met en zonder diabetes. Met statistische hulpmiddelen en netwerkanalyse selecteerden ze eerst uit duizenden genen een kleine groep waarvan de activiteit consistent veranderde bij diabetes en die al gelinkt waren aan vetmetabolisme of cellulair recyclen. Vervolgens pasten ze meerdere machine‑learningmethoden toe—technieken waarmee computers robuuste patronen in complexe data kunnen vinden—om te bepalen welke genen het beste diabetische van niet‑diabetische monsters onderscheidden. Over deze onafhankelijke benaderingen heen kwamen twee genen herhaaldelijk naar voren als centrale knooppunten: CCR1 en EGR2. Beide waren in de diabetische monsters actiever en hun expressieniveaus neigden ertoe samen te stijgen en te dalen.
Patronen bevestigen in bloed en lever
Om te controleren dat deze patronen geen toevalligheden van de oorspronkelijke datasets waren, testte het team verse bloedmonsters van mensen met en zonder type 2 diabetes. Met een standaard labtest vonden ze dat zowel CCR1- als EGR2-eiwitten inderdaad hoger waren in het bloed van personen met diabetes. Vervolgens gebruikten ze een goed vastgesteld muismodel van de ziekte dat obesitas, vette lever en hoge bloedsuiker ontwikkelt. In deze dieren stapelden zich grote vetafzettingen op in de lever en vertoonden merkers van de cellulair recyclingroute tekenen van blokkade. In dezelfde lever was het niveau van CCR1 en EGR2 duidelijk verhoogd, wat opnieuw de veranderingen weerspiegelde die in menselijk bloed werden gezien. Samen suggereren deze bevindingen dat de twee genen nauw verbonden zijn met de combinatie van vetophoping, verminderde recycling en slechte suikershuishouding.
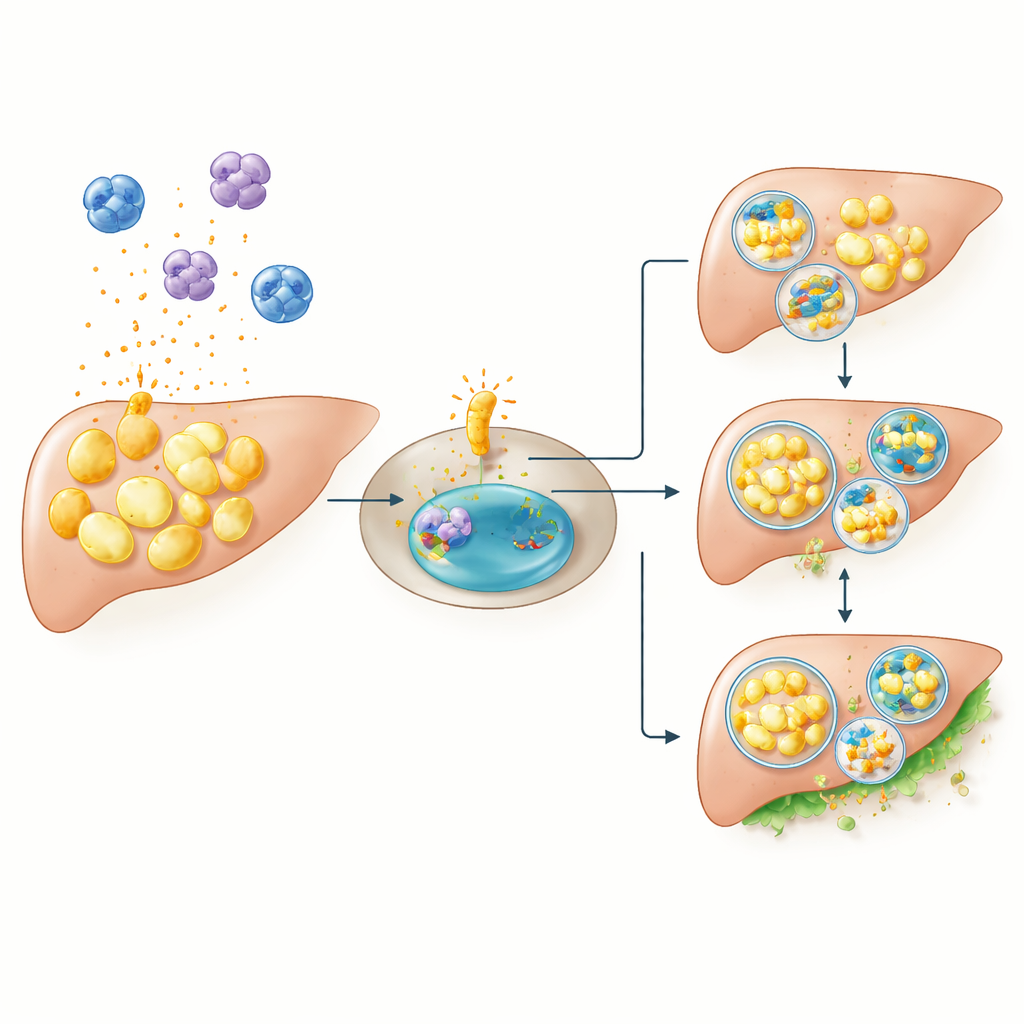
Oorzaak en gevolg onderzoeken in muizen
Correlatie alleen kan niet bewijzen dat deze genen diabetes veroorzaken. Om oorzaak en gevolg te testen, maakten de onderzoekers muizen zonder CCR1 en stelden ze die bloot aan een vetrijke voeding, een stress die normaal gesproken de bloedsuiker sterk doet stijgen. Zoals verwacht ontwikkelden gewone muizen op het rijke dieet hoge nuchtere en postprandiale glucosewaarden. In opvallend contrast waren muizen zonder CCR1 grotendeels beschermd: onder dezelfde vetrijke omstandigheden bleef hun bloedsuiker dicht bij die van normaal gevoede knock‑out dieren. Dit suggereert dat CCR1 niet nodig is voor het handhaven van de dagelijkse glucoseregulatie, maar een cruciale rol speelt wanneer het lichaam wordt uitgedaagd door overtollig dieetvet, waarschijnlijk door ontsteking te versterken en de juiste vetverwijdering binnen cellen te verstoren.
Wat dit betekent voor mensen met diabetes
Door big‑dataanalyse, metingen in menselijk bloed en gerichte muisexperimenten te combineren, belicht deze studie CCR1 en EGR2 als potentiële moleculaire "knoppen" die regelen hoe cellen met vet omgaan tijdens diabetes. Hogere niveaus van deze genen correleren met vette, ontstoken leverweefsels en met aanwijzingen dat het vetopruimende lipofagie‑systeem verstopt raakt. Belangrijk is dat het verwijderen van CCR1 bij muizen de toename van de bloedsuiker die normaal door een vetrijk dieet wordt veroorzaakt, dempt, wat wijst op een mogelijke nieuwe behandelingsstrategie. Hoewel er veel werk nodig is om precies te verduidelijken hoe CCR1 en EGR2 het vetrecyclingproces in verschillende weefsels aansturen, vallen ze nu op als veelbelovende biomarkers om diabetes eerder te signaleren en als startpunten voor geneesmiddelen die het vermogen van de cel herstellen om overtollig vet op te ruimen.
Bronvermelding: Liu, J., Zhang, X., Wang, Y. et al. Identification and verification of the key genes, CCR1 and EGR2, in diabetes-associated lipophagy. Sci Rep 16, 14274 (2026). https://doi.org/10.1038/s41598-026-43737-9
Trefwoorden: type 2 diabetes, lipofagie, vette lever, ontsteking, biomarkers