Clear Sky Science · es
Identificación y verificación de los genes clave, CCR1 y EGR2, en la lipofagia asociada a la diabetes
Por qué la grasa y el azúcar pueden desbordar nuestras células
La diabetes tipo 2 suele describirse como un problema de azúcar, pero la grasa juega un papel igualmente importante y estrechamente ligado. Cuando nuestros cuerpos están saturados de calorías en exceso, las gotitas de grasa se acumulan dentro de órganos como el hígado y el músculo. Las células sanas pueden "hacer limpieza" descomponiendo estas grasas almacenadas, pero en la diabetes este sistema de limpieza falla. El estudio resumido aquí plantea una pregunta simple pero potente: ¿qué genes se sitúan en la encrucijada entre la sobrecarga de grasa, la limpieza celular defectuosa y la subida de la glucosa en sangre, y podrían convertirse en nuevos signos de alarma o dianas terapéuticas?
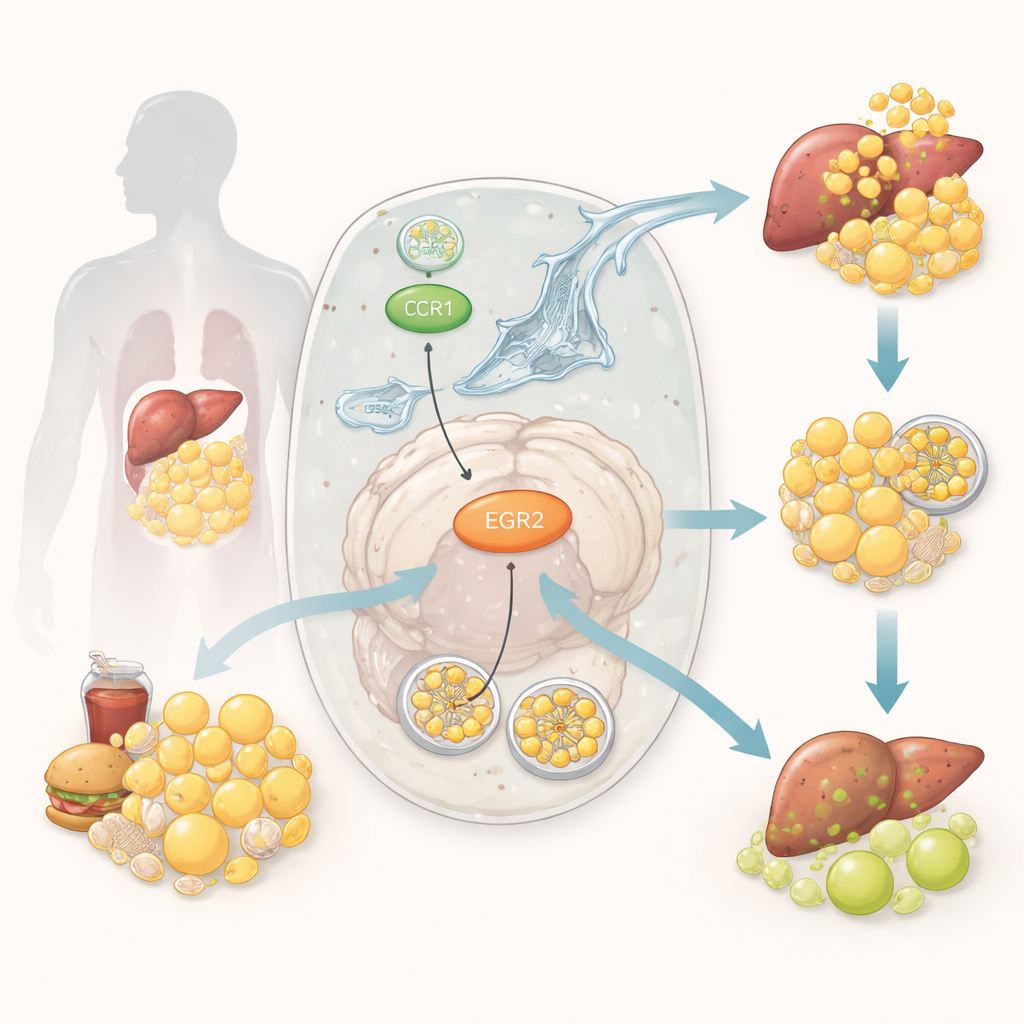
Una brigada celular de limpieza para la grasa
Dentro de nuestras células, una vía de reciclaje especializada, llamada lipofagia, ayuda a empaquetar y digerir pequeñas gotitas de grasa. Piénsalo como un camión de basura celular que recoge el exceso de grasa y lo lleva a un centro de eliminación para que el contenido pueda reutilizarse de forma segura. Cuando la lipofagia funciona bien, las reservas de grasa se mantienen en equilibrio y las células responden adecuadamente a la insulina. Cuando se altera, la grasa se acumula en tejidos como el hígado y el músculo, alimentando la inflamación y dificultando la acción de la insulina. Aunque los científicos saben que tanto el manejo defectuoso de la grasa como el reciclaje celular alterado están implicados en la diabetes, los interruptores moleculares precisos que conectan estos procesos han sido poco claros.
Buscando interruptores clave en datos humanos
Los investigadores empezaron extrayendo información de grandes bases de datos públicas de actividad génica en sangre de personas con y sin diabetes. Usando herramientas estadísticas y análisis de redes, primero redujeron miles de genes a un pequeño grupo cuya actividad cambiaba de forma consistente en la diabetes y que ya estaban vinculados al metabolismo de las grasas o al reciclaje celular. Luego aplicaron varios métodos de aprendizaje automático —técnicas que permiten a los ordenadores encontrar patrones robustos en datos complejos— para apuntar qué genes distinguían mejor las muestras diabéticas de las no diabéticas. A través de estos enfoques independientes, dos genes emergieron repetidamente como nodos centrales: CCR1 y EGR2. Ambos estaban más activos en las muestras diabéticas y sus niveles de expresión tendían a subir y bajar de forma paralela.
Confirmando patrones en sangre y hígado
Para comprobar que estos patrones no eran solo peculariedades de los conjuntos de datos originales, el equipo analizó muestras de sangre frescas de personas con y sin diabetes tipo 2. Usando un ensayo de laboratorio estándar, encontraron que las proteínas CCR1 y EGR2 eran efectivamente más altas en la sangre de individuos con diabetes. A continuación, recurrieron a un modelo murino bien establecido de la enfermedad que desarrolla obesidad, hígado graso y glucosa elevada. En estos animales, el hígado acumuló grandes depósitos de grasa y los marcadores de la vía de reciclaje celular mostraron signos de estar bloqueados. En esos mismos hígados, los niveles de CCR1 y EGR2 estaban claramente elevados, replicando los cambios observados en la sangre humana. En conjunto, estos hallazgos sugieren que los dos genes están estrechamente conectados con la combinación de acumulación de grasa, reciclaje alterado y mal control de la glucosa.
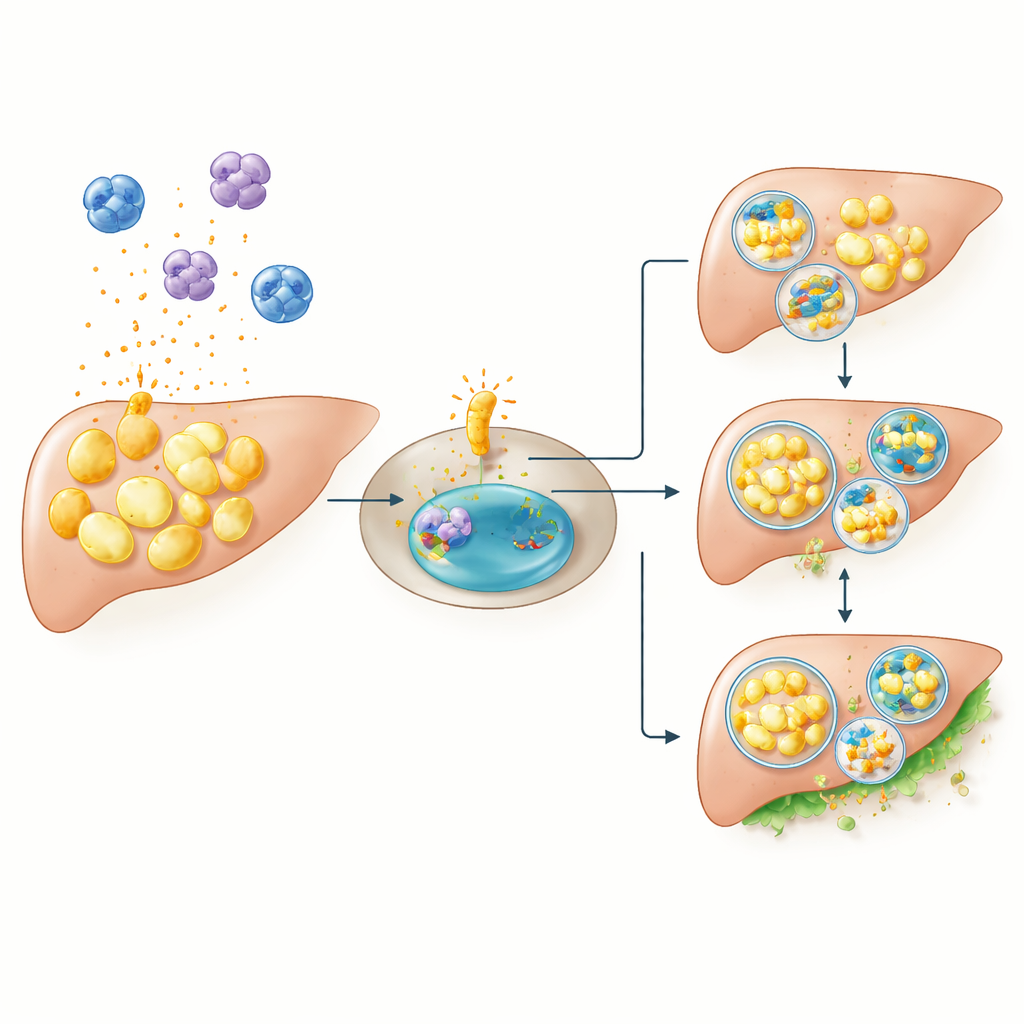
Indagando causa y efecto en ratones
La correlación por sí sola no puede probar que estos genes impulsen la diabetes. Para probar causa y efecto, los investigadores generaron ratones carecientes de CCR1 y los expusieron a una dieta alta en grasas, un estrés que normalmente eleva la glucosa en sangre de manera notable. Como era de esperar, los ratones normales con la dieta rica desarrollaron glucosa elevada en ayunas y tras las comidas. En marcado contraste, los ratones sin CCR1 estuvieron en gran medida protegidos: bajo las mismas condiciones de alta grasa, su glucosa en sangre se mantuvo cerca de la de los animales knockout alimentados normalmente. Esto sugiere que CCR1 no es necesario para mantener el equilibrio glucémico cotidiano, pero se convierte en un jugador crítico cuando el organismo se enfrenta al exceso de grasa dietética, probablemente al amplificar la inflamación e interferir con la correcta eliminación de grasa dentro de las células.
Qué implica esto para las personas con diabetes
Al combinar análisis de big data, mediciones en sangre humana y experimentos murinos dirigidos, este estudio destaca a CCR1 y EGR2 como posibles "perillas" moleculares que regulan cómo las células manejan la grasa durante la diabetes. Niveles más altos de estos genes se asocian con tejido hepático graso e inflamado y con señales de que el sistema de lipofagia está atascado. De forma importante, eliminar CCR1 en ratones atenúa el aumento de glucosa normalmente desencadenado por una dieta alta en grasas, lo que apunta a una posible nueva estrategia terapéutica. Aunque queda mucho trabajo para aclarar exactamente cómo CCR1 y EGR2 controlan el reciclaje de grasa en distintos tejidos, ahora se distinguen como biomarcadores prometedores para detectar la diabetes antes y como puntos de partida para fármacos dirigidos a restaurar la capacidad de la célula para eliminar el exceso de grasa.
Cita: Liu, J., Zhang, X., Wang, Y. et al. Identification and verification of the key genes, CCR1 and EGR2, in diabetes-associated lipophagy. Sci Rep 16, 14274 (2026). https://doi.org/10.1038/s41598-026-43737-9
Palabras clave: diabetes tipo 2, lipofagia, hígado graso, inflamación, biomarcadores