Clear Sky Science · de
Identifizierung und Validierung der Schlüsselgene CCR1 und EGR2 bei diabetes‑assoziierter Lipophagie
Warum Fett und Zucker unsere Zellen überwältigen können
Typ‑2‑Diabetes wird meist als ein Problem des Zuckers beschrieben, doch Fett spielt eine ebenso wichtige und eng verknüpfte Rolle. Wenn der Körper mit überschüssigen Kalorien überschwemmt wird, sammeln sich Fetttropfen in Organen wie Leber und Muskel an. Gesunde Zellen können „aufräumen“, indem sie diese gespeicherten Fette abbauen, doch bei Diabetes versagt dieses Reinigungs‑System. Die hier zusammengefasste Studie stellt eine einfache, aber wirkungsvolle Frage: Welche Gene stehen an der Schnittstelle zwischen Fettüberladung, gestörter zellulärer Reinigung und steigendem Blutzucker — und könnten sie neue Warnsignale oder Therapieziele werden?
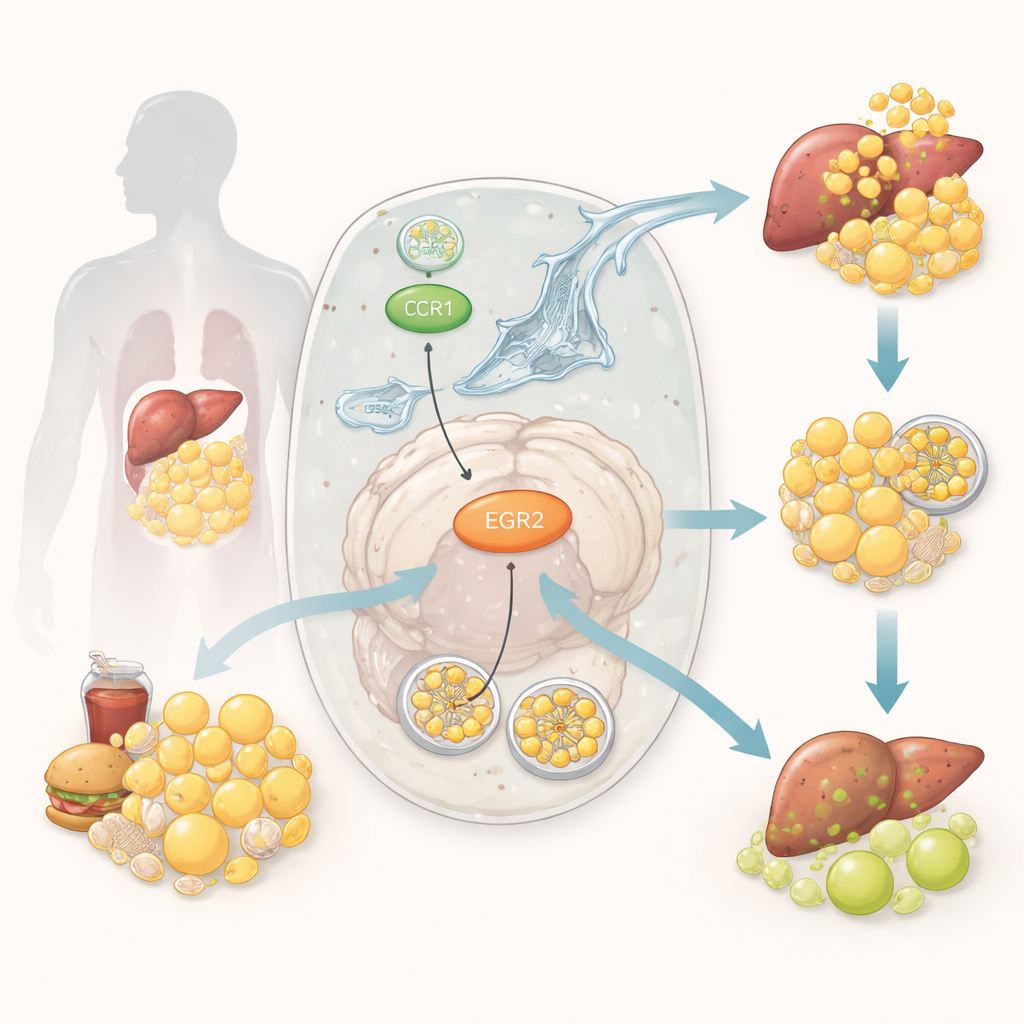
Eine zelluläre Reinigungscrew für Fett
In unseren Zellen hilft ein spezialisiertes Recycling‑System, die Lipophagie, winzige Fetttropfen zu verpacken und zu verdauen. Man kann es sich wie einen zellulären Müllwagen vorstellen, der überschüssiges Fett einsammelt und zu einer Entsorgungsstelle bringt, damit die Inhaltsstoffe sicher wiederverwendet werden können. Läuft die Lipophagie reibungslos, bleiben die Fettdepots im Gleichgewicht und die Zellen reagieren richtig auf Insulin. Ist sie gestört, häuft sich Fett in Geweben wie Leber und Muskel an, fördert Entzündungen und erschwert die Wirkung von Insulin. Zwar ist bekannt, dass sowohl fehlerhafte Fettverarbeitung als auch gestörtes zelluläres Recycling beim Diabetes eine Rolle spielen, doch die genauen molekularen Schalter, die diese Prozesse verbinden, waren bisher unklar.
Auf der Suche nach Schlüssel‑Schaltern in humanen Daten
Die Forscher begannen damit, große öffentliche Datenbanken zur Genaktivität aus dem Blut von Personen mit und ohne Diabetes zu durchforsten. Mit statistischen Werkzeugen und Netzwerkanalysen reduzierten sie zunächst Tausende von Genen auf eine kleine Gruppe, deren Aktivität sich bei Diabetes konsistent veränderte und die bereits mit Fettstoffwechsel oder zellulärem Recycling in Verbindung standen. Anschließend setzten sie mehrere Machine‑Learning‑Methoden ein — Techniken, mit denen Computer robuste Muster in komplexen Daten erkennen — um herauszufinden, welche Gene am besten zwischen diabetischen und nicht‑diabetischen Proben unterscheiden. Über diese unabhängigen Ansätze hinweg hoben sich wiederholt zwei Gene als zentrale Knoten hervor: CCR1 und EGR2. Beide waren in den diabetischen Proben stärker aktiv, und ihre Expressionsniveaus stiegen und fielen oft gemeinsam.
Bestätigung der Muster in Blut und Leber
Um zu prüfen, dass diese Muster keine Zufälligkeiten der Ausgangsdaten waren, testete das Team frische Blutproben von Personen mit und ohne Typ‑2‑Diabetes. Mit einem Standardlabortest fanden sie, dass sowohl CCR1‑ als auch EGR2‑Proteine tatsächlich im Blut von Menschen mit Diabetes erhöht waren. Danach nutzten sie ein etabliertes Mausmodell der Erkrankung, das Fettleibigkeit, Fettleber und hohen Blutzucker entwickelt. Bei diesen Tieren sammelte die Leber große Fettdepots an, und Marker des zellulären Recycling‑Systems zeigten Anzeichen einer Blockade. In denselben Lebern waren CCR1‑ und EGR2‑Spiegel deutlich erhöht, was die in menschlichem Blut beobachteten Veränderungen widerspiegelte. Zusammengenommen deuten diese Befunde darauf hin, dass die beiden Gene eng mit der Kombination aus Fettansammlung, gestörtem Recycling und schlechter Zuckerregulation verbunden sind.
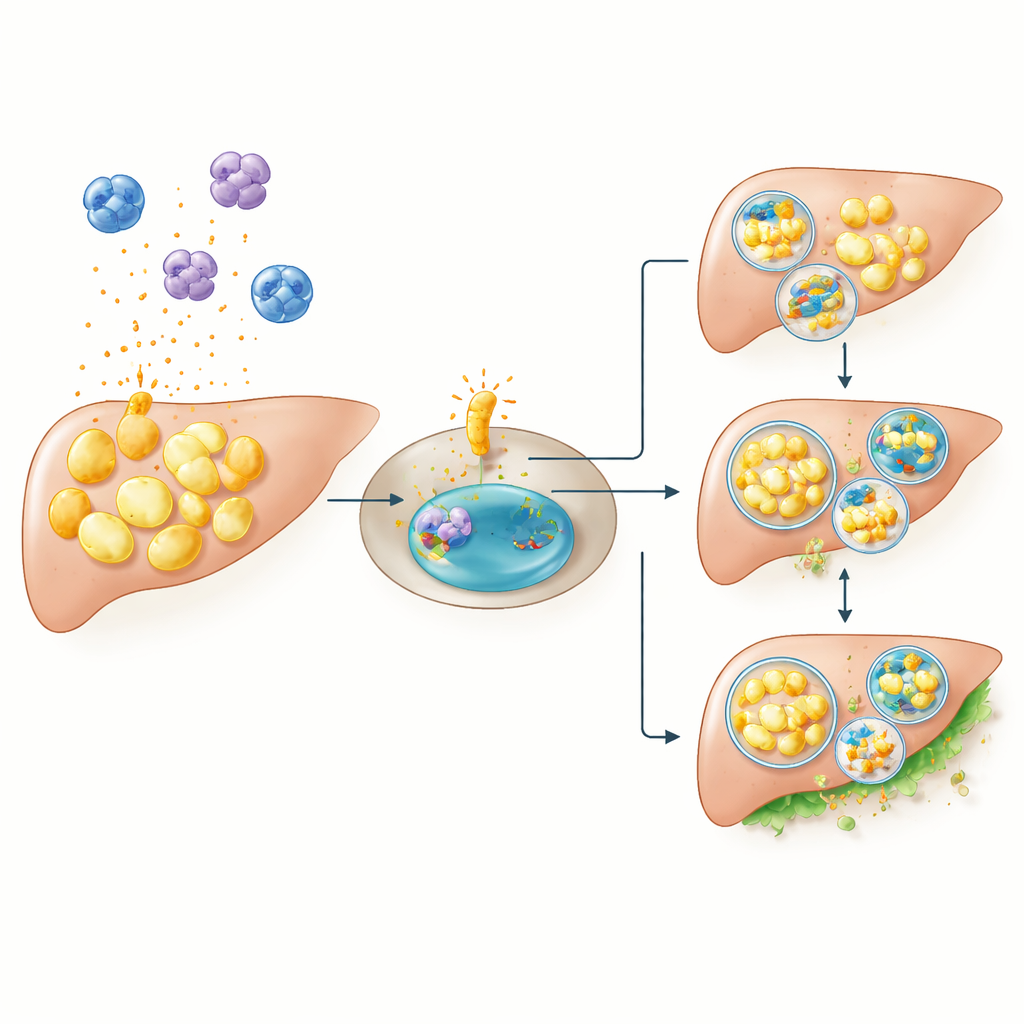
Ursache und Wirkung in Mäusen untersuchen
Korrelation allein kann nicht beweisen, dass diese Gene Diabetes vorantreiben. Um Ursache und Wirkung zu testen, erzeugten die Forscher Mäuse ohne CCR1 und setzten sie einer fettreichen Ernährung aus — einem Stressfaktor, der normalerweise den Blutzucker stark ansteigen lässt. Erwartungsgemäß entwickelten gewöhnliche Mäuse auf der fettreichen Diät hohe Nüchtern‑ und Nachmahlzeit‑Glukosewerte. Im auffälligen Gegensatz dazu waren Mäuse ohne CCR1 weitgehend geschützt: Unter denselben fettreichen Bedingungen blieben ihre Blutzuckerwerte nahe denen normal ernährter Knock‑out‑Tiere. Das deutet darauf hin, dass CCR1 nicht zum Aufrechterhalten des alltäglichen Glukosegleichgewichts erforderlich ist, wohl aber zu einem kritischen Faktor wird, wenn der Körper durch übermäßiges Nahrungsfett belastet wird — vermutlich indem es Entzündungen verstärkt und die korrekte Fettbeseitigung in Zellen stört.
Was das für Menschen mit Diabetes bedeutet
Durch die Kombination von Big‑Data‑Analyse, Messungen im menschlichen Blut und gezielten Mausversuchen hebt die Studie CCR1 und EGR2 als potenzielle molekulare „Regler“ hervor, die bestimmen, wie Zellen bei Diabetes mit Fett umgehen. Höhere Spiegel dieser Gene korrelieren mit fettiger, entzündeter Leber und mit Hinweisen darauf, dass das lipophagische System zur Fettbeseitigung verstopft ist. Wichtig ist, dass das Entfernen von CCR1 bei Mäusen den Anstieg des Blutzuckers dämpft, der normalerweise durch eine fettreiche Ernährung ausgelöst wird — ein möglicher neuer Behandlungsansatz. Obwohl noch viel Arbeit nötig ist, um genau zu klären, wie CCR1 und EGR2 das Fett‑Recycling in verschiedenen Geweben steuern, treten sie nun als vielversprechende Biomarker hervor, um Diabetes früher zu erkennen, und als Ausgangspunkte für Medikamente, die die zelluläre Fähigkeit zur Beseitigung von überschüssigem Fett wiederherstellen sollen.
Zitation: Liu, J., Zhang, X., Wang, Y. et al. Identification and verification of the key genes, CCR1 and EGR2, in diabetes-associated lipophagy. Sci Rep 16, 14274 (2026). https://doi.org/10.1038/s41598-026-43737-9
Schlüsselwörter: Typ‑2‑Diabetes, Lipophagie, Fettleber, Entzündung, Biomarker