Clear Sky Science · zh
用于乳腺超声的 AI 支持射频数据合成:定量超声组织表征的有效性
这对乳腺癌护理为何重要
乳腺癌筛查通常依赖看起来像颗粒状黑白云雾的超声图像。隐藏在这些图像背后的是丰富的原始信号,它们本可以揭示更多关于肿块是良性还是恶性的线索,但这些信号通常被丢弃,因为它们太大而难以存储。本研究探讨了人工智能是否能从普通超声图像中重建这些丢失的信号,从而在不更换临床中已有扫描仪的前提下,为更准确、可负担的乳腺癌评估打开可能性。
从简单图像到隐藏的信号细节
目前的乳腺超声检查通常使用所谓的 B 模式图像:以灰度显示组织形状和整体亮度的切片。在这些图像出现在屏幕之前,仪器首先记录原始回波信号,称为射频(RF)数据。定量超声(QUS)技术可以分析这些原始信号,以估计与组织内微小结构的大小、排列和浓度相关的属性。既有研究表明,此类定量映射有助于区分良性与恶性病变,甚至跟踪肿瘤对化疗的反应。问题在于 RF 数据体积巨大、难以存储和传输,且在商业扫描仪上常常无法获取,这使得 QUS 主要局限于研究实验室。
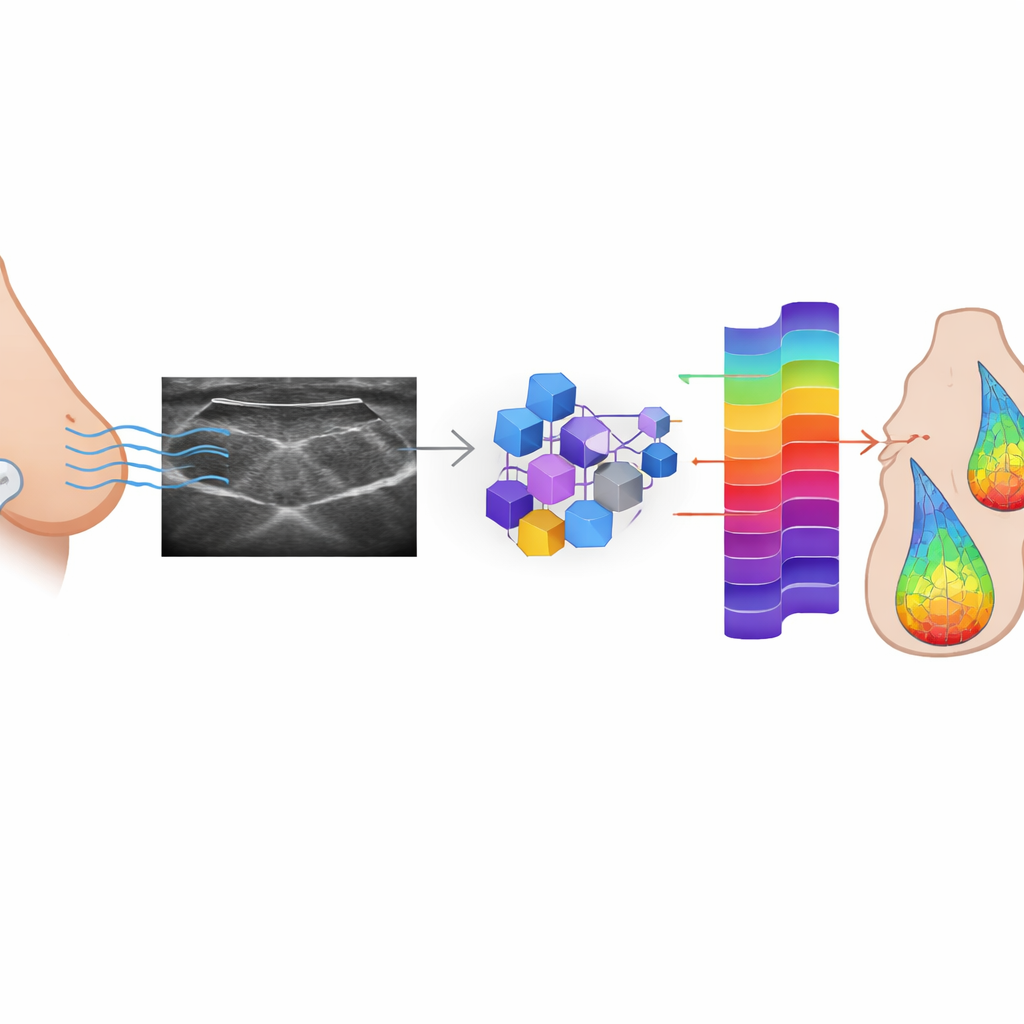
教 AI 重建丢失的信号
研究人员着手检验 AI 是否能从常规保存的 B 模式图像中学习重建 RF 数据。他们在来自 152 名存在可疑乳腺病变患者的大型配对 RF 与 B 模式帧数据集上,训练了三类条件生成对抗网络(cGAN)——一种广泛使用的 Pix2Pix 模型和两种基于视觉 Transformer 的版本(一个浅层,一个较深)。在这种对抗设置中,生成器网络试图从每个 B 模式图像生成逼真的 RF 信号,而判别器网络则学习分辨真实信号与合成信号。随着训练推进,生成器不断改进,直到其输出难以与原始信号区分。模型的调优不仅旨在欺骗判别器,还力求使每个生成的 RF 帧在数值上接近其真实对应帧。
将合成信号付诸检验
为了评估 AI 生成的 RF 数据与原始数据的匹配度,团队使用了多种图像质量评分,随后提出了一个更苛刻的问题:这些合成信号能否支持与真实 RF 数据相同的病变表征?在一个数千帧的留出测试集上,三种模型均生成了在结构上与真实信号非常相似的合成 RF,并产生了能较好保持病变形状与超声散斑外观的 B 模式重建图像。表现最强的模型——深层 Transformer cGAN——实现了最佳总体保真度。当从合成 RF 数据计算 QUS 图时,其数值和分布模式与从原始信号导出的非常相近,表明关键的组织信息被保留。
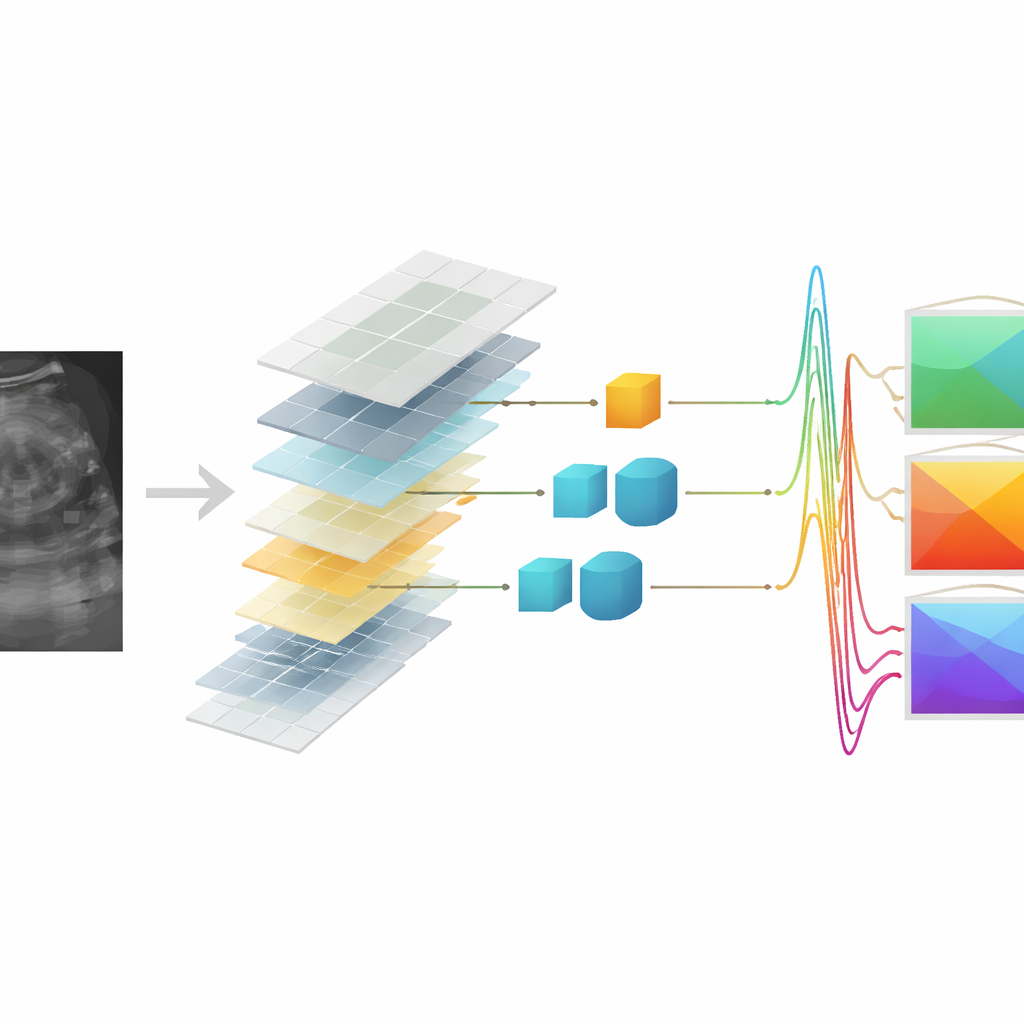
合成数据还能识别癌症吗?
决定性测试是这些基于合成的 QUS 图能否帮助区分良性与恶性乳腺病变。作者构建了一个分类流程,先选出最有信息量的 QUS 特征,然后训练支持向量机将两类分开。仅使用来自真实 RF 数据的特征时,系统对病变的正确分类率约为 82%。值得注意的是,当完全基于来自合成 RF 的 QUS 特征进行训练和测试时,深层 Transformer 和 Pix2Pix 模型的准确率约为 81%,在统计变异范围内基本与原始性能相当。在某些情形下,当用合成特征测试一个在真实数据特征上训练的分类器时,深层 Transformer 模型甚至略微超越了基线,凸显了所学映射的稳健性。
展望更智能的扫描
这项工作表明,AI 可以有效地从标准图像“填补”缺失的原始超声信号,同时保留有助于区分良性与恶性乳腺病变的关键定量线索。从实际角度看,未来医院或能直接从常规 B 模式数据运行 QUS 分析,而无需在每台扫描仪上记录或存储庞大的 RF 数据集。该研究是一个早期概念验证,限于一种类型的超声系统并专注于乳腺病变,但它指向了一个未来:现有超声设备可通过软件增强,提供更深层、更客观的组织健康洞见——有望在不增加硬件或侵入性程序的情况下改进癌症诊断和治疗决策。
引用: Sheibani-Asl, N., Osapoetra, L.O., Czarnota, G.J. et al. AI-enabled RF data synthesis for breast ultrasound: efficacy in quantitative ultrasound tissue characterization. Sci Rep 16, 12544 (2026). https://doi.org/10.1038/s41598-026-43319-9
关键词: 乳腺超声, 人工智能, 定量超声, 医学图像合成, 癌症诊断