Clear Sky Science · ru
Синтез RF-данных с помощью ИИ для маммографического УЗИ: эффективность в количественной УЗ-характеризации тканей
Почему это важно для ухода при раке молочной железы
Скрининг рака молочной железы часто опирается на УЗ-изображения, похожие на зернистые черно‑белые облака. За этими изображениями скрываются богатые сырые сигналы, которые могли бы рассказать гораздо больше о том, доброкачественное ли образование или опасно, однако такие сигналы обычно удаляются, потому что они слишком объёмны для хранения. В этом исследовании проверяется, может ли искусственный интеллект воссоздавать потерянные сигналы по обычным УЗ-картинкам, что откроет путь к более точной и доступной оценке рака молочной железы без замены сканеров, уже используемых в клиниках.
От обычных картинок к скрытым деталям сигнала
Современные обследования молочной железы обычно используют так называемые B‑режимные изображения: градации серого, показывающие форму и общую яркость тканей. Прежде чем эти изображения появятся на экране, аппарат сначала записывает сырые эхо‑сигналы, известные как радиочастотные (RF) данные. Методы количественного ультразвука (QUS) анализируют эти сырые сигналы, чтобы оценить параметры, связанные с размером, расположением и концентрацией мелких структур в ткани. Предыдущие исследования показали, что такие количественные карты помогают отличать доброкачественные образования от злокачественных и даже отслеживать ответ опухолей на химиотерапию. Проблема в том, что RF-данные очень объёмны, их трудно хранить и передавать, и они часто недоступны на коммерческих сканерах, что ограничивало применение QUS в основном лабораторными исследованиями.
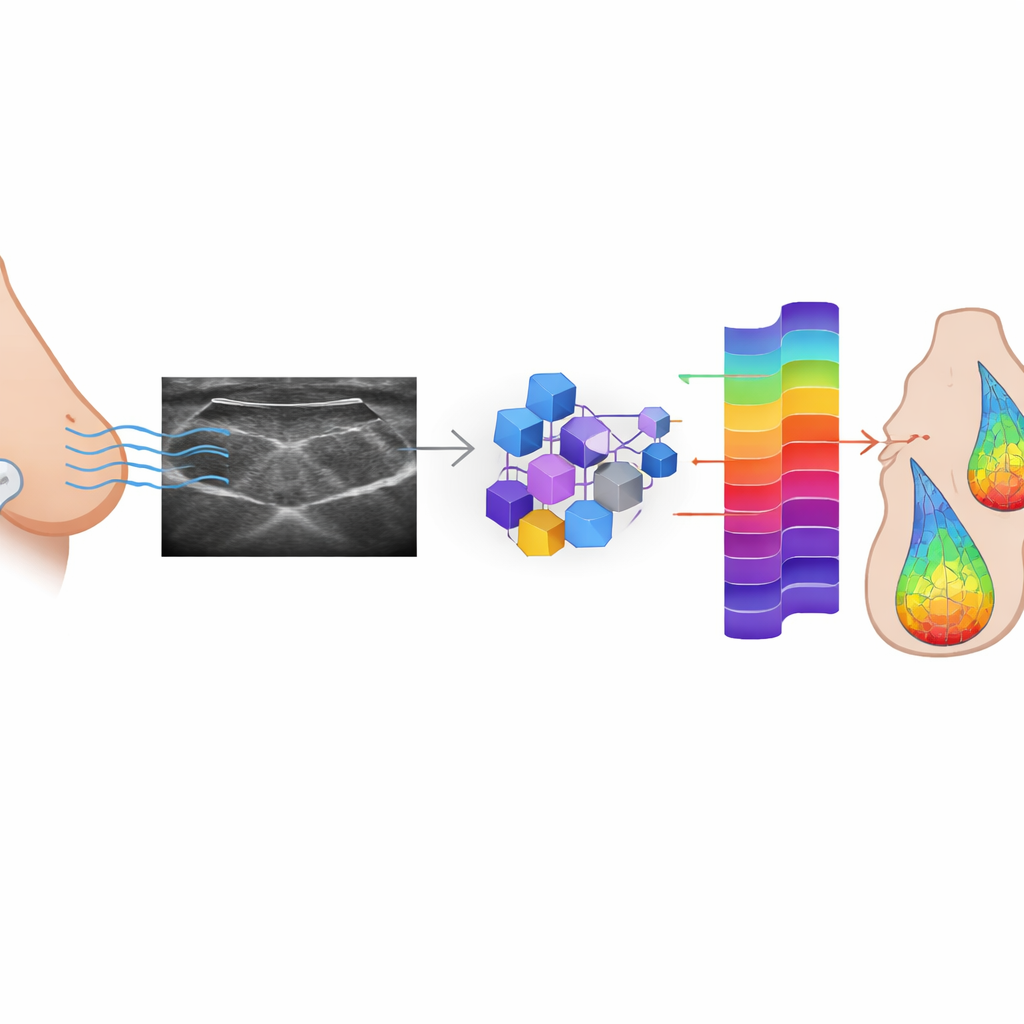
Обучение ИИ восстанавливать утерянные сигналы
Исследователи проверяли, сможет ли ИИ научиться реконструировать RF-данные по B‑режимным изображениям, которые рутинно сохраняются. Они обучили три типа условных генеративных состязательных сетей (cGAN): широко используемую модель Pix2Pix и две версии на базе визуальных трансформеров (один мелкой, другой глубже) на большой выборке парных RF- и B‑режимных кадров от 152 пациентов с подозрительными очагами в молочной железе. В этой состязательной схеме генератор пытается создать реалистичные RF-сигналы из каждого B‑режимного изображения, а дискриминатор учится отличать реальные сигналы от синтетических. Со временем генератор улучшается до тех пор, пока его выходы не становятся трудноотличимыми от оригиналов. Модели настраивали не только на то, чтобы обманывать дискриминатор, но и на то, чтобы каждое сгенерированное RF-кадровое представление было численно близко к своему истинному аналогу.
Проверка синтетических сигналов на практике
Чтобы оценить, насколько хорошо синтезированные ИИ RF-данные соответствуют оригиналам, команда использовала несколько метрик качества изображения и затем задала более жесткий вопрос: могут ли синтезированные сигналы поддерживать ту же характеристику очагов, что и реальные RF-данные? На отложенной тестовой выборке из тысяч кадров все три модели сгенерировали RF, структурно очень похожие на реальные сигналы, и привели к реконструкциям B‑режима, которые точно сохраняли форму очагов и зернистую (speckle) структуру УЗ-изображения. Наиболее сильная модель — глубокий трансформерный cGAN — показала наилучшую общую достоверность. Когда из синтетических RF вычисляли QUS‑карты, их численные значения и распределения сильно напоминали те, что получены из оригинальных сигналов, что указывает на сохранение ключевой информации о ткани.
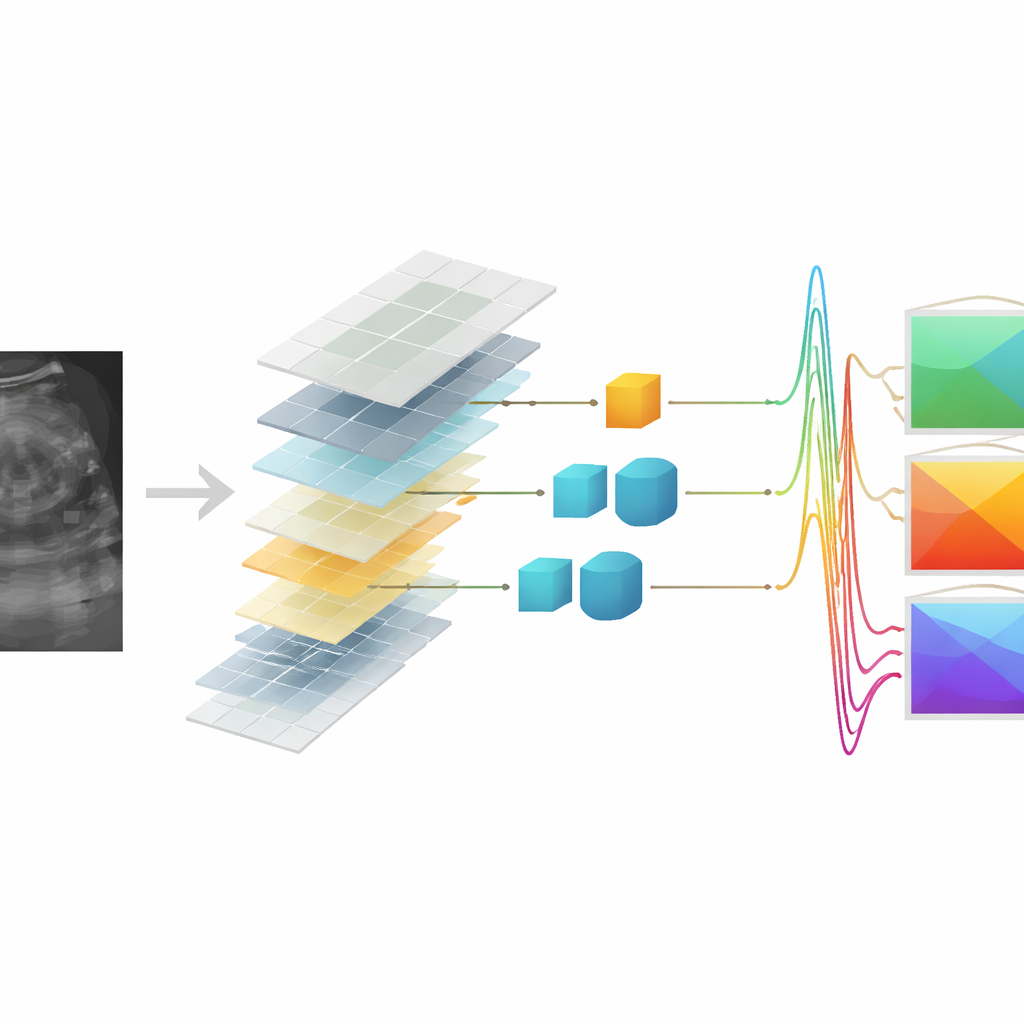
Могут ли синтетические данные выявлять рак?
Решающим испытанием было то, смогут ли QUS‑карты, полученные из синтетических данных, отличать доброкачественные очаги от злокачественных. Авторы построили классификационный конвейер, который сначала выбирал наиболее информативные QUS‑признаки, а затем обучал метод опорных векторов для разделения двух групп. Используя только признаки из реальных RF-данных, система правильно классифицировала очаги примерно с 82% точностью. Удивительно, но при обучении и тестировании исключительно на QUS‑признаках, полученных из синтетического RF, модели глубокого трансформера и Pix2Pix достигли примерно 81% точности, практически соответствуя исходной производительности в пределах статистической изменчивости. В некоторых сценариях модель глубокого трансформера даже немного превзошла базу, когда синтетические признаки использовали для тестирования классификатора, обученного на признаках из реальных данных, что подчёркивает устойчивость выученного отображения.
Взгляд в будущее умных обследований
Эта работа показывает, что ИИ может эффективно «заполнять» недостающие сырые ультразвуковые сигналы по стандартным изображениям при сохранении ключевых количественных признаков, которые помогают отличать безвредные очаги от опасных. Практически это означает, что однажды больница сможет запускать QUS‑анализ непосредственно по рутинным B‑режимным данным, не требуя записи или хранения массивных RF‑наборов на каждом сканере. Исследование является ранним доказательством концепции, ограничено одним типом ультразвуковой системы и сфокусировано на очагах молочной железы, но указывает на будущее, в котором существующие ультразвуковые аппараты можно улучшить с помощью программного обеспечения для получения более глубокого и объективного понимания состояния ткани — что потенциально повысит точность диагностики рака и принятия решений о лечении без добавления нового оборудования или инвазивных процедур.
Цитирование: Sheibani-Asl, N., Osapoetra, L.O., Czarnota, G.J. et al. AI-enabled RF data synthesis for breast ultrasound: efficacy in quantitative ultrasound tissue characterization. Sci Rep 16, 12544 (2026). https://doi.org/10.1038/s41598-026-43319-9
Ключевые слова: ультразвуковое исследование молочной железы, искусственный интеллект, количественное ультразвуковое исследование, синтез медицинских изображений, диагностика рака