Clear Sky Science · it
Sintesi di dati RF abilitata dall’IA per l’ecografia mammaria: efficacia nella caratterizzazione quantitativa del tessuto tramite ultrasuoni
Perché questo è importante per la cura del cancro al seno
Lo screening per il cancro al seno si basa spesso su immagini ecografiche che sembrano nuvole granulose in bianco e nero. Dietro a quelle immagini si nascondono segnali grezzi ricchi di informazioni che potrebbero rivelare molto di più sul fatto che una massa sia benigna o pericolosa, ma questi segnali vengono di solito scartati perché troppo ingombranti da conservare. Questo studio esplora se l’intelligenza artificiale possa ricreare quei segnali perduti a partire dalle normali immagini ecografiche, aprendo la strada a valutazioni del cancro al seno più accurate e accessibili senza modificare gli scanner già in uso nelle cliniche.
Dalle immagini semplici ai dettagli del segnale nascosto
Gli esami ecografici al seno di oggi tipicamente usano le cosiddette immagini in modalità B: sezioni in scala di grigi che mostrano la forma e la luminosità complessiva dei tessuti. Prima che queste immagini compaiano sullo schermo, la macchina registra i segnali di eco grezzi, noti come dati a radiofrequenza (RF). Le tecniche di ecografia quantitativa (QUS) possono analizzare questi segnali grezzi per stimare proprietà legate alla dimensione, disposizione e concentrazione di piccole strutture all’interno del tessuto. Ricerche precedenti hanno mostrato che tali mappe quantitative possono aiutare a distinguere lesioni benigne da maligne e persino a monitorare la risposta dei tumori alla chemioterapia. Il problema è che i dati RF sono enormi, difficili da conservare e trasmettere, e spesso inaccessibili sugli scanner commerciali, cosa che ha confinato la QUS principalmente ai laboratori di ricerca.
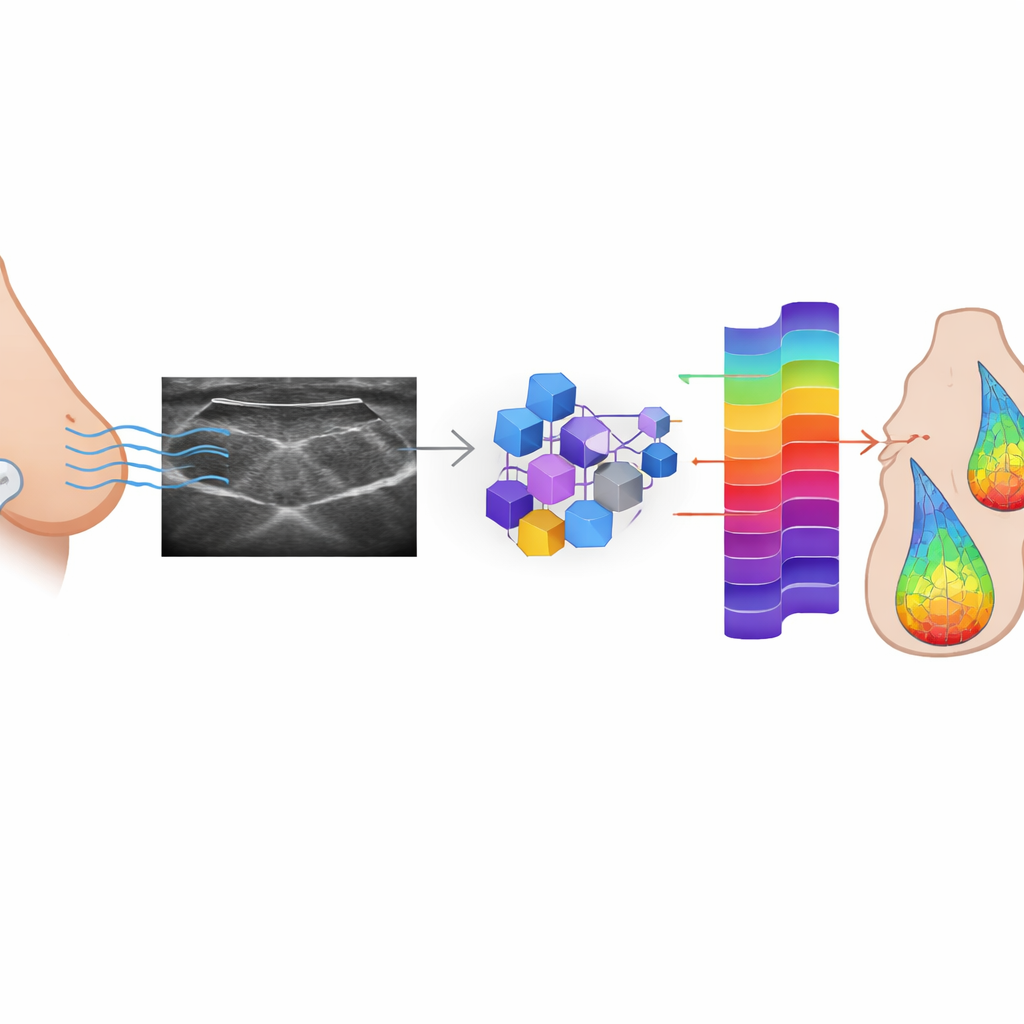
Insegnare all’IA a ricostruire i segnali perduti
I ricercatori hanno cercato di verificare se l’IA potesse apprendere a ricostruire i dati RF a partire dalle immagini in modalità B che vengono salvate di routine. Hanno addestrato tre tipi di reti generative antagoniste condizionate (cGAN)—un modello Pix2Pix ampiamente utilizzato e due versioni basate su vision transformer (una superficiale, una più profonda)—su un ampio dataset di frame RF e B‑mode accoppiati provenienti da 152 pazienti con lesioni mammarie sospette. In questo schema antagonista, una rete generatrice cerca di creare segnali RF realistici a partire da ogni immagine B‑mode, mentre una rete discriminatrice impara a distinguere segnali reali da sintetici. Col tempo, il generatore migliora finché i suoi output diventano difficili da distinguere dagli originali. I modelli sono stati ottimizzati non solo per ingannare il discriminatore ma anche per mantenere ogni frame RF generato numericamente vicino al suo corrispondente reale.
Mettere alla prova i segnali sintetici
Per valutare quanto i dati RF generati dall’IA corrispondessero agli originali, il team ha utilizzato diversi punteggi di qualità dell’immagine e ha poi posto una domanda più difficile: i segnali sintetici possono supportare lo stesso tipo di caratterizzazione delle lesioni dei dati RF reali? Su un set di test escluso dall’addestramento composto da migliaia di frame, tutti e tre i modelli hanno prodotto RF sintetiche strutturalmente molto simili ai segnali reali e hanno portato a ricostruzioni in B‑mode che preservavano da vicino la forma delle lesioni e l’aspetto puntinato tipico dell’ecografia. Il modello più potente, il cGAN con transformer profondo, ha ottenuto la migliore fedeltà complessiva. Quando sono state calcolate mappe QUS dai RF sintetici, i loro valori numerici e i pattern di distribuzione somigliavano fortemente a quelli derivati dai segnali originali, suggerendo che le informazioni tessutali chiave erano state mantenute.
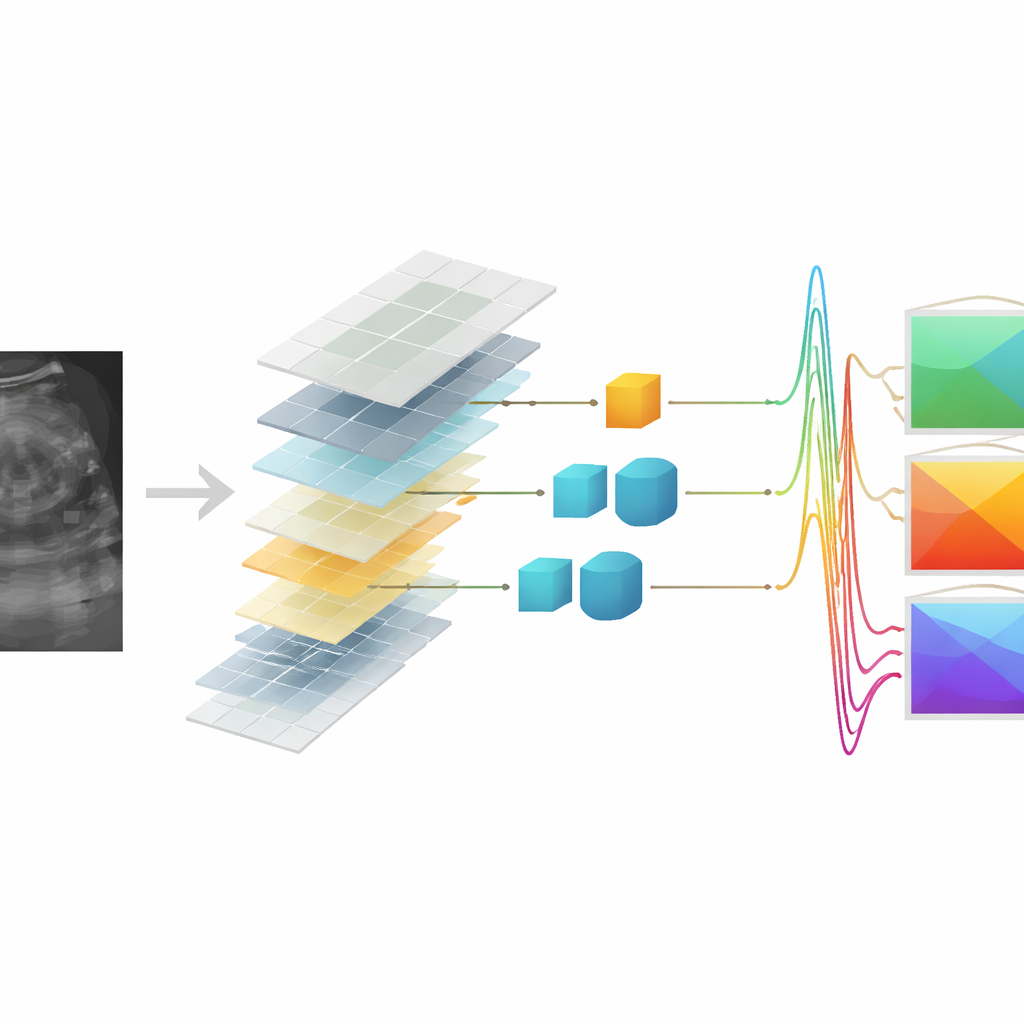
I dati sintetici possono ancora individuare il cancro?
La prova decisiva era se queste mappe QUS basate su dati sintetici potessero aiutare a distinguere lesioni mammarie benigne da maligne. Gli autori hanno costruito una pipeline di classificazione che prima selezionava le caratteristiche QUS più informative e poi addestrava una macchina a vettori di supporto per separare i due gruppi. Usando soltanto caratteristiche ricavate da dati RF reali, il sistema ha classificato correttamente le lesioni con circa l’82% di accuratezza. Sorprendentemente, quando addestrati e testati esclusivamente su caratteristiche QUS derivate da RF sintetici, i modelli deep transformer e Pix2Pix hanno raggiunto circa l’81% di accuratezza, eguagliando sostanzialmente le prestazioni originali entro la variazione statistica. In alcuni scenari il modello deep transformer ha addirittura superato leggermente il baseline quando le caratteristiche sintetiche sono state usate per testare un classificatore addestrato su caratteristiche reali, sottolineando la robustezza della mappatura appresa.
Prospettive per ecografie più intelligenti
Questo lavoro dimostra che l’IA può efficacemente “colmare” i segnali grezzi mancanti dell’ecografia standard preservando i principali indicatori quantitativi che aiutano a separare lesioni mammarie innocue da quelle pericolose. In termini pratici, un ospedale potrebbe un giorno eseguire analisi QUS direttamente da dati B‑mode di routine, senza la necessità di registrare o archiviare enormi dataset RF su ogni scanner. Lo studio è una prova di principio iniziale, limitata a un tipo di sistema ecografico e focalizzata sulle lesioni mammarie, ma indica un futuro in cui le macchine ecografiche esistenti possono essere potenziate via software per offrire un’analisi più profonda e oggettiva della salute dei tessuti—potenzialmente migliorando la diagnosi e le decisioni terapeutiche sul cancro senza aggiungere nuovo hardware o procedure invasive.
Citazione: Sheibani-Asl, N., Osapoetra, L.O., Czarnota, G.J. et al. AI-enabled RF data synthesis for breast ultrasound: efficacy in quantitative ultrasound tissue characterization. Sci Rep 16, 12544 (2026). https://doi.org/10.1038/s41598-026-43319-9
Parole chiave: ecografia mammaria, intelligenza artificiale, ecografia quantitativa, sintesi di immagini mediche, diagnosi del cancro