Clear Sky Science · zh
IL-8通过中性粒细胞与间皮细胞的相互作用促成术后粘连形成
为什么术后瘢痕带很重要
许多接受腹部手术的人随后会出现称为粘连的内部瘢痕带,这些瘢痕带可能扭曲肠道、引起慢性疼痛或影响生育能力。尽管影响甚远,医生可供选择的可靠预防方法仍然很少。本研究探讨了一种强有力的免疫信号IL-8,并阐明它如何推动从干净的外科切口到顽固内瘢痕组织的早期连锁反应——以及用抗体阻断IL-8如何在灵长类动物模型中显著减少这些粘连。
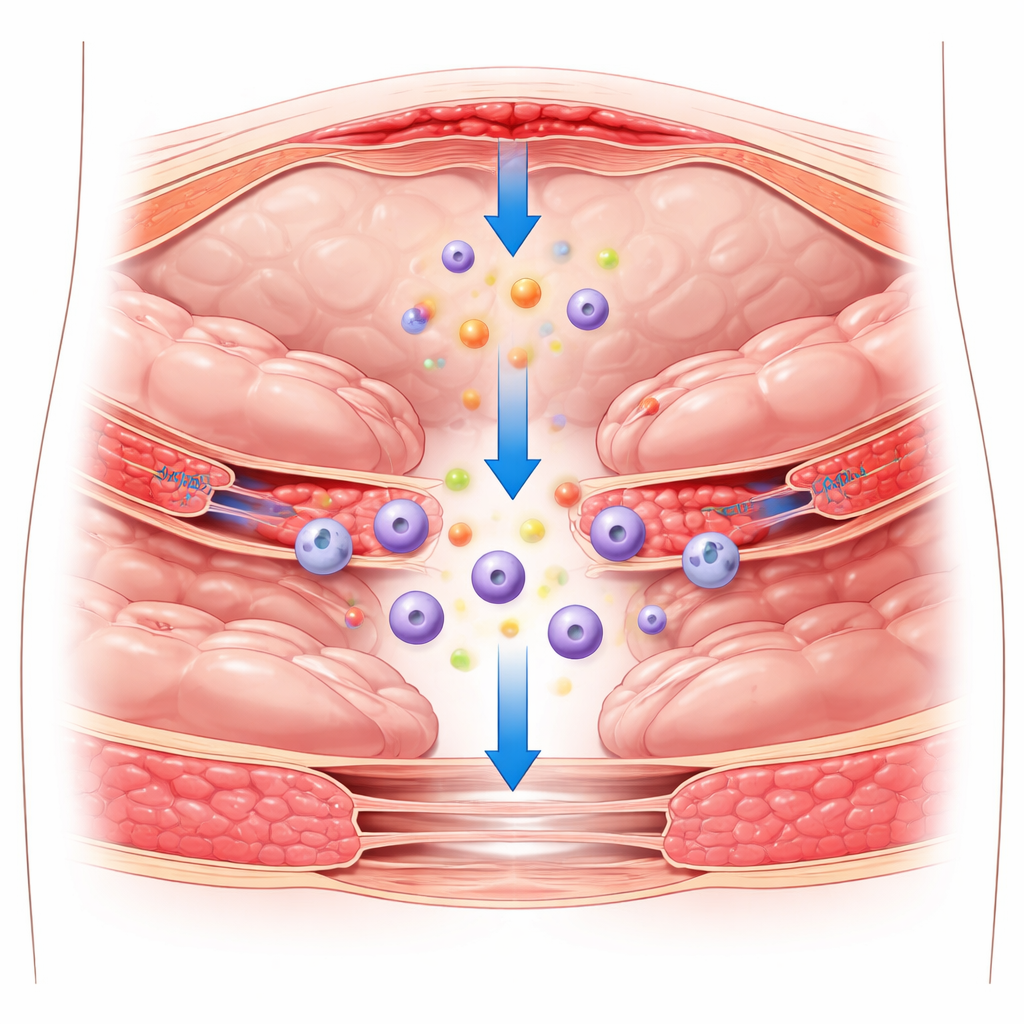
手术留下的隐形瘢痕
腹部手术后,覆盖器官和腹壁的光滑衬里可能受损。正常情况下,这层由称为间皮细胞的薄层细胞组成的衬里,能让器官相互滑动而不粘连。受伤时,它会以炎症作出反应:免疫细胞涌入、凝血通路启动,形成称为纤维蛋白的暂时蛋白网。如果这种早期反应没有被严格控制,纤维蛋白可能成为永久纤维带的骨架,将器官绑在一起,形成术后粘连。现有的预防方法主要使用物理薄膜或凝胶将组织分隔开,但这些屏障效果有限,问题仍未得到解决。
召唤“先行者”的关键信号
研究者将注意力集中在IL-8上,这是一种在组织受伤时迅速升高并已知能吸引中性粒细胞的化学信号,中性粒细胞是机体的主要“先行者”白细胞之一。与没有IL-8基因的小鼠不同,人类和绒毛猕猴(短尾猕猴)具有该基因,使这些猴子成为研究人类的有用替代模型。在有人细胞的体外实验中,IL-8激活了中性粒细胞上的两种主要受体,并比仅使用一种受体的相关趋化因子CXCL1更强烈地吸引这些细胞。这种更强的牵引力表明,IL-8是将中性粒细胞带入手术部位的主导开关,尽管它们有助于对抗危险,但也为过度瘢痕化奠定基础。
衬里细胞与免疫细胞之间的恶性循环
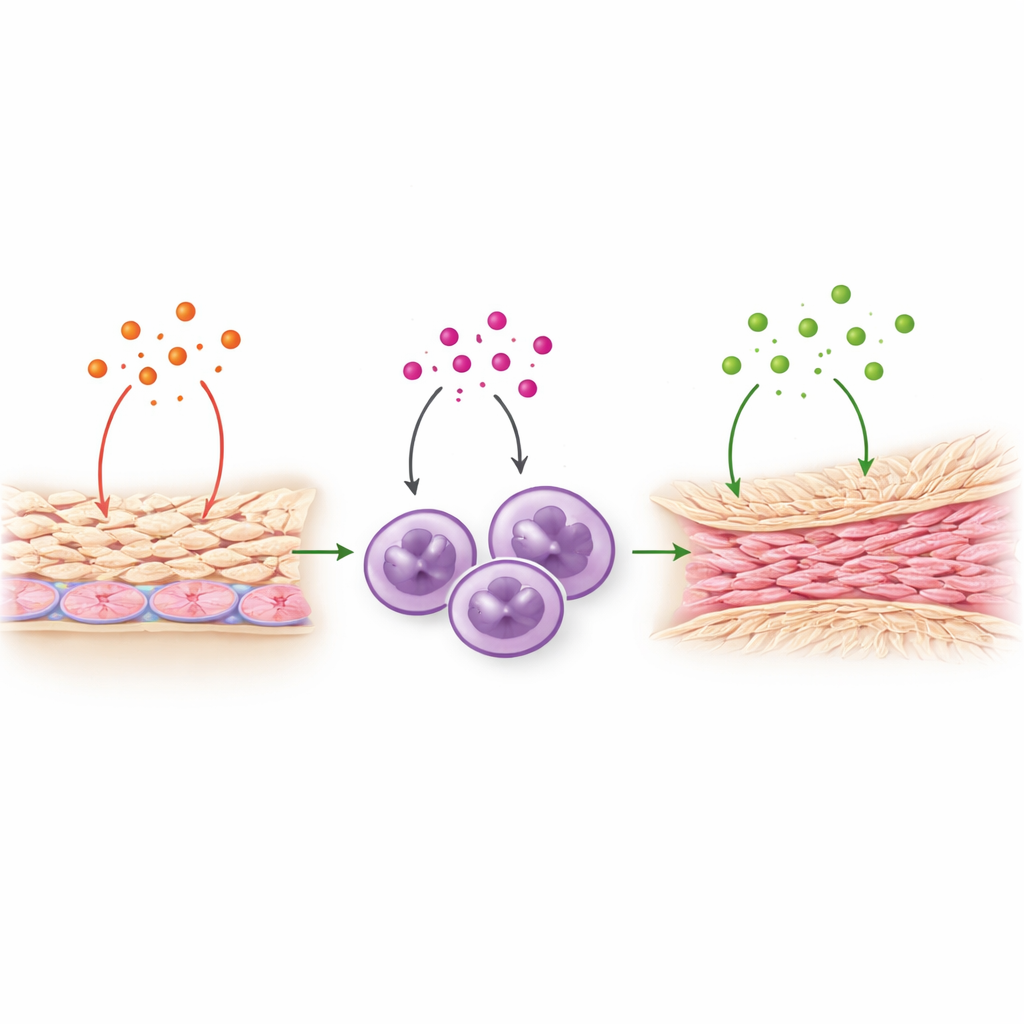
IL-8的作用不仅仅是召集中性粒细胞。团队证明IL-8还能直接作用于腹腔内的间皮细胞。间皮细胞暴露于IL-8后释放出更多的TNF‑α,这是另一种强效炎症信号,已被卷入粘连形成的过程。反过来,TNF‑α促使间皮细胞产生更多IL-8,形成自我增强的环路。TNF‑α还刺激中性粒细胞增加TGF‑β1的产生,TGF‑β1是纤维化的主控因子,促使组织沉积持久的胶原纤维。总体上,这些步骤描绘出一条传导路线:IL-8 → 间皮细胞激活并释放TNF‑α → 中性粒细胞激活并释放TGF‑β1 → 纤维瘢痕组织的堆积。重要的是,IL-8本身并不直接开启纤维化基因,但它放大了那些直接作用的信号。
在猴子体内测试IL-8抑制剂
为了观察这一通路在有生命机体中的表现,科学家使用了对腹部和子宫实施标准化损伤以诱发粘连的绒毛猕猴。受伤腹壁中的IL-8水平在手术后6小时内飙升,并在一周内趋向基线,标志着IL-8最为活跃的狭窄早期窗口。研究组随后在部分猴子手术前两天静脉给予一次AMY109,这是一种中和IL-8的长效抗体。26天后用腹腔镜检查时,接受AMY109的动物腹壁上的粘连明显更小且更少。子宫上的粘连也趋于轻微,在两只接受治疗的猴子中甚至完全缺失,这表明抑制IL-8能够在不明显损害正常伤口愈合的情况下保护腹腔内的多个部位。
这对患者意味着什么
综合来看,这些发现将IL-8定位为腹部手术后早期炎症与后期纤维化的核心组织者。通过强烈招募中性粒细胞并与间皮细胞形成反馈环,增强TNF‑α和TGF‑β1,IL-8将短暂的愈合反应转变为顽固的内部瘢痕带。在猴子中用像AMY109这样的抗体阻断IL-8能显著减少这些粘连,提出了一种可能的新药策略,针对生物学过程而不仅仅依赖物理屏障。如果在人类中得到类似证实,患者未来可能在围手术期接受短程IL-8阻断治疗,从而降低发生疼痛且可能改变生活的术后粘连的风险。
引用: Nakagawa, K., Tanimura, H., Yamazaki, M. et al. IL-8 contributes to postoperative adhesion formation through the crosstalk of neutrophils and mesothelial cells. Sci Rep 16, 14221 (2026). https://doi.org/10.1038/s41598-026-42159-x
关键词: 术后粘连, 白细胞介素-8, 中性粒细胞, 纤维化, 猕猴模型