Clear Sky Science · ru
IL-8 способствует образованию послеоперационных спаек через взаимодействие нейтрофилов и мезотелиальных клеток
Почему послеоперационные рубцовые тяжи имеют значение
У многих людей после абдоминальных операций развиваются внутренние рубцовые тяжи — спайки, которые могут перекручивать кишечник, вызывать хроническую боль или мешать фертильности. Несмотря на их влияние, у врачей мало надёжных способов предотвратить образование этих липких тяжей. В этом исследовании изучается мощный иммунный сигнал IL-8 и показано, как он запускает раннюю цепочку событий, переводящую чистый хирургический разрез в плотную внутреннюю рубцовую ткань — и как блокирование IL-8 антителом может существенно уменьшить эти спайки в приматной модели.
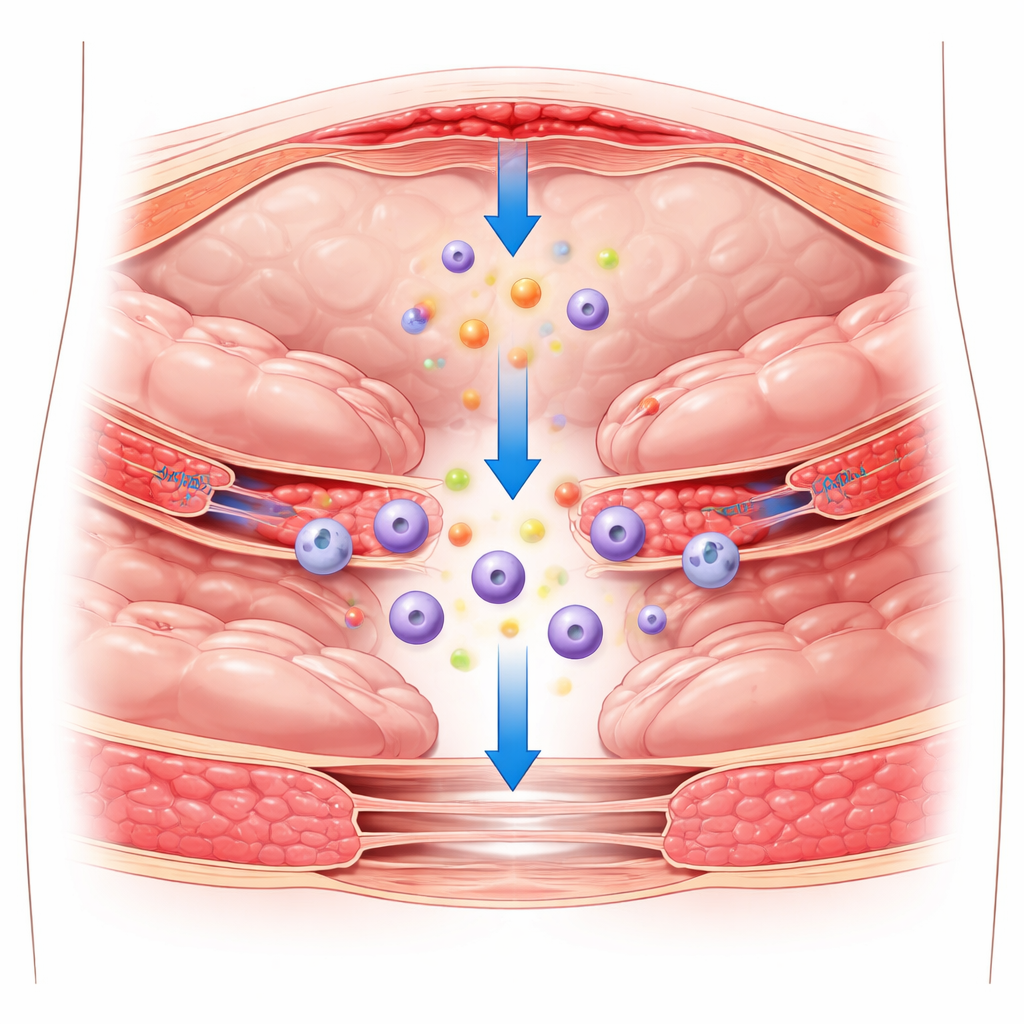
Скрытые рубцы, оставшиеся после операции
После вмешательства в брюшной полости повреждается гладкая оболочка, покрывающая органы и стенку живота. Обычно эта оболочка, состоящая из тонкого слоя клеток — мезотелиальных клеток, обеспечивает скольжение органов друг относительно друга без прилипания. При повреждении она отвечает воспалением: в очаг поступают иммунные клетки, включаются пути свертывания крови, и образуется временная белковая сеть — фибрин. Если эта начальная реакция плохо контролируется, фибрин может стать основой для постоянных волокнистых тяжей, которые связывают органы между собой, образуя послеоперационные спайки. Существующие методы профилактики в основном используют физические плёнки или гели, чтобы держать ткани разъединёнными, но эти барьеры работают лишь частично и не устраняют проблему полностью.
Ключевой сигнал, призывающий первоотклик
Исследователи сосредоточились на IL-8 — химическом сигнале, который быстро повышается при повреждении ткани и известен тем, что привлекает нейтрофилы, одну из основных «первых реагирующих» лейкоцитарных популяций. В отличие от мышей, у которых нет гена IL-8, у человека и макаков-циномолгов он присутствует, что делает этих обезьян полезными моделями для человека. В лабораторных испытаниях на человеческих клетках IL-8 активировал оба своих основных рецептора на нейтрофилах и привлек значительно больше этих клеток, чем родственный хемоаттрактант CXCL1, который использует только один из рецепторов. Эта превосходящая «притяжательная» способность указывает на то, что IL-8 является доминирующим переключателем, привлекающим нейтрофилы в хирургическую область, где они могут помогать бороться с опасностью, но также закладывать основу для избыточного рубцевания.
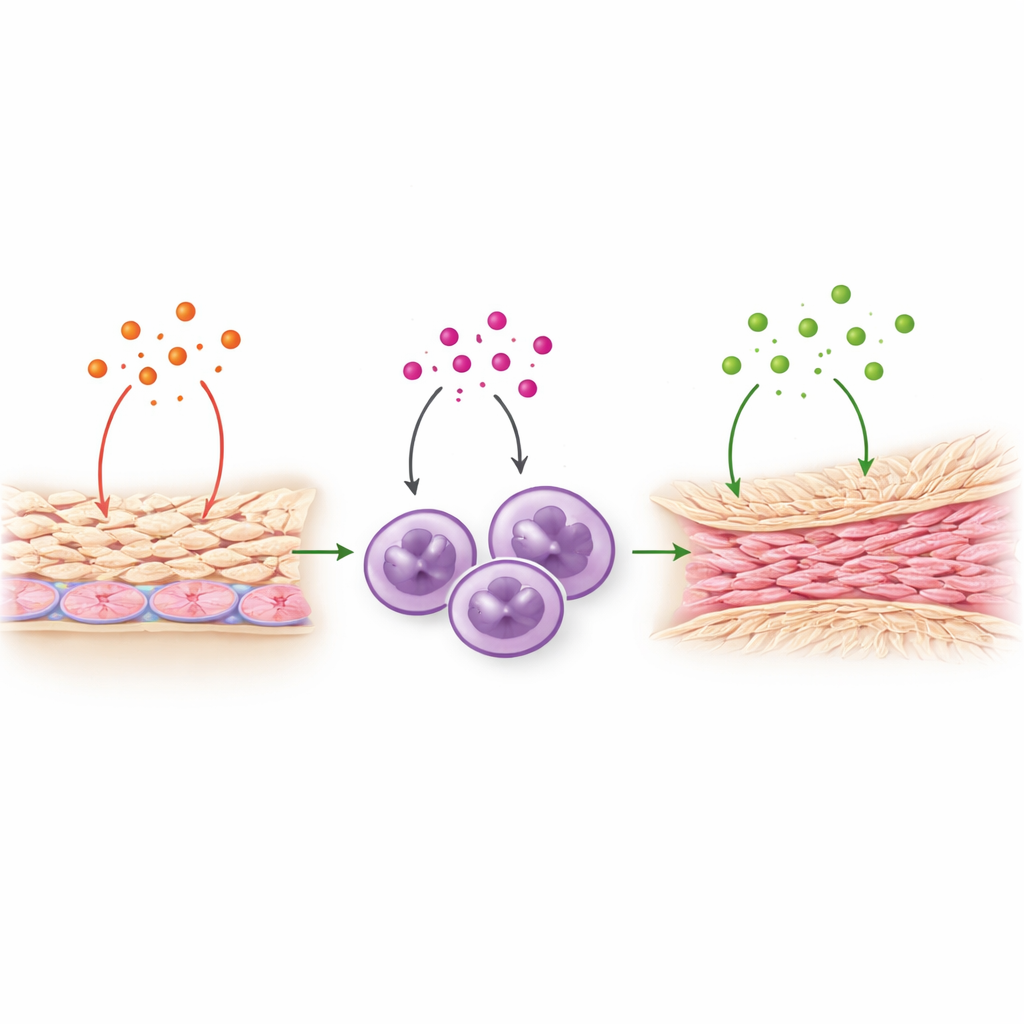
Порочный круг между клетками оболочки и иммунными клетками
Оказалось, что IL-8 делает больше, чем просто привлекает нейтрофилы. Команда показала, что IL-8 может действовать прямо на мезотелиальные клетки, выстилающие внутреннюю поверхность брюшной полости. При воздействии IL-8 эти клетки выделяли больше TNF‑альфа, другого мощного провоспалительного сигнала, уже вовлечённого в образование спаек. В свою очередь, TNF‑альфа стимулировал мезотелиальные клетки синтезировать больше IL-8, что создавало самоподдерживающуюся петлю. TNF‑альфа также побуждал нейтрофилы усиливать продукцию TGF‑beta1, важнейшего регулятора фиброза, который способствует отложению долговременных коллагеновых волокон. В совокупности эти шаги описывают эстафету: IL-8 → активация мезотелия и выделение TNF‑альфа → активация нейтрофилов и выделение TGF‑beta1 → накопление волокнистой рубцовой ткани. Важно, что сам IL-8 напрямую не включал генетическую программу фиброза, но усиливал сигналы, которые это делают.
Испытание блокатора IL-8 на обезьянах
Чтобы увидеть, как этот путь работает в живом организме, учёные использовали макаков-циномолгов, которым провели стандартизированные поврежения брюшной полости и матки для индукции спаек. Уровни IL-8 в повреждённой стенке живота резко возрастали в течение шести часов после операции и снижались к исходному уровню в течение недели, обозначив узкое раннее окно, когда IL-8 наиболее активен. Команда ввела некоторым обезьянам однократную внутривенную дозу AMY109, долго действующего антитела, нейтрализующего IL-8, за два дня до операции. При осмотре лапароскопом через 26 дней у животных, получавших AMY109, было заметно меньше и мельче спаек на стенке живота по сравнению с не получавшими лечение животными. Спайки на матке также, как правило, были менее выражены, а у двух обработанных обезьян полностью отсутствовали, что указывает на то, что ослабление действия IL-8 может защищать несколько участков внутри брюшной полости без очевидного вреда для нормального заживления ран.
Что это может значить для пациентов
В сумме результаты показывают IL-8 как центрального организатора раннего воспаления и последующего фиброза после абдоминальной операции. Сильно привлекая нейтрофилы и создавая петлю обратной связи с мезотелиальными клетками, усиливающую TNF‑альфа и TGF‑beta1, IL-8 способствует превращению кратковременной репаративной реакции в устойчивые внутренние рубцовые тяжи. Блокирование IL-8 антителом вроде AMY109 у обезьян существенно уменьшало эти спайки, указывая на потенциальную новую лекарственную стратегию, нацеленную на биологию процесса, а не только на использование физических барьеров. Если аналогичные результаты подтвердятся у людей, пациенты в будущем могли бы получить короткий курс терапии, блокирующей IL-8, в периоперационном периоде для снижения риска болезненных, меняющих жизнь послеоперационных спаек.
Цитирование: Nakagawa, K., Tanimura, H., Yamazaki, M. et al. IL-8 contributes to postoperative adhesion formation through the crosstalk of neutrophils and mesothelial cells. Sci Rep 16, 14221 (2026). https://doi.org/10.1038/s41598-026-42159-x
Ключевые слова: послеоперационные спайки, интерлейкин-8, нейтрофилы, фиброз, модель на обезьянах