Clear Sky Science · pl
IL-8 przyczynia się do powstawania zrostów pooperacyjnych poprzez dialog neutrofili i komórek mezotelialnych
Dlaczego zrosty po operacji mają znaczenie
Wiele osób po zabiegach w obrębie jamy brzusznej później rozwija wewnętrzne pasma bliznowate, zwane zrostami, które mogą skręcać jelita, powodować przewlekły ból lub utrudniać płodność. Pomimo ich wpływu lekarze dysponują niewieloma niezawodnymi sposobami zapobiegania tworzeniu się tych lepkich włókien. W badaniu tym przeanalizowano silny sygnał odpornościowy zwany IL-8 i pokazano, jak napędza on wczesny ciąg zdarzeń prowadzący od czystego nacięcia chirurgicznego do trwałej wewnętrznej blizny — oraz jak zahamowanie IL-8 za pomocą przeciwciała może znacząco zmniejszyć powstawanie zrostów w modelu naczelich.
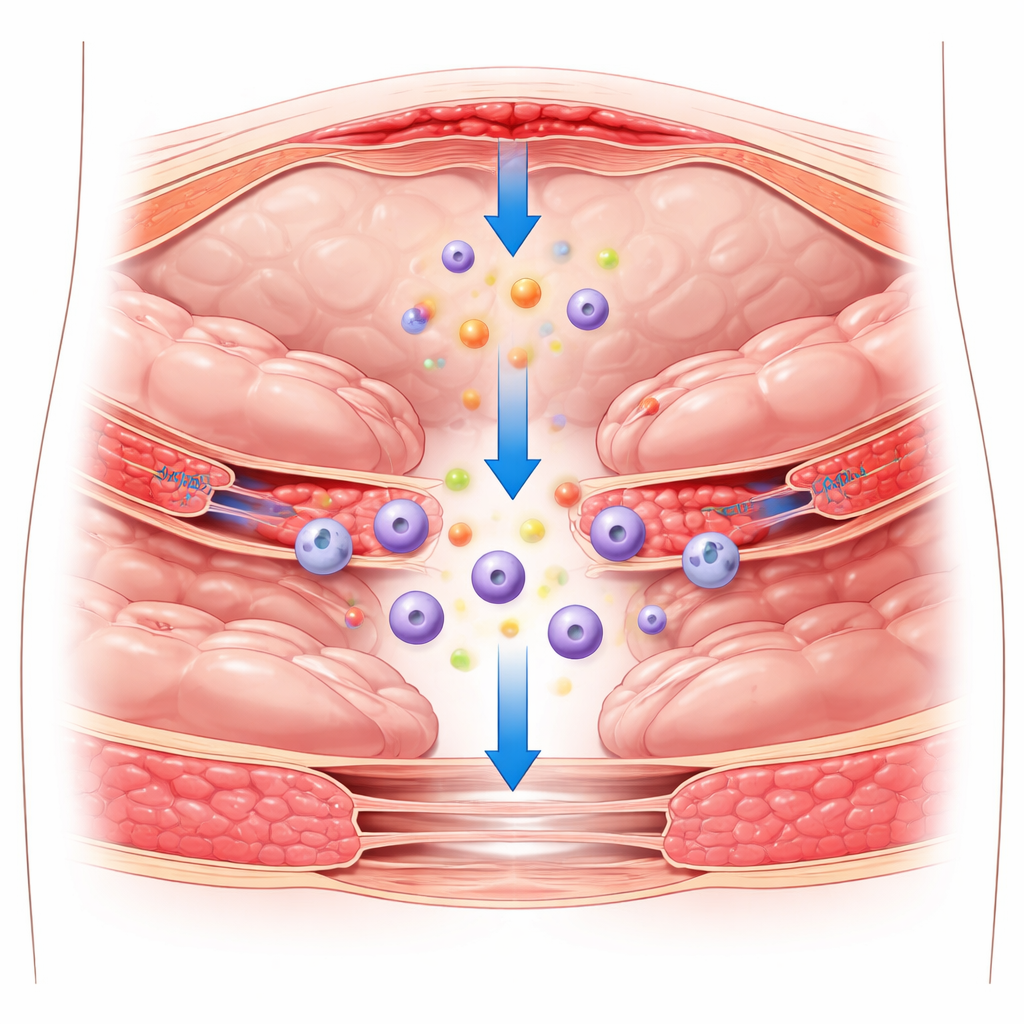
Ukryte blizny pozostawione przez operację
Po operacji w jamie brzusznej uszkodzona może zostać gładka wyściółka pokrywająca narządy i ścianę brzucha. Zwykle ta wyściółka, złożona z cienkiej warstwy komórek zwanych komórkami mezotelialnymi, umożliwia organom ślizganie się względem siebie bez przywierania. W przypadku uszkodzenia reaguje ona stanem zapalnym: do tkanek napływają komórki odpornościowe, uruchamiane są szlaki krzepnięcia krwi, a powstaje tymczasowa białkowa sieć zwana fibryną. Jeśli ta wczesna odpowiedź nie jest ściśle kontrolowana, fibryna może stać się szkieletem trwałych włóknistych pasm, które łączą narządy, tworząc zrosty pooperacyjne. Istniejące metody zapobiegania polegają głównie na stosowaniu fizycznych folii lub żeli oddzielających tkanki, ale bariery te działają tylko częściowo i nie rozwiązują problemu.
Kluczowy sygnał przywołujący pierwszych ratowników
Naukowcy skupili się na IL-8, chemicznym sygnale, który szybko rośnie po uszkodzeniu tkanek i który jest znany z przyciągania neutrofili, jednych z głównych „pierwszych ratowników” wśród białych krwinek. W odróżnieniu od myszy, które nie posiadają genu IL-8, ludzie i makaki czynomolguskie go mają, co czyni te małpy przydatnym modelem zastępczym dla ludzi. W badaniach laboratoryjnych z ludzkimi komórkami IL-8 aktywował oba swoje główne receptory na neutrofilach i przyciągał znacznie więcej tych komórek niż spokrewniony chemokin, CXCL1, który wykorzystuje tylko jeden receptor. Ta większa siła przyciągania sugeruje, że IL-8 jest dominującym przełącznikiem ściągającym neutrofile na pole operacyjne, gdzie mogą one pomagać w walce z zagrożeniem, ale także przygotowywać grunt pod nadmierne bliznowacenie.
Błędne koło między komórkami wyściółki a komórkami odpornościowymi
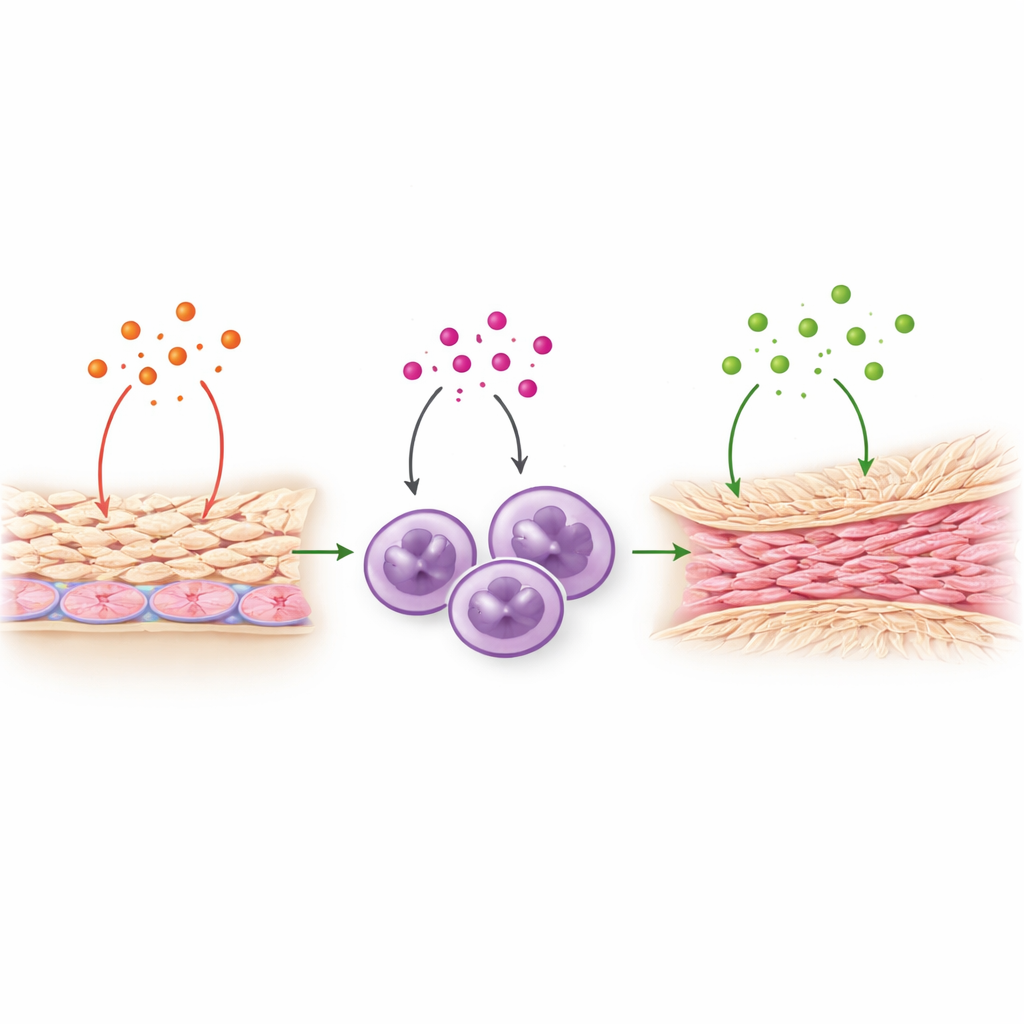
Okazało się, że IL-8 robi więcej niż tylko przywołuje neutrofile. Zespół wykazał, że IL-8 może działać bezpośrednio na komórki mezotelialne wyściełające jamę brzuszną. Po ekspozycji na IL-8 te komórki wydzielały większe ilości TNF‑alpha, kolejnego silnego sygnału zapalnego, który już był powiązany z powstawaniem zrostów. Z kolei TNF‑alpha skłaniał komórki mezotelialne do produkcji większej ilości IL-8, tworząc samonapędzającą się pętlę. TNF‑alpha także stymulował neutrofile do zwiększonej produkcji TGF‑beta1, głównego regulatora włóknienia, który zachęca tkankę do odkładania trwałych włókien kolagenowych. Razem te kroki kreślą przekaz: IL-8 → aktywacja mezotelium i uwolnienie TNF‑alpha → aktywacja neutrofili i uwolnienie TGF‑beta1 → narastanie włóknistej tkanki bliznowatej. Co ważne, IL-8 sam w sobie nie włączał bezpośrednio genów włóknienia, lecz wzmacniał sygnały, które to robią.
Testowanie blokeru IL-8 u małp
Aby zbadać, jak ta ścieżka zachowuje się w żywym organizmie, naukowcy użyli makaków czynomolguskich, którym dokonano ustandaryzowanych uszkodzeń brzucha i macicy, by wywołać zrosty. Poziomy IL-8 w uszkodzonej ścianie brzucha gwałtownie wzrosły w ciągu sześciu godzin po operacji i zmalały w kierunku wartości wyjściowych w ciągu tygodnia, wyznaczając wąskie, wczesne okno, kiedy IL-8 jest najbardziej aktywna. Zespół podał następnie niektórym małpom jedną dożylną dawkę AMY109, długo działającego przeciwciała neutralizującego IL-8, na dwa dni przed operacją. Gdy zwierzęta zbadano laparoskopowo 26 dni później, te, które otrzymały AMY109, miały wyraźnie mniejsze i rzadsze zrosty na ścianie brzucha niż zwierzęta nieleczone. Zrosty na macicy również miały tendencję do łagodniejszego przebiegu, a u dwóch leczonych małp nie wystąpiły wcale, co sugeruje, że osłabienie sygnalizacji IL-8 może chronić wiele miejsc wewnątrz jamy brzusznej bez oczywistego szkodzenia normalnemu gojeniu ran.
Co to może znaczyć dla pacjentów
Podsumowując, wyniki stawiają IL-8 jako centralnego organizatora wczesnego stanu zapalnego i późniejszego włóknienia po operacji brzusznej. Poprzez silne rekrutowanie neutrofili i napędzanie pętli sprzężenia zwrotnego z komórkami mezotelialnymi, która zwiększa TNF‑alpha i TGF‑beta1, IL-8 przyczynia się do przekształcenia krótkotrwałej odpowiedzi gojenia w uporczywe wewnętrzne pasma bliznowate. Zahamowanie IL-8 przeciwciałem takim jak AMY109 u małp znacząco zmniejszyło te zrosty, wskazując na potencjalnie nową strategię lekową celującą w biologię, zamiast opierać się wyłącznie na barierach fizycznych. Jeśli podobne rezultaty zostaną potwierdzone u ludzi, pacjenci mogliby kiedyś otrzymać krótki kurs leczenia blokującego IL-8 w okresie okołozabiegowym, aby zmniejszyć ryzyko bolesnych, zmieniających życie zrostów pooperacyjnych.
Cytowanie: Nakagawa, K., Tanimura, H., Yamazaki, M. et al. IL-8 contributes to postoperative adhesion formation through the crosstalk of neutrophils and mesothelial cells. Sci Rep 16, 14221 (2026). https://doi.org/10.1038/s41598-026-42159-x
Słowa kluczowe: zrosty pooperacyjne, interleukina-8, neutrofile, zwłóknienie, model małpi