Clear Sky Science · pt
IL-8 contribui para a formação de aderências pós-operatórias por meio do diálogo entre neutrófilos e células mesoteliais
Por que as faixas de cicatriz após a cirurgia importam
Muitas pessoas que passam por cirurgia abdominal desenvolvem mais tarde faixas internas de tecido cicatricial, chamadas aderências, que podem torcer o intestino, causar dor crônica ou interferir na fertilidade. Apesar do impacto, os médicos dispõem de poucas maneiras confiáveis de evitar que essas faixas aderentes se formem. Este estudo investiga um potente sinal imunológico chamado IL-8 e mostra como ele impulsiona a cadeia inicial de eventos que leva de um corte cirúrgico limpo a tecido cicatricial interno resistente — e como bloquear a IL-8 com um anticorpo pode reduzir marcadamente essas aderências em um modelo de primata.
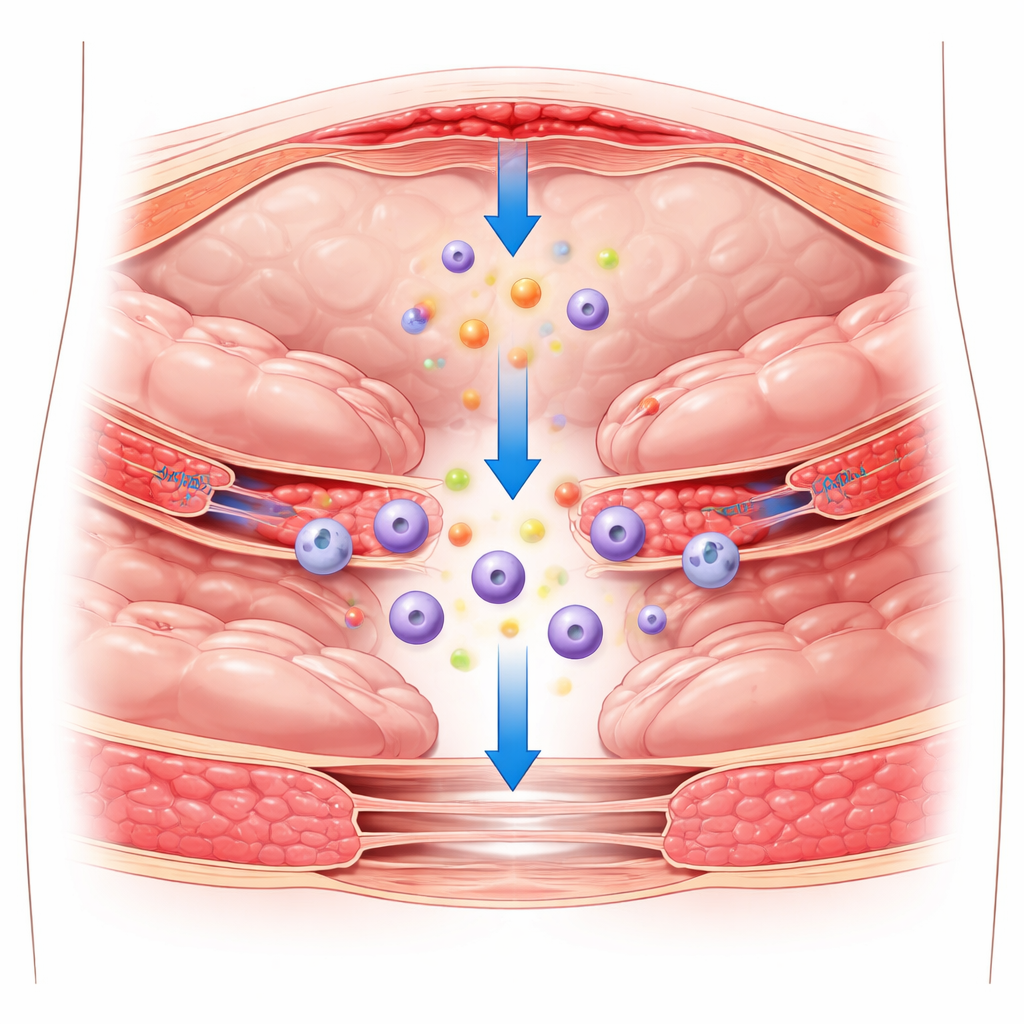
As cicatrizes ocultas deixadas pela cirurgia
Após uma operação no abdome, o revestimento liso que cobre os órgãos e a parede abdominal pode ser danificado. Normalmente esse revestimento, formado por uma fina camada de células chamadas mesoteliais, ajuda os órgãos a deslizar uns pelos outros sem aderir. Quando lesionado, ele reage com inflamação: células imunes afluem, vias de coagulação são ativadas e uma malha proteica temporária chamada fibrina se forma. Se essa resposta inicial não for rigidamente controlada, a fibrina pode se tornar a base para bandas fibrosas permanentes que prendem órgãos entre si, criando aderências pós-operatórias. Os métodos de prevenção existentes usam principalmente filmes ou géis físicos para manter os tecidos separados, mas essas barreiras funcionam apenas parcialmente e não resolveram o problema.
Um sinal-chave que convoca os primeiros socorros
Os pesquisadores concentraram-se na IL-8, um sinal químico que aumenta rapidamente quando o tecido é lesionado e que é conhecido por atrair neutrófilos, um dos principais leucócitos “primeiros socorros” do corpo. Ao contrário de camundongos, que não possuem o gene da IL-8, humanos e macacos-cinomolgos o têm, tornando esses macacos substitutos úteis para humanos. Em testes de laboratório com células humanas, a IL-8 ativou ambos os seus receptores principais nos neutrófilos e atraiu muito mais dessas células do que uma quimiocina relacionada, CXCL1, que usa apenas um dos receptores. Esse poder de atração superior sugere que a IL-8 é um interruptor dominante para trazer neutrófilos ao campo cirúrgico, onde eles podem ajudar a combater perigos, mas também preparar o terreno para cicatrização excessiva.
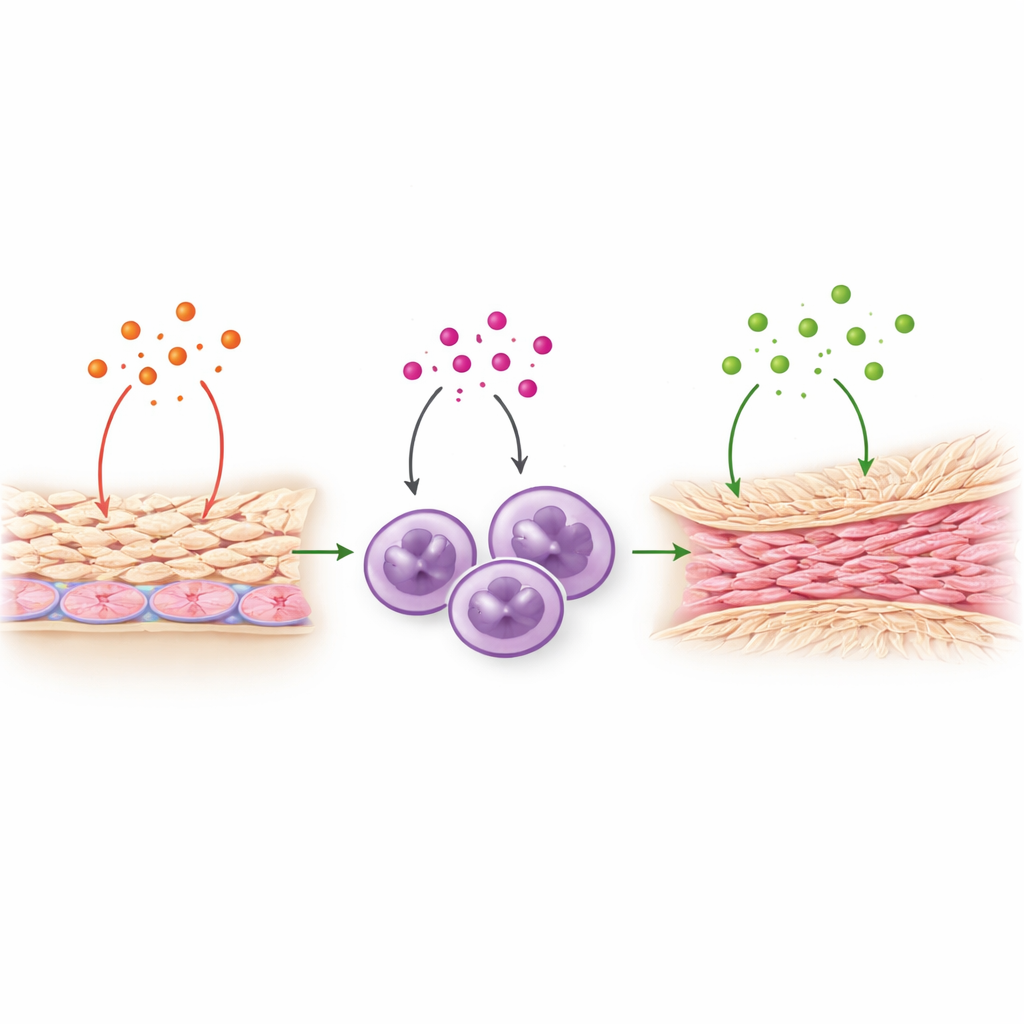
Um ciclo vicioso entre células do revestimento e células imunes
A IL-8 revelou-se bem mais do que um simples chamador de neutrófilos. A equipe demonstrou que a IL-8 pode atuar diretamente sobre as células mesoteliais, que revestem o interior do abdome. Quando expostas à IL-8, essas células liberaram maiores quantidades de TNF‑alfa, outro potente sinal inflamatório já implicado na formação de aderências. Por sua vez, o TNF‑alfa estimulou as células mesoteliais a produzir mais IL-8, estabelecendo um circuito auto-reforçador. O TNF‑alfa também incentivou os neutrófilos a aumentar a produção de TGF‑beta1, um controlador mestre da fibrose que estimula o tecido a depositar fibras de colágeno duradouras. Juntos, esses passos delineiam uma revezamento: IL-8 → ativação mesotelial e liberação de TNF‑alfa → ativação de neutrófilos e liberação de TGF‑beta1 → acúmulo de tecido cicatricial fibrótico. Importante, a própria IL-8 não acionou diretamente genes de fibrose, mas amplificou os sinais que o fazem.
Testando um bloqueador de IL-8 em macacos
Para ver como essa via se comporta em um organismo vivo, os cientistas usaram macacos-cinomolgos que foram submetidos a lesões padronizadas na parede abdominal e no útero para desencadear aderências. Os níveis de IL-8 na parede abdominal lesionada dispararam dentro de seis horas após a cirurgia e diminuíram em direção à linha de base dentro de uma semana, marcando uma janela inicial estreita na qual a IL-8 está mais ativa. A equipe então administrou a alguns macacos uma dose única intravenosa de AMY109, um anticorpo de longa ação que neutraliza a IL-8, dois dias antes da cirurgia. Quando os animais foram examinados 26 dias depois por laparoscopia, aqueles que haviam recebido AMY109 apresentaram aderências na parede abdominal marcadamente menores e em menor número do que os animais não tratados. As aderências no útero também tenderam a ser mais brandas e, em dois macacos tratados, estavam ausentes, sugerindo que atenuar a IL-8 pode proteger múltiplos sítios dentro do abdome sem prejuízo óbvio à cicatrização normal.
O que isso pode significar para os pacientes
Em conjunto, os achados colocam a IL-8 como um organizador central da inflamação inicial e da fibrose tardia após cirurgia abdominal. Ao recrutar fortemente neutrófilos e conduzir um circuito de feedback com células mesoteliais que eleva TNF‑alfa e TGF‑beta1, a IL-8 ajuda a transformar uma resposta de cura de curta duração em faixas internas de cicatriz persistentes. Bloquear a IL-8 com um anticorpo como o AMY109 em macacos reduziu substancialmente essas aderências, apontando para uma nova estratégia medicamentosa potencial que mira a biologia em vez de depender apenas de barreiras físicas. Se resultados semelhantes forem confirmados em humanos, os pacientes podem um dia receber um curto curso de tratamento bloqueador de IL-8 ao redor do momento da cirurgia para reduzir o risco de aderências pós-operatórias dolorosas e que alteram a vida.
Citação: Nakagawa, K., Tanimura, H., Yamazaki, M. et al. IL-8 contributes to postoperative adhesion formation through the crosstalk of neutrophils and mesothelial cells. Sci Rep 16, 14221 (2026). https://doi.org/10.1038/s41598-026-42159-x
Palavras-chave: aderências pós-operatórias, interleucina-8, neutrófilos, fibrose, modelo de macaco