Clear Sky Science · de
IL-8 trägt zur Bildung postoperativer Verwachsungen durch das Zusammenspiel von Neutrophilen und Mesothelzellen bei
Warum Narbenbänder nach Operationen wichtig sind
Viele Menschen, die sich einer Bauchoperation unterziehen, entwickeln später innere Narbenbänder, sogenannte Verwachsungen, die den Darm verdrehen, chronische Schmerzen verursachen oder die Fruchtbarkeit beeinträchtigen können. Trotz ihrer Auswirkungen haben Ärztinnen und Ärzte nur wenige verlässliche Mittel, um das Entstehen dieser klebrigen Stränge zu verhindern. Diese Studie untersucht ein starkes immunologisches Signal namens IL-8 und zeigt, wie es die frühe Kaskade von Ereignissen antreibt, die von einem sauberen chirurgischen Schnitt zu hartem Narbengewebe im Inneren führt — und wie das Blockieren von IL-8 mit einem Antikörper diese Verwachsungen in einem Primatenmodell deutlich reduzieren kann.
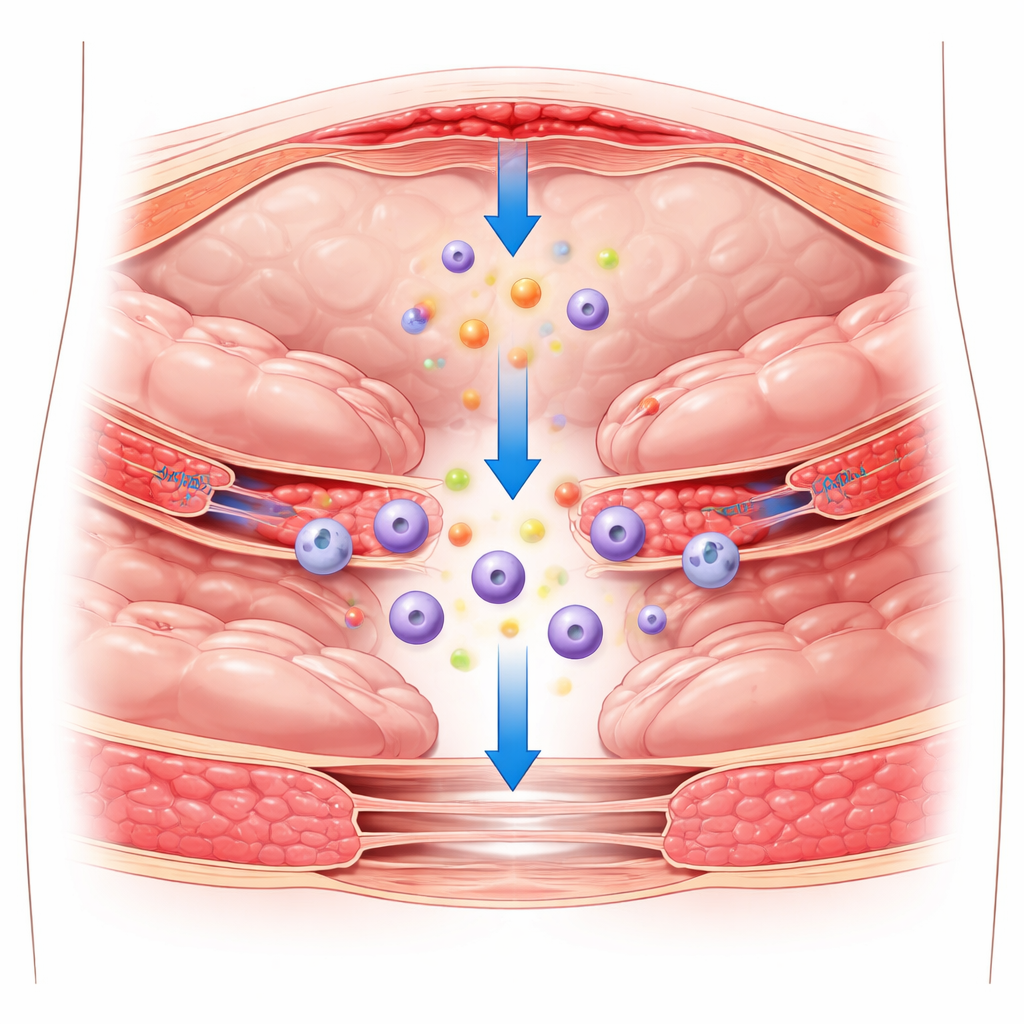
Die verborgenen Narben nach einer Operation
Nach einem Eingriff im Bauchraum kann die glatte Auskleidung, die Organe und die Bauchwand bedeckt, geschädigt werden. Normalerweise hilft diese Auskleidung, die aus einer dünnen Zellschicht namens Mesothelzellen besteht, dabei, dass Organe aneinander vorbeigleiten, ohne zu verkleben. Bei Verletzung reagiert sie mit Entzündung: Immunzellen strömen herbei, Gerinnungswege werden aktiviert und ein vorübergehendes Proteinnetz namens Fibrin bildet sich. Wenn diese frühe Reaktion nicht streng kontrolliert wird, kann das Fibrin zur Grundlage für dauerhafte faserige Bänder werden, die Organe miteinander verbinden und postoperative Verwachsungen schaffen. Bestehende Präventionsmethoden verwenden größtenteils physische Folien oder Gele, um Gewebe auseinanderzuhalten, aber diese Barrieren wirken nur teilweise und haben das Problem nicht gelöst.
Ein Schlüsselsignal, das die Ersthelfer heranzieht
Die Forschenden konzentrierten sich auf IL-8, ein chemisches Signal, das bei Gewebeverletzung schnell ansteigt und dafür bekannt ist, Neutrophile anzulocken — eine der wichtigsten „Ersthelfer“-Weißen-Blutkörperchen des Körpers. Anders als Mäuse, die kein IL-8-Gen besitzen, haben Menschen und Zytomolgusaffen dieses Gen, was diese Affen zu nützlichen Modellorganismen für den Menschen macht. In Laborversuchen mit menschlichen Zellen aktivierte IL-8 beide seiner Hauptrezeptoren auf Neutrophilen und zog deutlich mehr dieser Zellen an als ein verwandtes Chemokin, CXCL1, das nur einen der Rezeptoren nutzt. Diese überlegene Anziehungskraft deutet darauf hin, dass IL-8 ein dominanter Schalter ist, um Neutrophile in das Operationsgebiet zu bringen, wo sie zwar bei der Abwehr helfen, aber auch die Grundlage für übermäßige Narbenbildung legen können.
Ein Teufelskreis zwischen Auskleidungszellen und Immunzellen
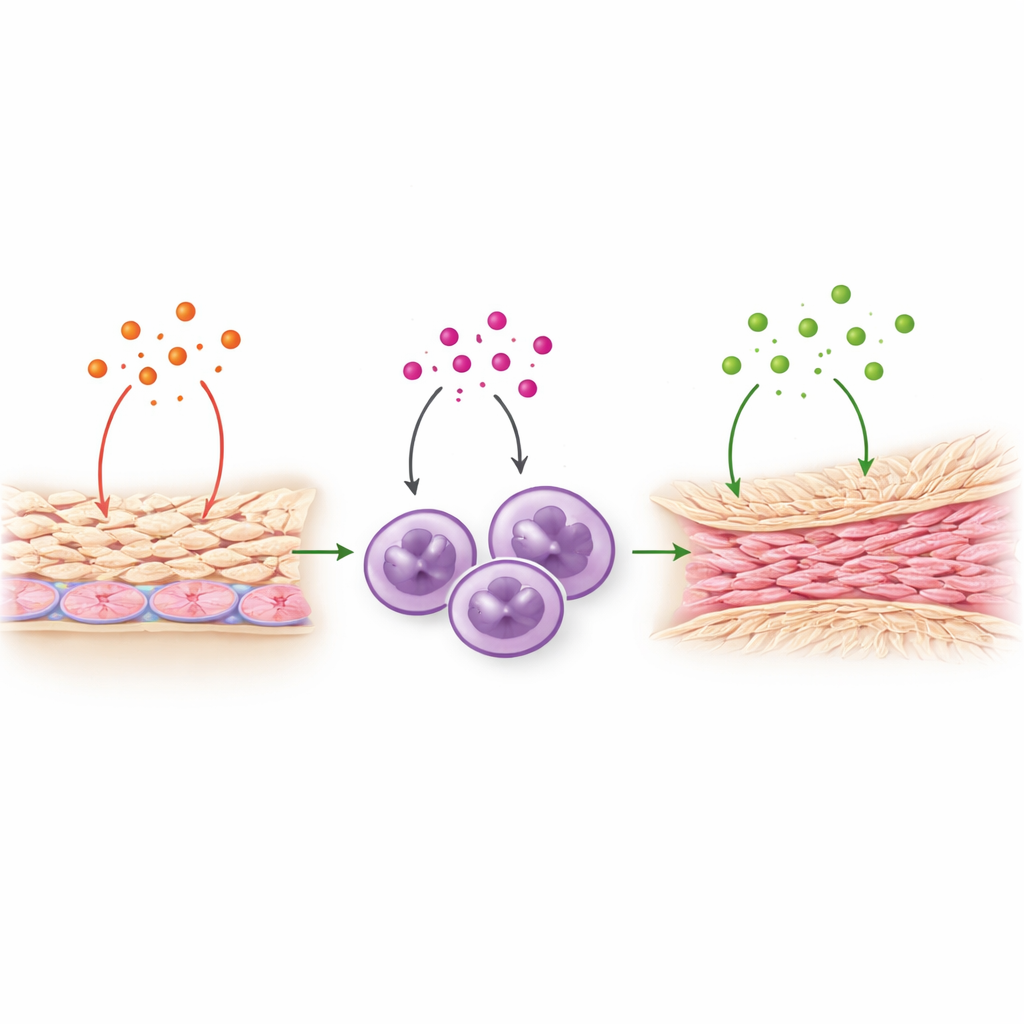
IL-8 erwies sich als mehr als nur Rufzeichen für Neutrophile. Das Team zeigte, dass IL-8 direkt auf Mesothelzellen wirken kann, die den inneren Bauch auskleiden. Unter IL-8-Exposition setzten diese Auskleidungszellen höhere Mengen an TNF‑alpha frei, ein weiteres starkes Entzündungssignal, das bereits mit der Verwachsungsbildung in Verbindung gebracht wurde. Umgekehrt regte TNF‑alpha die Mesothelzellen an, mehr IL-8 zu produzieren, wodurch eine sich selbst verstärkende Schleife entstand. TNF‑alpha stimulierte außerdem Neutrophile zur verstärkten Produktion von TGF‑beta1, einem zentralen Regulator der Fibrose, der das Gewebe zur Ablagerung langlebiger Kollagenfasern anregt. Zusammengenommen skizzieren diese Schritte eine Staffelübergabe: IL-8 → Aktivierung des Mesothels und Freisetzung von TNF‑alpha → Aktivierung der Neutrophilen und Freisetzung von TGF‑beta1 → Aufbau faserigen Narbengewebes. Wichtig ist, dass IL-8 selbst nicht direkt Fibrosegene anschaltete, sondern die Signale verstärkte, die dies tun.
Test eines IL-8-Blockers bei Affen
Um zu sehen, wie dieser Signalweg in einem lebenden Organismus funktioniert, setzten die Wissenschaftler Zytomolgusaffen ein, die standardisierte Verletzungen von Bauch- und Gebärmuttergewebe erlitten, um Verwachsungen auszulösen. Die IL-8-Spiegel in der verletzten Bauchwand stiegen innerhalb von sechs Stunden nach der Operation an und fielen innerhalb einer Woche wieder gegen den Ausgangswert, was ein enges frühes Zeitfenster markiert, in dem IL-8 am aktivsten ist. Das Team verabreichte einigen Affen dann zwei Tage vor der Operation eine einzelne intravenöse Dosis von AMY109, einem langwirksamen Antikörper, der IL‑8 neutralisiert. Bei der Untersuchung der Tiere 26 Tage später mit einem Laparoskop hatten die mit AMY109 behandelten Tiere deutlich kleinere und weniger Verwachsungen an der Bauchwand als unbehandelte Tiere. Verwachsungen an der Gebärmutter waren ebenfalls tendenziell milder, und bei zwei behandelten Affen fehlten sie völlig, was darauf hindeutet, dass das Abdämpfen von IL-8 mehrere Bereiche im Bauchraum schützen kann, ohne offensichtliche Schäden am normalen Wundheilungsprozess zu verursachen.
Was das für Patienten bedeuten könnte
In der Summe stellen die Befunde IL-8 als zentralen Organisator früher Entzündungsreaktionen und späterer Fibrose nach Bauchoperationen dar. Indem IL-8 Neutrophile stark anzieht und eine Rückkopplungsschleife mit Mesothelzellen antreibt, die TNF‑alpha und TGF‑beta1 erhöht, hilft IL-8 dabei, eine kurzlebige Heilungsreaktion in hartnäckige innere Narbenbänder zu verwandeln. Das Blockieren von IL-8 mit einem Antikörper wie AMY109 reduzierte diese Verwachsungen bei Affen deutlich und weist auf eine potenzielle neue Medikationsstrategie hin, die die zugrundeliegende Biologie angreift, statt sich nur auf physische Barrieren zu stützen. Wenn ähnliche Ergebnisse beim Menschen bestätigt werden, könnten Patienten eines Tages rund um den Zeitpunkt der Operation eine kurze Behandlung mit einem IL‑8‑Blocker erhalten, um ihr Risiko für schmerzhafte, lebensverändernde postoperative Verwachsungen zu senken.
Zitation: Nakagawa, K., Tanimura, H., Yamazaki, M. et al. IL-8 contributes to postoperative adhesion formation through the crosstalk of neutrophils and mesothelial cells. Sci Rep 16, 14221 (2026). https://doi.org/10.1038/s41598-026-42159-x
Schlüsselwörter: postoperative Verwachsungen, Interleukin-8, Neutrophile, Fibrose, Affendmodell