Clear Sky Science · it
IL-8 contribuisce alla formazione di aderenze postoperatorie attraverso il dialogo tra neutrofili e cellule mesoteliali
Perché le bande cicatriziali dopo un intervento chirurgico sono importanti
Molte persone sottoposte a interventi addominali sviluppano in seguito bande cicatriziali interne, chiamate aderenze, che possono torcere l’intestino, causare dolore cronico o interferire con la fertilità. Nonostante il loro impatto, i medici hanno pochi strumenti affidabili per prevenire la formazione di questi filamenti aderenti. Questo studio indaga un potente segnale immunitario chiamato IL-8 e mostra come esso guidi la catena iniziale di eventi che porta da un taglio chirurgico pulito a tessuto cicatriziale interno resistente — e come il blocco di IL-8 con un anticorpo possa ridurre notevolmente queste aderenze in un modello di primate.
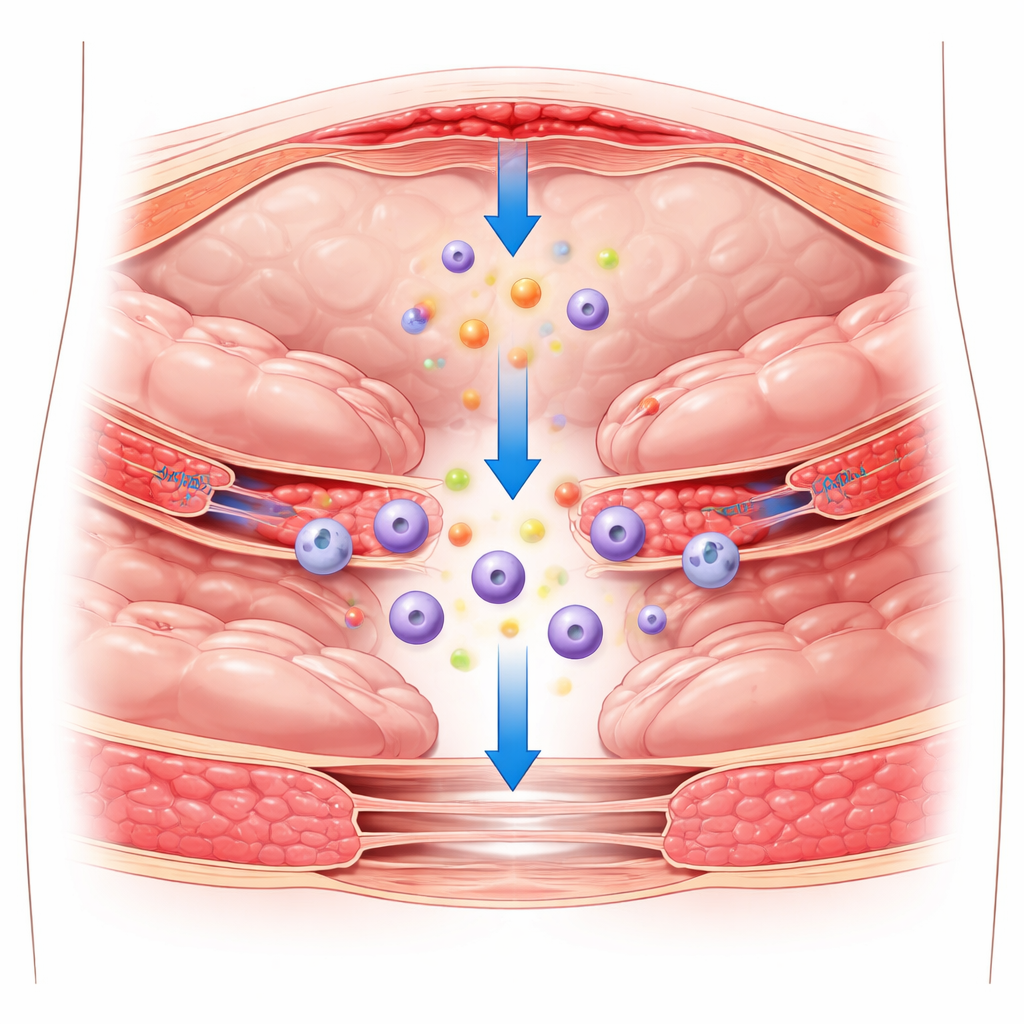
Le cicatrici nascoste lasciate dalla chirurgia
Dopo un’operazione nell’addome, il rivestimento liscio che copre gli organi e la parete addominale può essere danneggiato. Normalmente quel rivestimento, costituito da un sottile strato di cellule chiamate cellule mesoteliali, aiuta gli organi a scorrere l’uno sull’altro senza aderire. Quando è lesionato, risponde con infiammazione: le cellule immunitarie affluiscono, si attivano le vie di coagulazione e si forma una rete proteica temporanea chiamata fibrina. Se questa risposta iniziale non è strettamente controllata, la fibrina può diventare l’ossatura per bande fibrose permanenti che legano gli organi tra loro, creando aderenze postoperatorie. I metodi preventivi esistenti utilizzano per lo più film o gel fisici per mantenere i tessuti separati, ma queste barriere funzionano solo parzialmente e non hanno risolto il problema.
Un segnale chiave che richiama i primi soccorritori
I ricercatori si sono concentrati su IL-8, un segnale chimico che aumenta rapidamente quando il tessuto è danneggiato e che è noto per attrarre i neutrofili, uno dei principali globuli bianchi “primi soccorritori” del corpo. Diversamente dai topi, che non possiedono il gene IL-8, gli esseri umani e le scimmie cynomolgus lo hanno, rendendo queste scimmie utili modelli surrogati per l’uomo. Nei test di laboratorio con cellule umane, IL-8 ha attivato entrambi i suoi recettori principali sui neutrofili e ha attirato molti più di questi cellule rispetto a una chemochina correlata, CXCL1, che utilizza solo uno dei recettori. Questa superiore capacità di richiamo suggerisce che IL-8 sia un interruttore dominante per portare i neutrofili nel campo chirurgico, dove possono contribuire a contrastare il pericolo ma anche gettare le basi per una cicatrizzazione eccessiva.
Un circolo vizioso tra cellule del rivestimento e cellule immunitarie
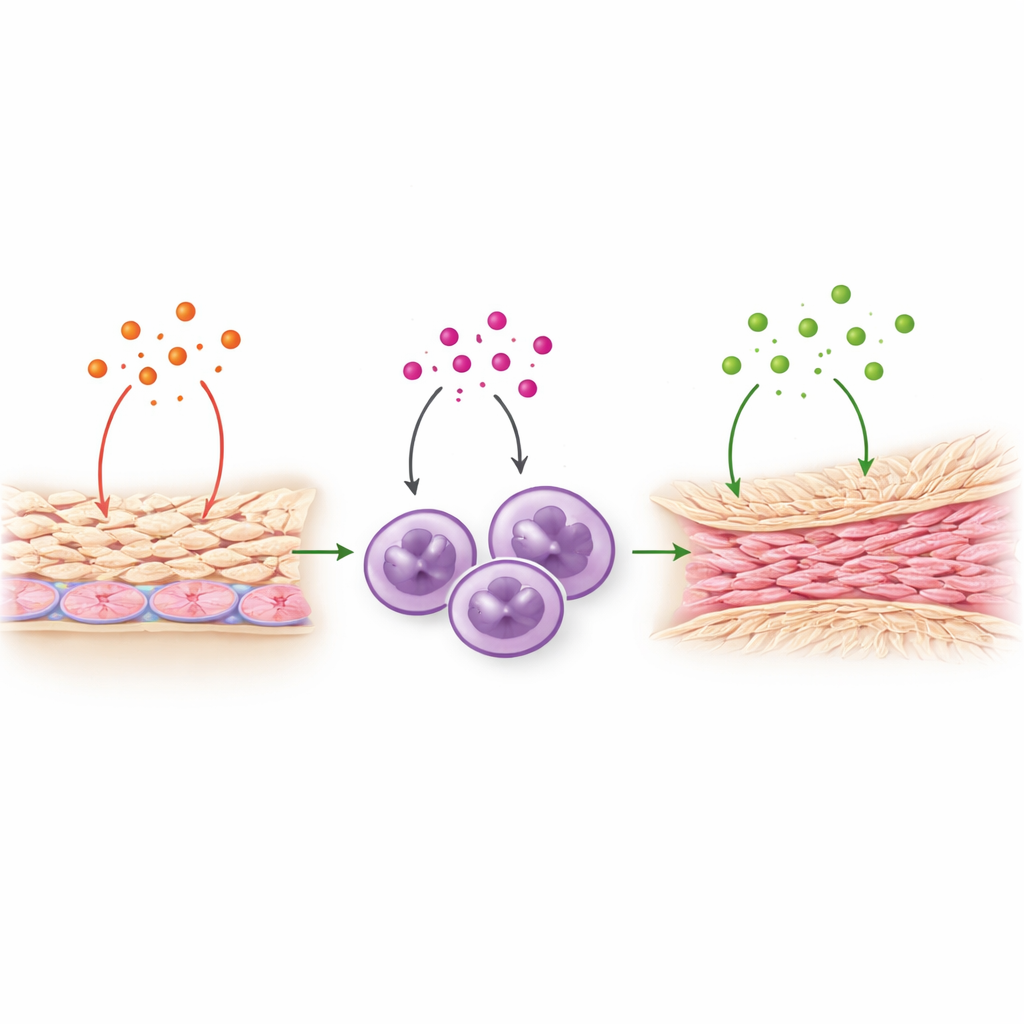
IL-8 si è rivelato fare più che richiamare i neutrofili. Il gruppo ha dimostrato che IL-8 può agire direttamente sulle cellule mesoteliali, che rivestono l’interno dell’addome. Quando esposte a IL-8, queste cellule di rivestimento rilasciavano quantità maggiori di TNF‑alpha, un altro potente segnale infiammatorio già implicato nella formazione delle aderenze. A sua volta, il TNF‑alpha spingeva le cellule mesoteliali a produrre più IL-8, instaurando un circuito auto‑rinforzante. Il TNF‑alpha stimolava inoltre i neutrofili ad aumentare la produzione di TGF‑beta1, un regolatore maestro della fibrosi che favorisce la deposizione di fibre di collagene durature. Insieme, questi passaggi delineano un relay: IL-8 → attivazione delle mesoteliali e rilascio di TNF‑alpha → attivazione dei neutrofili e rilascio di TGF‑beta1 → accumulo di tessuto cicatriziale fibroso. È importante notare che IL-8 di per sé non attivava direttamente i geni della fibrosi, ma amplificava i segnali che lo fanno.
Testare un bloccante di IL-8 nelle scimmie
Per vedere come questo percorso si comporta in un organismo vivente, gli scienziati hanno usato scimmie cynomolgus sottoposte a lesioni addominali e uterine standardizzate per indurre aderenze. I livelli di IL-8 nella parete addominale lesa sono aumentati rapidamente entro sei ore dall’intervento e sono tornati verso il livello basale entro una settimana, segnando una stretta finestra precoce in cui IL-8 è più attivo. Il gruppo ha quindi somministrato ad alcune scimmie una singola dose endovenosa di AMY109, un anticorpo a lunga durata d’azione che neutralizza IL‑8, due giorni prima dell’intervento. Quando gli animali sono stati esaminati 26 giorni dopo con un laparoscopio, quelli trattati con AMY109 presentavano aderenze sulla parete addominale significativamente più piccole e meno numerose rispetto agli animali non trattati. Anche le aderenze sull’utero tendevano a essere più lievi e in due scimmie trattate erano assenti del tutto, suggerendo che l’attenuazione di IL-8 può proteggere più siti all’interno dell’addome senza danni evidenti alla normale guarigione delle ferite.
Cosa potrebbe significare per i pazienti
Complessivamente, i risultati ritraggono IL-8 come un organizzatore centrale dell’infiammazione iniziale e della successiva fibrosi dopo un intervento addominale. Reclutando fortemente i neutrofili e alimentando un circuito di retroazione con le cellule mesoteliali che aumenta TNF‑alpha e TGF‑beta1, IL-8 contribuisce a trasformare una risposta di guarigione di breve durata in bande cicatriziali interne ostinate. Il blocco di IL-8 con un anticorpo come AMY109 nelle scimmie ha ridotto sostanzialmente queste aderenze, indicando una potenziale nuova strategia farmacologica che mira alla biologia piuttosto che affidarsi solo a barriere fisiche. Se risultati analoghi saranno confermati nell’uomo, un giorno i pazienti potrebbero ricevere un breve trattamento intorno al periodo chirurgico volto a ridurre il rischio di aderenze postoperatorie dolorose e che cambiano la vita.
Citazione: Nakagawa, K., Tanimura, H., Yamazaki, M. et al. IL-8 contributes to postoperative adhesion formation through the crosstalk of neutrophils and mesothelial cells. Sci Rep 16, 14221 (2026). https://doi.org/10.1038/s41598-026-42159-x
Parole chiave: aderenze postoperatorie, interleuchina-8, neutrofili, fibrosi, modello di scimmia