Clear Sky Science · fr
IL-8 contribue à la formation d’adhérences post-opératoires via le dialogue entre neutrophiles et cellules mésothéliales
Pourquoi les bandes cicatricielles après une chirurgie comptent
Beaucoup de personnes ayant subi une chirurgie abdominale développent par la suite des bandes cicatricielles internes, appelées adhérences, qui peuvent tordre l’intestin, provoquer des douleurs chroniques ou gêner la fertilité. Malgré leur impact, les médecins disposent de peu de moyens fiables pour empêcher la formation de ces structures collantes. Cette étude examine un signal immunitaire puissant, l’IL-8, et montre comment il déclenche la chaîne d’évènements précoces qui conduit d’une incision chirurgicale nette à des tissus cicatriciels internes résistants — et comment le blocage de l’IL-8 par un anticorps peut réduire fortement ces adhérences dans un modèle de primate.
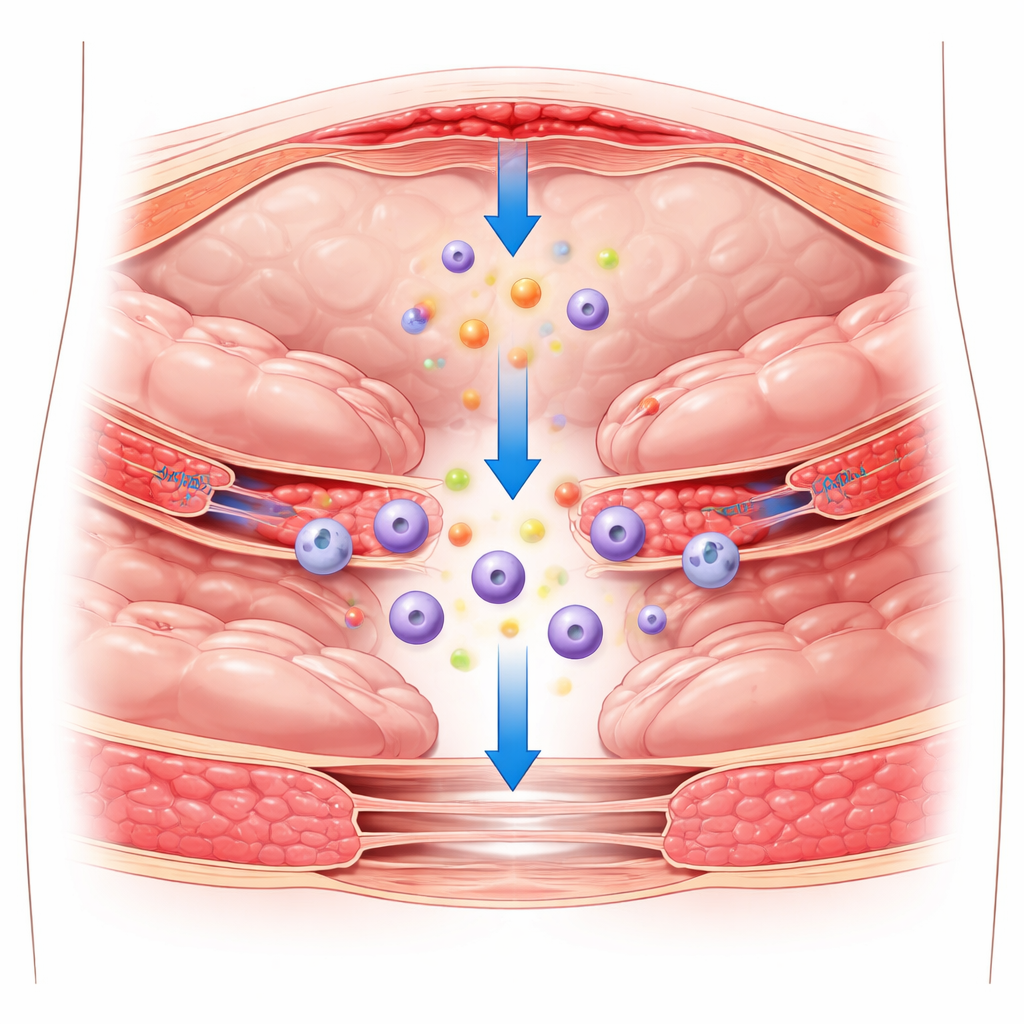
Les cicatrices cachées laissées par la chirurgie
Après une intervention dans l’abdomen, le revêtement lisse qui recouvre les organes et la paroi abdominale peut être endommagé. Normalement, ce revêtement, constitué d’une fine couche de cellules appelées cellules mésothéliales, permet aux organes de glisser les uns sur les autres sans adhérer. Lorsqu’il est blessé, il réagit par une inflammation : des cellules immunitaires affluent, les voies de coagulation sanguine s’activent et un réseau protéique temporaire appelé fibrine se forme. Si cette réponse initiale n’est pas strictement contrôlée, la fibrine peut devenir l’ossature de bandes fibreuses permanentes qui relient les organes entre eux, créant des adhérences post-opératoires. Les méthodes de prévention existantes utilisent principalement des films ou des gels physiques pour séparer les tissus, mais ces barrières ne fonctionnent qu’en partie et n’ont pas résolu le problème.
Un signal clé qui attire les premiers intervenants
Les chercheurs se sont concentrés sur l’IL-8, un signal chimique qui augmente rapidement lors d’une lésion tissulaire et qui est connu pour attirer les neutrophiles, l’une des principales cellules « premiers intervenants » du système immunitaire. Contrairement aux souris, qui ne possèdent pas le gène IL-8, les humains et les singes cynomolgus en sont dotés, ce qui rend ces singes des modèles pertinents pour l’homme. Dans des essais en laboratoire sur des cellules humaines, l’IL-8 a activé ses deux récepteurs principaux sur les neutrophiles et a attiré bien plus de ces cellules qu’une chimiokine connexe, CXCL1, qui n’utilise qu’un seul récepteur. Ce pouvoir d’attraction supérieur suggère que l’IL-8 est un commutateur dominant pour amener les neutrophiles sur le site opératoire, où ils peuvent aider à combattre le danger mais aussi préparer le terrain à une cicatrisation excessive.
Une boucle vicieuse entre les cellules de la muqueuse et les cellules immunitaires
Il s’est avéré que l’IL-8 fait plus que simplement appeler les neutrophiles. L’équipe a montré que l’IL-8 peut agir directement sur les cellules mésothéliales qui tapissent l’intérieur de l’abdomen. Exposées à l’IL-8, ces cellules libéraient des quantités accrues de TNF‑alpha, un autre signal inflammatoire puissant déjà impliqué dans la formation d’adhérences. En retour, le TNF‑alpha poussait les cellules mésothéliales à produire davantage d’IL-8, établissant une boucle auto-renforçante. Le TNF‑alpha stimulait aussi les neutrophiles à augmenter leur production de TGF‑beta1, un régulateur majeur de la fibrose qui favorise le dépôt de fibres de collagène durables. Ensemble, ces étapes dessinent un relais : IL-8 → activation des mésothéliums et libération de TNF‑alpha → activation des neutrophiles et libération de TGF‑beta1 → accumulation de tissu cicatriciel fibreux. Il est important de noter que l’IL-8 en lui-même n’a pas activé directement les gènes de la fibrose, mais il a amplifié les signaux qui le font.
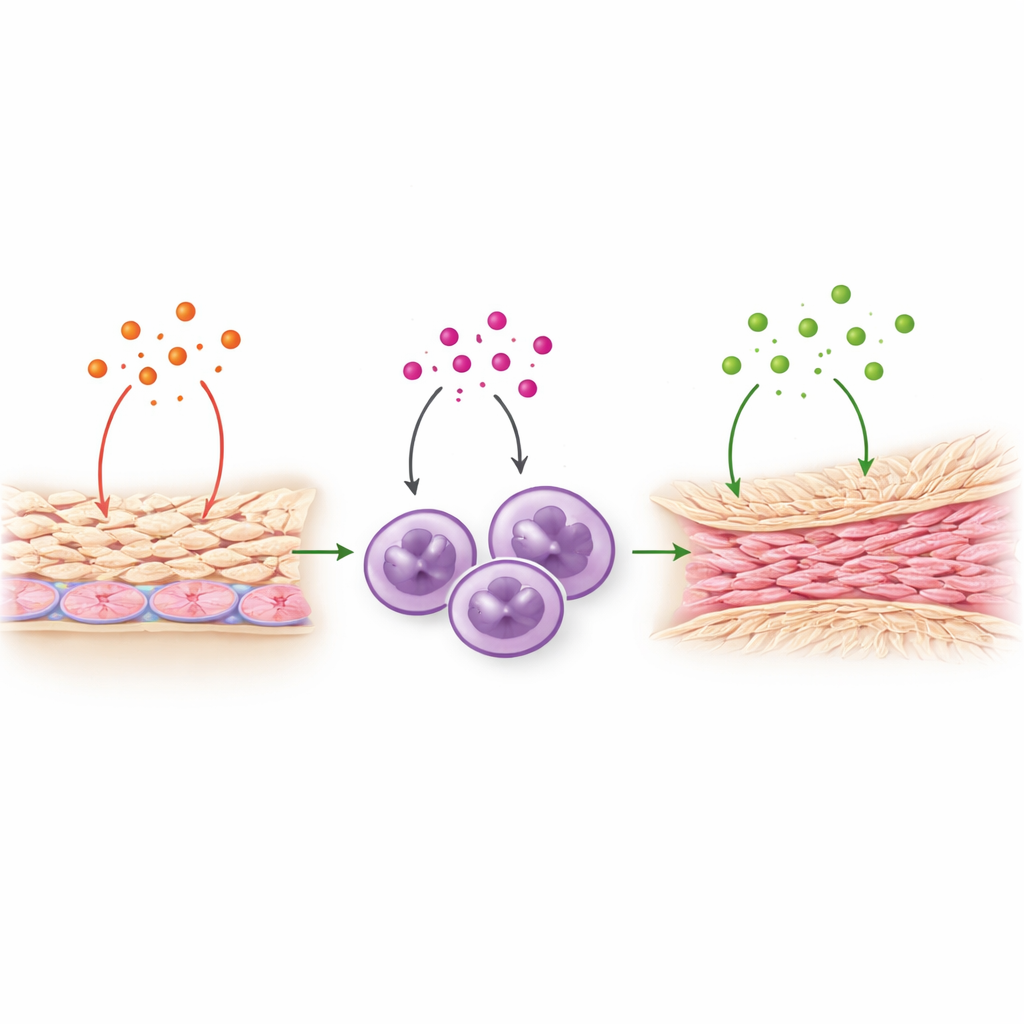
Tester un bloqueur d’IL-8 chez le singe
Pour observer le comportement de cette voie dans un organisme vivant, les chercheurs ont utilisé des singes cynomolgus soumis à une lésion standardisée de la paroi abdominale et de l’utérus pour déclencher des adhérences. Les niveaux d’IL-8 dans la paroi abdominale lésée culminaient dans les six heures suivant la chirurgie puis retombaient vers la ligne de base en l’espace d’une semaine, marquant une fenêtre précoce étroite où l’IL-8 est le plus actif. L’équipe a ensuite administré à certains singes une dose intraveineuse unique d’AMY109, un anticorps à longue action qui neutralise l’IL-8, deux jours avant l’intervention. Lors des examens 26 jours plus tard par laparoscopie, les animaux ayant reçu AMY109 présentaient des adhérences nettement moins nombreuses et de moindre taille sur la paroi abdominale que les animaux non traités. Les adhérences utérines étaient également en tendance plus légères, et chez deux singes traités elles étaient absentes, ce qui suggère qu’atténuer l’IL-8 peut protéger plusieurs sites à l’intérieur de l’abdomen sans nuire de façon évidente à la cicatrisation normale.
Ce que cela pourrait signifier pour les patients
Pris dans leur ensemble, les résultats placent l’IL-8 comme un organiseur central de l’inflammation précoce et de la fibrose ultérieure après une chirurgie abdominale. En recrutant fortement les neutrophiles et en établissant une boucle de rétroaction avec les cellules mésothéliales qui augmente le TNF‑alpha et le TGF‑beta1, l’IL-8 contribue à transformer une réponse de guérison de courte durée en bandes cicatricielles internes persistantes. Le blocage de l’IL-8 par un anticorps comme AMY109 chez le singe a réduit sensiblement ces adhérences, indiquant une stratégie médicamenteuse potentielle qui cible la biologie plutôt que de se reposer uniquement sur des barrières physiques. Si des résultats similaires sont confirmés chez l’humain, les patients pourraient un jour recevoir une courte période de traitement bloquant l’IL-8 autour du moment de la chirurgie pour réduire leur risque d’adhérences post-opératoires douloureuses et altérantes de la vie.
Citation: Nakagawa, K., Tanimura, H., Yamazaki, M. et al. IL-8 contributes to postoperative adhesion formation through the crosstalk of neutrophils and mesothelial cells. Sci Rep 16, 14221 (2026). https://doi.org/10.1038/s41598-026-42159-x
Mots-clés: adhérences post-opératoires, interleukine-8, neutrophiles, fibrose, modèle de singe