Clear Sky Science · zh
无需饲养细胞的脐带血来源自然杀伤细胞体外扩增以增强增殖与功能成熟
为什么增培养自然杀伤细胞很重要
科学家们正在加速将人体自身的免疫细胞转化为现成的癌症疗法。其中最有前景的是自然杀伤(NK)细胞,它们无需与每位患者进行个性化匹配即可识别并摧毁癌细胞。本研究探讨了如何在实验室中可靠地从脐带血中大量培养NK细胞,而不依赖辅助的“饲养”细胞,以及如何以既高效又足够经济的方式实现,为现实世界的治疗提供可能。
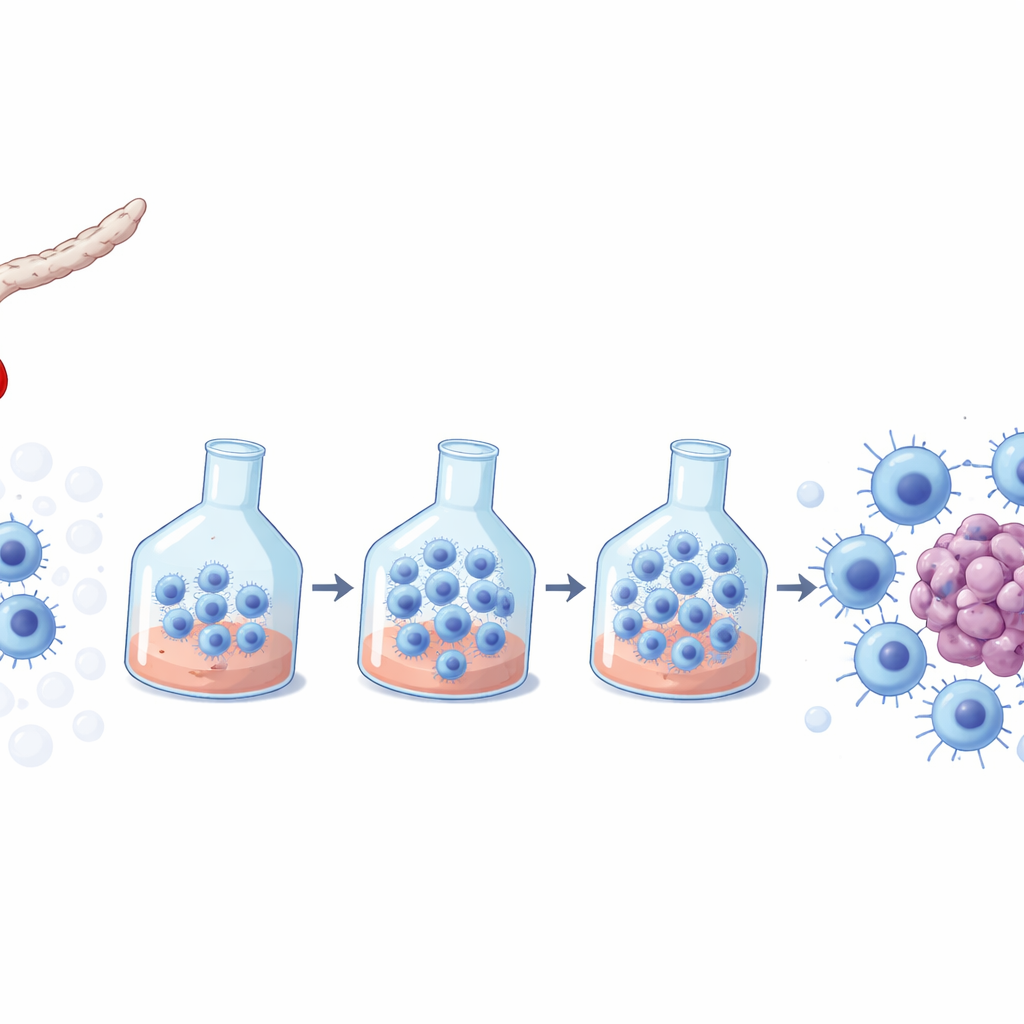
来自新生儿血液的抗癌细胞
NK细胞是免疫的前哨,能够识别并当场杀死被病毒感染或发生癌变的细胞。脐带血在分娩后从脐带收集,作为NK细胞的来源具有吸引力:获取方便、广泛存储,并且在受体中引发危险免疫反应的风险较低。然而,每单位脐带血所含NK细胞数量不足以直接用于治疗,因此必须在体外进行扩增——在体外增殖,同时保持其效力和安全性。许多商业化的NK细胞培养配方是为成人血液设计的,尚不清楚哪些配方最适合来源于脐带血的NK细胞。
测试不同的生长配方
研究人员首先用磁珠从冷冻脐带血样本中分离出富含NK的CD56阳性细胞。该过程显著提高了NK细胞的比例,但回收率不到三分之一,且引发了一定的早期细胞应激,强调了需要强效扩增方案的原因。团队随后比较了六种市售培养基,均补充了免疫信号因子白介素‑2,以评估哪种培养基在无饲养细胞条件下最能支持NK细胞生长。通过筛选,他们选择了三个条件进行深入分析:NK‑Xpander(NKX)和两种浓度不同的NK MACS(NKM1为较低补充,NKM2为较高补充)。
增殖并激活细胞
在大约四周的培养期内,NKX、NKM1和NKM2中的NK细胞均经历了一个相对平静的“滞后”期,随后进入强劲的生长期,出现细胞聚集并大量增殖。总体细胞数平均增加约15–19倍,每单位脐带血产出约2亿细胞,存活率高于90%。与此同时,它们的抗癌能力显著提升。最初,刚分离的细胞对标准白血病细胞系的杀伤力仅为中等,去颗粒(释放毒性颗粒)的迹象也有限。扩增后,三种培养基处理的NK细胞在靶细胞杀伤和去颗粒水平上都有大幅提高,表明体外扩增不仅增加了细胞数量,也功能性地激活了它们。
不同“口味”的杀伤细胞与成本问题
尽管三种培养基在总体扩增率上相似,但它们对NK细胞的塑造各有不同。在所有条件下,与攻击准备状态相关的激活性表面标志显著上升,而抑制性标志则保持相对稳定。在NKX中,与抗体依赖性细胞毒性相关的关键受体表达保持较高,保留了一部分更具攻击性的细胞群体。相比之下,NKM1和NKM2培养的细胞逐渐转向CD56亮、CD16低的表型,这种表型通常与更偏向调节和信号分泌的行为相关,而非直接杀伤。团队还进行了详细的成本分析。NKX和NKM1在每百万细胞的生产成本上相近,而NKM2由于使用了两倍的补充剂,大致将制造成本提高了一倍,但并未带来明显更优的性能。
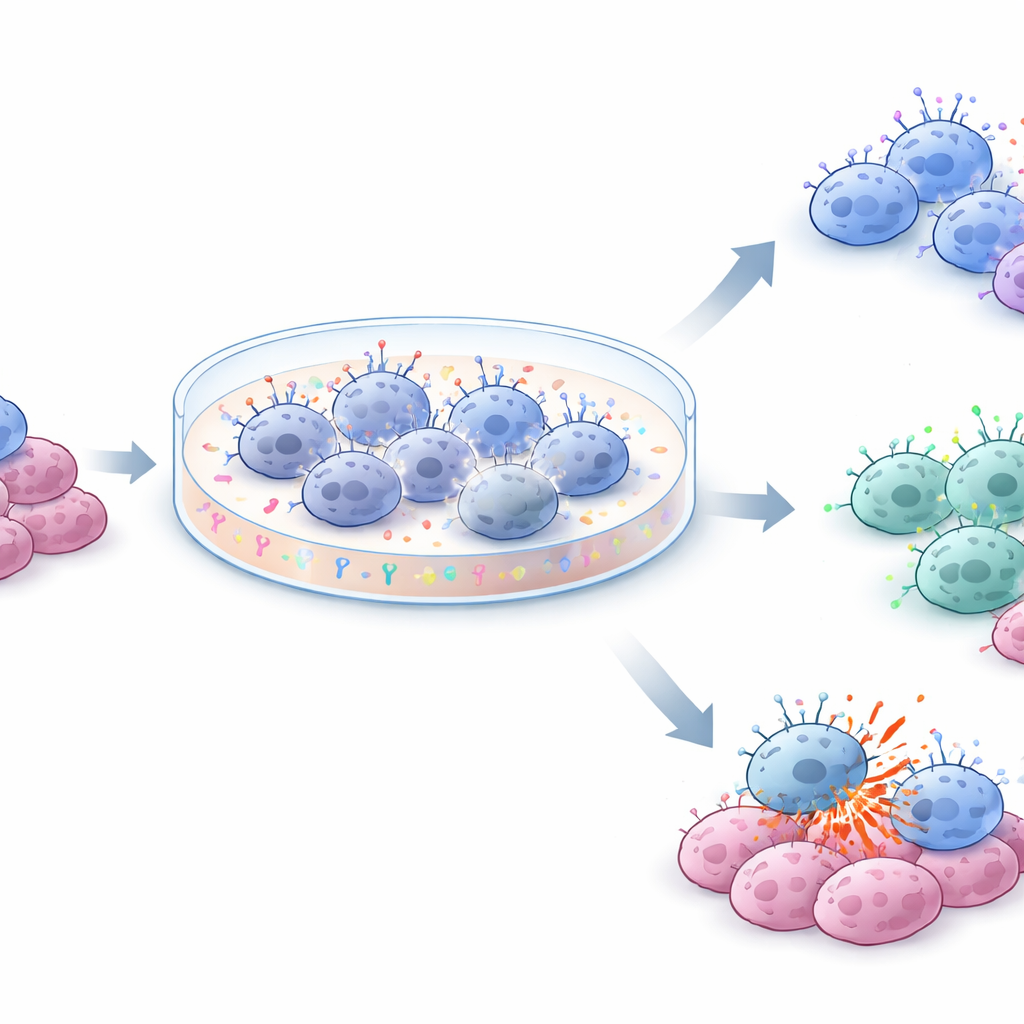
这对未来治疗意味着什么
对非专业读者来说,关键信息是:现在可以在无需复杂饲养系统的条件下体外扩增大量脐带血来源的NK细胞,同时保持其存活、活性并控制成本。NK‑Xpander在不同供体间提供了更可预测的扩增,并更好地保留了可与治疗性抗体协同作用的NK细胞,因而适合用于抗癌应用。NK MACS,尤其是在较低补充水平下,仍能有效扩增细胞,但更倾向于产生更具调节特性的NK表型,可能适合其他临床目的。总体而言,这项工作为将捐赠脐带血转化为可标准化、可规模化并可银行化、运输的现成免疫细胞产品提供了一条实用路径。
引用: Doutor, I., Costa, G., Filipe, B. et al. Feeder-free ex vivo expansion of cord blood-derived natural killer cells for enhanced proliferation and functional maturation. Sci Rep 16, 10417 (2026). https://doi.org/10.1038/s41598-026-41101-5
关键词: 脐带血, 自然杀伤细胞, 癌症免疫治疗, 细胞扩增, 现成治疗