Clear Sky Science · fr
Expansion ex vivo sans cellules nourricières de cellules NK dérivées du sang de cordon pour une prolifération et une maturation fonctionnelle améliorées
Pourquoi la culture des cellules tueuses naturelles est importante
Les scientifiques cherchent à transformer les propres cellules immunitaires du corps en traitements anticancéreux prêts à l’emploi. Parmi les plus prometteuses figurent les cellules tueuses naturelles (NK), capables d’éliminer les cellules cancéreuses sans nécessiter d’appariement personnalisé pour chaque patient. Cette étude examine comment produire de manière fiable un grand nombre de cellules NK à partir du sang de cordon ombilical en laboratoire, sans recourir à des cellules nourricières d’appoint, et comment le faire de façon suffisamment puissante et économique pour des thérapies en pratique clinique.
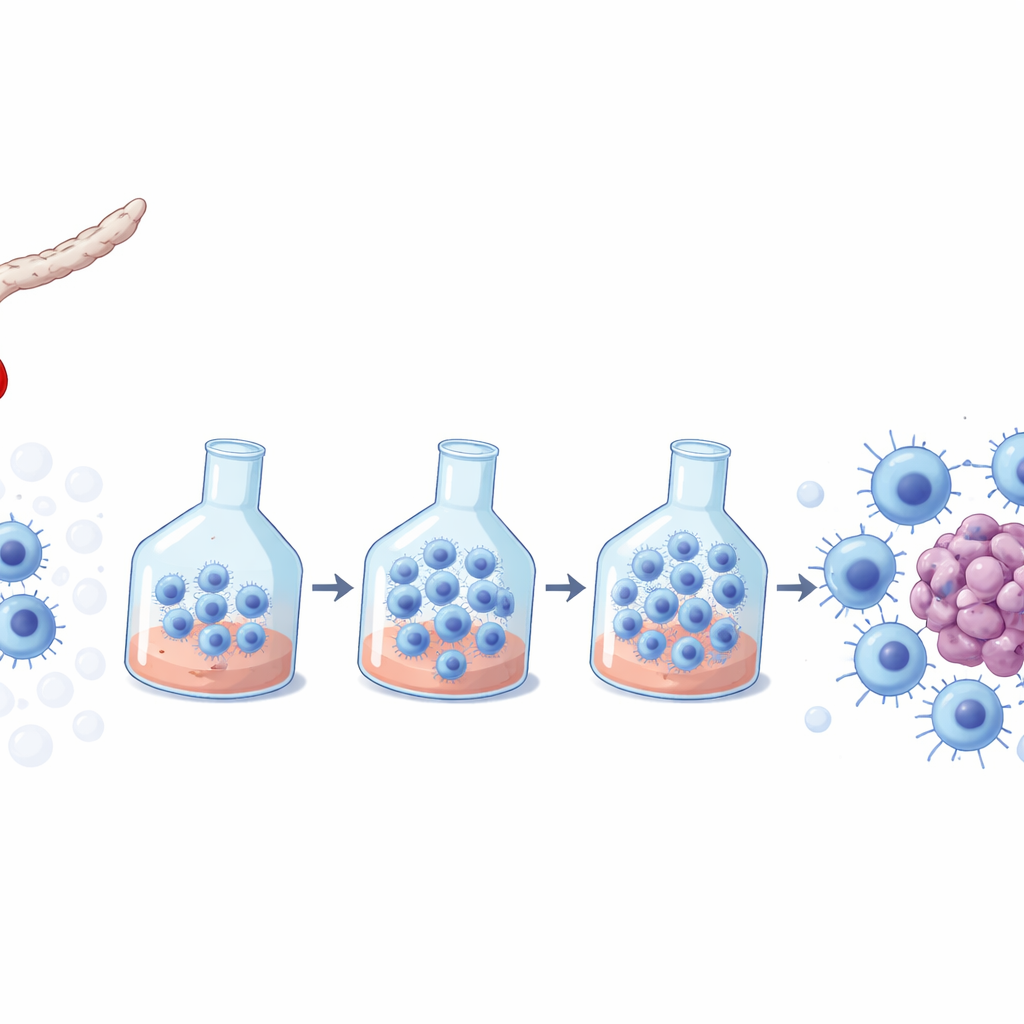
Une cellule anticancéreuse issue du sang de nouveau‑nés
Les cellules NK sont des sentinelles immunitaires capables de reconnaître et de tuer sur le champ des cellules infectées par des virus ou devenues cancéreuses. Le sang de cordon, prélevé sur le cordon ombilical après la naissance, est une source intéressante de cellules NK car il est facile à obtenir, largement stocké en banques et présente un risque réduit de déclencher des réactions immunitaires dangereuses chez le receveur. Cependant, chaque unité de sang de cordon contient trop peu de cellules NK pour traiter directement un patient ; les cellules doivent donc être multipliées ex vivo — c’est‑à‑dire cultivées hors du corps — tout en conservant leur puissance et leur sécurité. De nombreuses recettes commerciales pour la croissance des NK ont été conçues pour du sang adulte, laissant ouverte la question de celles qui soutiennent le mieux les NK dérivées du sang de cordon.
Tester différentes formules de culture
Les chercheurs ont commencé par isoler des cellules riches en NK, positives pour CD56, à partir d’échantillons de sang de cordon congelés en utilisant des billes magnétiques. Ce procédé a fortement augmenté la proportion de cellules NK mais n’a récupéré qu’un tiers d’entre elles et a provoqué un certain stress cellulaire initial, soulignant la nécessité de protocoles d’expansion robustes. L’équipe a ensuite comparé six milieux de culture commerciaux, tous complétés par le signal immunitaire interleukine‑2, pour déterminer lesquels soutiennent le mieux la croissance des NK sans cellules nourricières. De ce criblage, trois conditions ont été retenues pour une analyse approfondie : NK‑Xpander (NKX) et deux versions de NK MACS (NKM1 avec un niveau de supplément plus faible, et NKM2 avec un niveau plus élevé).
Multiplier et activer les cellules
Lorsqu’elles ont été cultivées pendant environ quatre semaines, les cellules NK en NKX, NKM1 et NKM2 ont toutes traversé une période initiale d’« inhibition » avant d’entrer dans une phase de croissance robuste où elles se sont regroupées en amas et ont multiplié leur nombre. En moyenne, le nombre total de cellules a augmenté d’environ 15 à 19 fois, produisant autour de 200 millions de cellules par unité de sang de cordon, avec une viabilité élevée supérieure à 90 %. Parallèlement, leurs capacités cytotoxiques se sont considérablement améliorées. Initialement, les cellules fraîchement isolées montraient seulement une capacité modeste à tuer une lignée leucémique standard et des signes limités de dégranulation — le processus de libération de paquets toxiques. Après expansion, les NK issues des trois milieux ont présenté une bien meilleure capacité à tuer des cellules cibles et des niveaux de dégranulation plus élevés, indiquant que le processus ex vivo n’augmentait pas seulement le nombre de cellules mais les activait fonctionnellement.
Différents profils de cellules tueuses et la question du coût
Bien que les trois milieux aient produit une expansion globale similaire, ils ont façonné les cellules NK de manières différentes. Dans toutes les conditions, un marqueur de surface activateur associé à l’état de préparation à l’attaque a fortement augmenté, tandis qu’un marqueur inhibiteur est resté relativement stable. Dans NKX, l’expression d’un récepteur clé lié à la cytotoxicité dirigée par anticorps est restée plus élevée, préservant une population de cellules plus agressivement cytotoxiques. En revanche, les cellules cultivées en NKM1 et NKM2 ont progressivement évolué vers un profil CD56‑bright, CD16‑bas, souvent associé à un comportement plus régulateur et producteur de signaux plutôt qu’à une action cytotoxique directe. L’équipe a également réalisé une analyse détaillée des coûts. NKX et NKM1 ont produit des cellules à un coût similaire par million de cellules, tandis que NKM2, qui utilisait deux fois plus de supplément, a approximativement doublé les coûts de fabrication sans fournir de performance clairement supérieure.
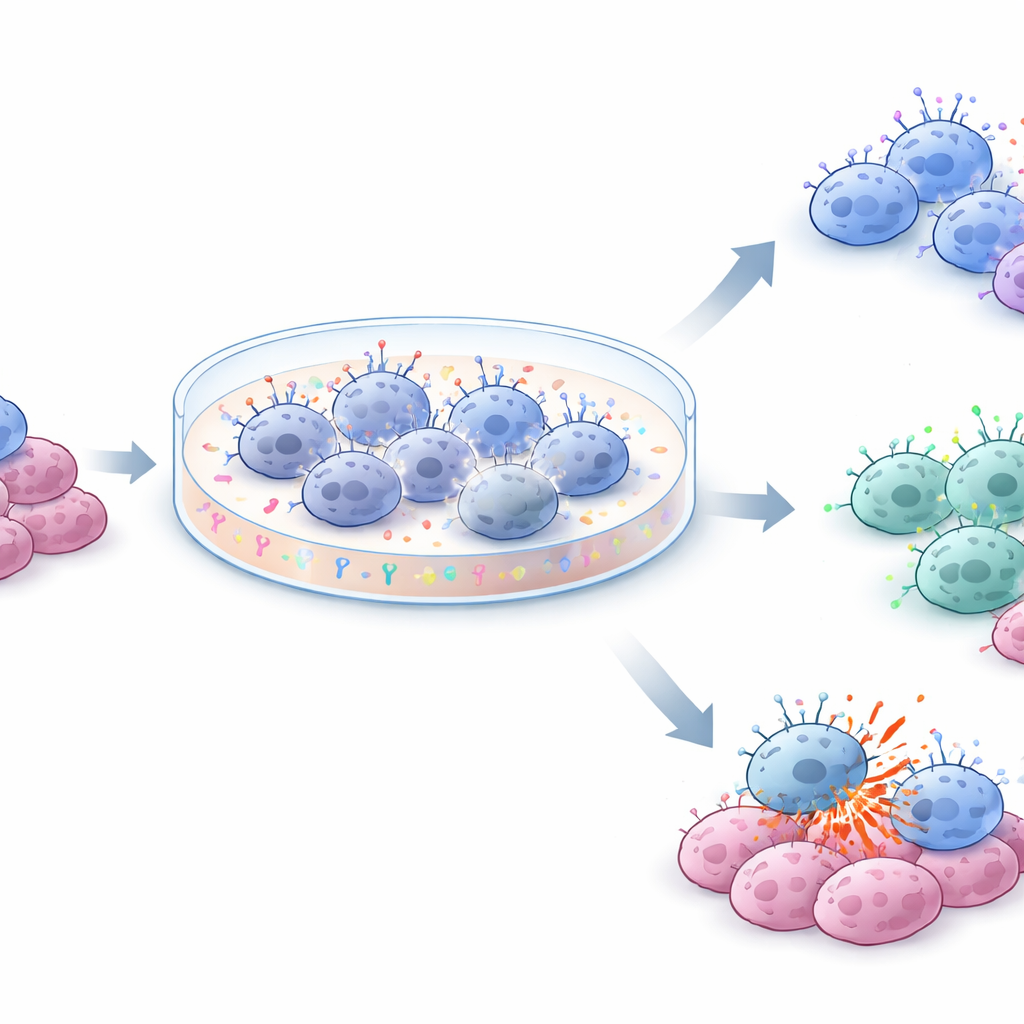
Ce que cela signifie pour les thérapies futures
Pour les lecteurs non spécialistes, le message central est qu’il est désormais possible de produire, sans systèmes nourriciers complexes, de grands lots de cellules NK dérivées du sang de cordon en laboratoire, tout en les maintenant viables, actives et relativement peu coûteuses. NK‑Xpander a offert l’expansion la plus prévisible entre donneurs et a mieux préservé des NK capables de coopérer avec des anticorps thérapeutiques, ce qui le rend bien adapté aux applications anticancéreuses. NK MACS, en particulier à faible niveau de supplément, a néanmoins permis une expansion efficace mais tendait à générer un profil NK plus orienté vers la régulation, qui pourrait convenir à d’autres objectifs cliniques. Dans l’ensemble, ce travail fournit une feuille de route pratique pour transformer le sang de cordon donné en produits standardisés et évolutifs de cellules NK pouvant être bankés et expédiés comme immunothérapies prêtes à l’emploi.
Citation: Doutor, I., Costa, G., Filipe, B. et al. Feeder-free ex vivo expansion of cord blood-derived natural killer cells for enhanced proliferation and functional maturation. Sci Rep 16, 10417 (2026). https://doi.org/10.1038/s41598-026-41101-5
Mots-clés: sang de cordon, cellules tueuses naturelles, immunothérapie du cancer, expansion cellulaire, thérapies prêtes à l’emploi