Clear Sky Science · pt
Expansão ex vivo sem alimentadores de células NK derivadas de sangue de cordão para proliferação e maturação funcional aprimoradas
Por que o crescimento de células natural killer importa
Cientistas correm para transformar as próprias células imunológicas do corpo em tratamentos contra o câncer prontos para uso. Entre as mais promissoras estão as células natural killer (NK), que podem destruir células cancerosas sem necessidade de combinação personalizada para cada paciente. Este estudo explora como cultivar de forma confiável grandes quantidades de células NK a partir do sangue de cordão umbilical no laboratório, sem depender de células “alimentadoras”, e como fazer isso de modo potente e acessível o suficiente para terapias do mundo real.
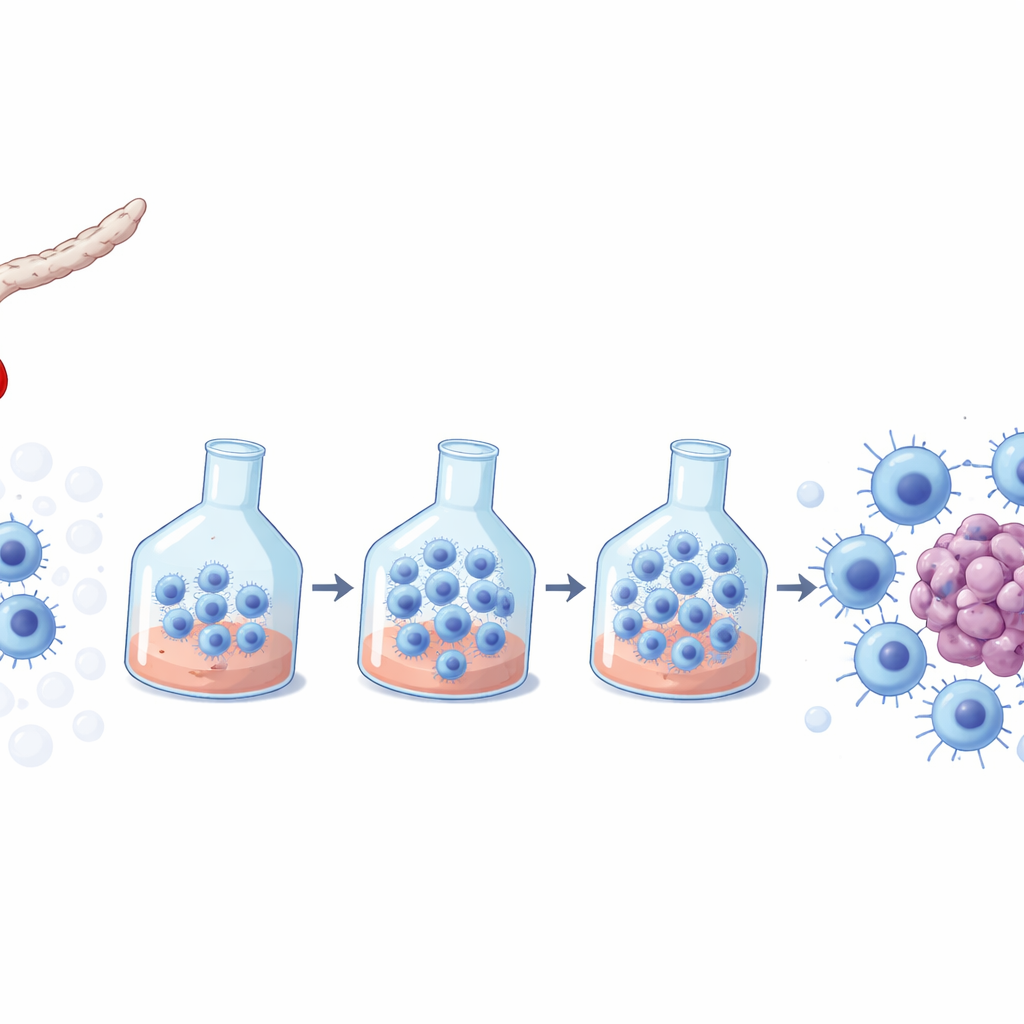
Uma célula que combate o câncer vinda do sangue de recém‑nascido
As células NK são sentinelas imunológicas capazes de reconhecer e eliminar, à primeira vista, células infectadas por vírus ou cancerosas. O sangue de cordão, coletado do cordão umbilical após o parto, é uma fonte atraente de células NK porque é fácil de obter, amplamente armazenado em bancos e apresenta menor risco de desencadear reações imunes perigosas nos receptores. No entanto, cada unidade de sangue de cordão contém poucas células NK para tratar um paciente diretamente, por isso elas precisam ser multiplicadas ex vivo — crescidas fora do corpo — mantendo‑as potentes e seguras. Muitas receitas comerciais para crescimento de NK foram desenhadas para sangue adulto, deixando em aberto a questão de quais melhor sustentam as células derivadas de sangue de cordão.
Testando diferentes “receitas” de cultivo
Os pesquisadores começaram isolando células ricas em NK positivas para CD56 a partir de amostras de sangue de cordão congeladas usando partículas magnéticas. Esse processo aumentou bastante a proporção de NK, mas recuperou menos de um terço das células e causou algum estresse celular inicial, ressaltando por que são necessários protocolos de expansão robustos. A equipe então comparou seis meios de cultura comerciais, todos suplementados com a sinalização imune interleucina‑2, para ver qual sustentaria melhor o crescimento de NK sem alimentadores. A partir dessa triagem, selecionaram três condições para análise aprofundada: NK‑Xpander (NKX) e duas versões do NK MACS (NKM1 com nível menor de suplemento e NKM2 com nível maior).
Multiplicando e ativando as células
Quando cultivadas por cerca de quatro semanas, as células NK em NKX, NKM1 e NKM2 passaram por um período inicial de adaptação antes de entrarem em uma fase de crescimento robusto, formando aglomerados e se multiplicando. Em média, o número total de células aumentou aproximadamente de 15 a 19 vezes, gerando cerca de 200 milhões de células por unidade de sangue de cordão, com alta viabilidade acima de 90%. Ao mesmo tempo, sua capacidade de matar células cancerosas melhorou dramaticamente. Inicialmente, células recém‑isoladas mostraram apenas capacidade modesta para eliminar uma linhagem padrão de leucemia e sinais limitados de desgranulação — o processo de liberar pacotes tóxicos. Após a expansão, as células NK dos três meios exibiram muito mais capacidade de matar células‑alvo e níveis mais altos de desgranulação, indicando que o processo ex vivo não só aumentou o número de células como também as ativou funcionalmente.
Diferentes perfis de células assassinas e a questão do custo
Embora os três meios tenham produzido expansão global semelhante, eles moldaram as células NK de maneiras diferentes. Em todas as condições, um marcador de superfície ativador associado à prontidão para atacar aumentou acentuadamente, enquanto um marcador inibitório permaneceu relativamente estável. No NKX, a expressão de um receptor chave ligado à citotoxicidade mediada por anticorpos permaneceu mais alta, preservando uma população de células mais agressivamente citotóxicas. Em contraste, células cultivadas em NKM1 e NKM2 deslocaram‑se gradualmente para um perfil CD56‑brilhante, CD16‑baixo, frequentemente associado a comportamento mais regulatório e produtor de sinais em vez de ataque direto. A equipe também realizou uma análise detalhada de custos. NKX e NKM1 produziram células com custo por milhão semelhante, enquanto NKM2, que usou o dobro de suplemento, aproximadamente dobrou os custos de fabricação, sem oferecer desempenho claramente superior.
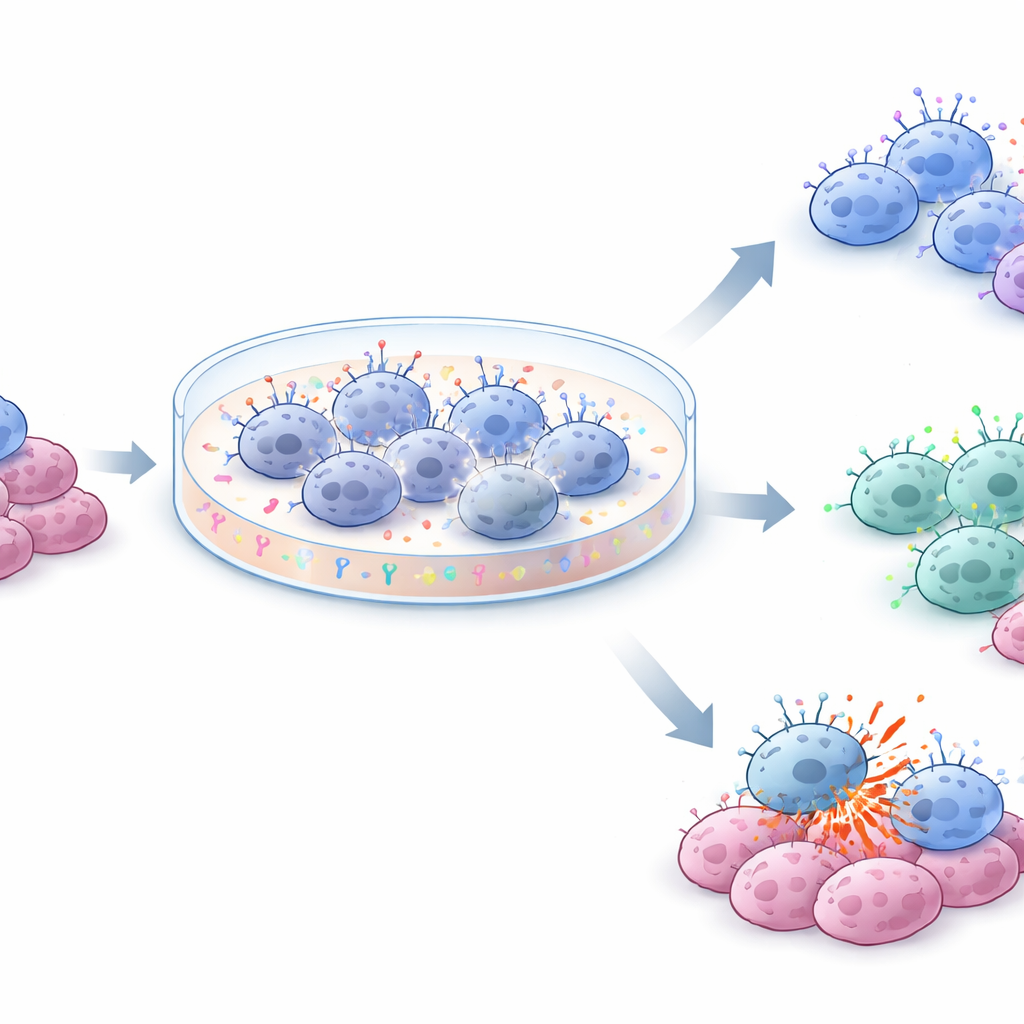
O que isso significa para terapias futuras
Para leitores não especializados, a mensagem principal é que agora é viável cultivar grandes lotes de células NK derivadas de sangue de cordão no laboratório sem sistemas complexos de alimentadores, mantendo‑as vivas, ativas e relativamente baratas. O NK‑Xpander ofereceu a expansão mais previsível entre diferentes doadores e preservou melhor células NK que podem atuar em conjunto com anticorpos terapêuticos, tornando‑o bem adequado para aplicações de combate ao câncer. O NK MACS, particularmente com níveis inferiores de suplemento, ainda expandiu as células de forma eficaz, mas tendia a gerar um perfil NK mais regulatório que pode ser adequado a outros objetivos clínicos. No geral, este trabalho fornece um roteiro prático para transformar sangue de cordão doado em produtos padronizados e escaláveis de células NK que podem ser bancados e enviados como imunoterapias prontas para uso.
Citação: Doutor, I., Costa, G., Filipe, B. et al. Feeder-free ex vivo expansion of cord blood-derived natural killer cells for enhanced proliferation and functional maturation. Sci Rep 16, 10417 (2026). https://doi.org/10.1038/s41598-026-41101-5
Palavras-chave: sangue de cordão, células natural killer, imunoterapia contra o câncer, expansão celular, terapias prontas para uso