Clear Sky Science · nl
Voeder‑vrije ex vivo expansie van uit navelstrengbloed afkomstige natural killer‑cellen voor verbeterde proliferatie en functionele rijping
Waarom het kweken van natural killer‑cellen ertoe doet
Wetenschappers strijden om de eigen immuuncellen van het lichaam om te vormen tot kant‑klaar behandelingen tegen kanker. Een van de veelbelovende kandidaten zijn natural killer (NK)‑cellen, die kankercellen kunnen vernietigen zonder per patiënt precies afgestemd te hoeven zijn. Deze studie onderzoekt hoe je op betrouwbare wijze grote aantallen NK‑cellen uit navelstrengbloed in het laboratorium kunt vermeerderen, zonder afhankelijk te zijn van helper‑“feeder”cellen, en hoe dat op een manier kan die zowel krachtig als betaalbaar genoeg is voor praktische therapieën.
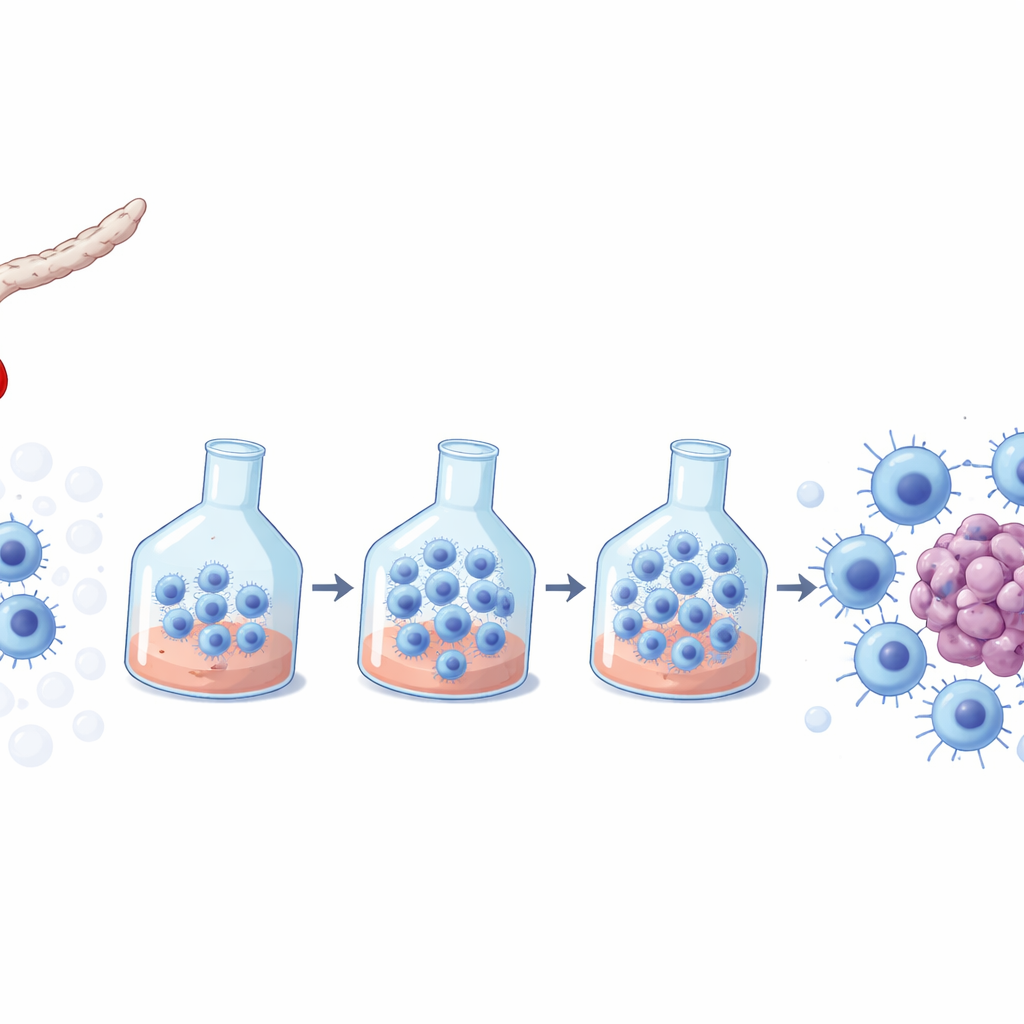
Een kankerverdelgende cel uit pasgeboren bloed
NK‑cellen zijn immuunsentinels die virusgeïnfecteerde of kankercellen direct kunnen herkennen en doden. Navelstrengbloed, verzameld uit de navelstreng na de geboorte, is een aantrekkelijke bron van NK‑cellen omdat het gemakkelijk te verkrijgen, veelvuldig gebankt en minder geneigd is om gevaarlijke immuunreacties bij ontvangers te veroorzaken. Toch bevat elke eenheid navelstrengbloed te weinig NK‑cellen om een patiënt direct te behandelen, dus moeten de cellen ex vivo — buiten het lichaam — worden vermeerderd, terwijl ze krachtig en veilig blijven. Veel commerciële protocollen voor NK‑celgroei zijn ontworpen voor volwassen bloed, waardoor de vraag blijft welke protocollen het beste cord‑blood‑afgeleide NK‑cellen ondersteunen.
Verschillende kweekrecepten testen
De onderzoekers begonnen met het isoleren van NK‑rijke CD56‑positieve cellen uit ingevroren navelstrengbloedmonsters met magnetische kralen. Dit vergrootte het aandeel NK‑cellen aanzienlijk, maar leverde minder dan een derde van de oorspronkelijke cellen terug en veroorzaakte wat vroege celstress, wat benadrukt waarom sterke expansieprotocollen nodig zijn. Het team vergeleek vervolgens zes commercieel verkrijgbare kweekmedia, allemaal versterkt met de immuunstimulerende factor interleukine‑2, om te zien welke het beste feeder‑vrije NK‑celgroei zouden ondersteunen. Uit deze screening selecteerden ze drie condities voor diepgaander analyse: NK‑Xpander (NKX) en twee versies van NK MACS (NKM1 met een lager supplementniveau, en NKM2 met een hoger niveau).
De cellen vermenigvuldigen en activeren
Bij kweek gedurende ongeveer vier weken doorliepen NK‑cellen in NKX, NKM1 en NKM2 eerst een rustige “latente” fase voordat ze een robuuste groeifase ingingen waarin ze clusters vormden en vermenigvuldigden. Gemiddeld namen de totale celaantallen zo’n 15–19‑voud toe, wat ruwweg 200 miljoen cellen per navelstrengbloedunit opleverde, met een hoge vitaliteit boven 90%. Tegelijkertijd verbeterde hun kankerdodende vermogen aanzienlijk. Aanvankelijk vertoonden vers geïsoleerde cellen slechts een bescheiden capaciteit om een standaard leukemiecellenlijn te doden en beperkte tekenen van degranulatie — het proces van het loslaten van toxische pakketjes. Na expansie toonden NK‑cellen uit alle drie de media veel sterkere doelcel‑doding en hogere degranulatie‑niveaus, wat aangeeft dat het ex vivo proces niet alleen het aantal cellen verhoogde maar ze ook functioneel activeerde.
Verschillende types killer‑cellen en de kostenvraag
Hoewel de drie media vergelijkbare totale expansie produceerden, vormden ze de NK‑cellen op verschillende manieren. In alle condities steeg een activerend oppervlaktemarker dat geassocieerd is met paraatheid om aan te vallen sterk, terwijl een remmende marker relatief stabiel bleef. In NKX bleef de expressie van een belangrijke receptor die gekoppeld is aan antilichaam‑gerichte doding hoger, waardoor een populatie van agressiever cytotoxische cellen behouden bleef. Daarentegen verschoven cellen gekweekt in NKM1 en NKM2 geleidelijk naar een CD56‑bright, CD16‑laag profiel dat vaak geassocieerd wordt met meer regulerende, signaalproducerende functies in plaats van directe doding. Het team voerde ook een gedetailleerde kostenanalyse uit. NKX en NKM1 produceerden cellen tegen vergelijkbare kosten per miljoen, terwijl NKM2, dat twee keer zoveel supplement gebruikte, de productiekosten grofweg verdubbelde zonder duidelijk betere prestaties te leveren.
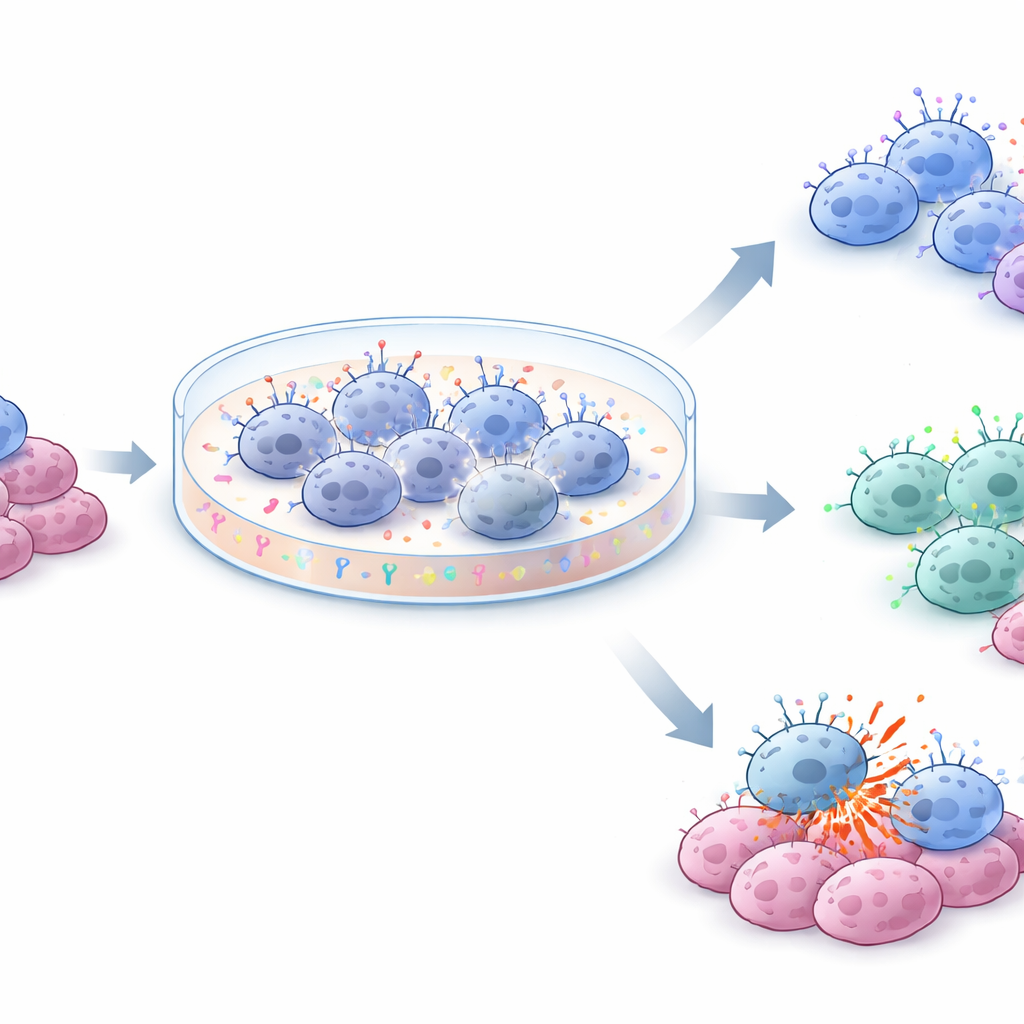
Wat dit betekent voor toekomstige therapieën
Voor niet‑specialistische lezers is de kernboodschap dat het nu haalbaar is om grote batches van uit navelstrengbloed afkomstige NK‑cellen in het laboratorium te kweken zonder complexe feeder‑systemen, terwijl ze levensvatbaar, actief en relatief goedkoop blijven. NK‑Xpander bood de meest voorspelbare expansie over verschillende donoren en behield beter NK‑cellen die goed samenwerken met therapeutische antilichamen, waardoor het goed geschikt is voor kankerbestrijdende toepassingen. NK MACS, vooral bij lagere supplementniveaus, breidde de cellen nog steeds effectief uit maar neigde ertoe een meer regulerend‑achtig NK‑profiel te genereren dat mogelijk bij andere klinische doelen past. Al met al biedt dit werk een praktisch stappenplan om gedoneerd navelstrengbloed om te zetten in gestandaardiseerde, schaalbare NK‑celproducten die gebankt en verzonden kunnen worden als kant‑klaar immunotherapieproducten.
Bronvermelding: Doutor, I., Costa, G., Filipe, B. et al. Feeder-free ex vivo expansion of cord blood-derived natural killer cells for enhanced proliferation and functional maturation. Sci Rep 16, 10417 (2026). https://doi.org/10.1038/s41598-026-41101-5
Trefwoorden: navelstrengbloed, natural killer‑cellen, kankerimmunotherapie, celexpansie, kant‑klaar therapieën