Clear Sky Science · it
Espansione ex vivo senza feeder di cellule natural killer derivate da sangue cordonale per una maggiore proliferazione e maturazione funzionale
Perché è importante far crescere le Natural Killer
Gli scienziati corrono per trasformare le cellule immunitarie del corpo in terapie contro il cancro pronte all'uso. Tra le più promettenti ci sono le cellule natural killer (NK), capaci di distruggere le cellule tumorali senza necessitare di una corrispondenza personalizzata per ogni paziente. Questo studio esplora come ottenere in modo affidabile grandi quantità di NK dal sangue cordonale in laboratorio, senza ricorrere a cellule “feeder” di supporto, e come farlo in modo potente e sufficientemente economico per applicazioni cliniche reali.
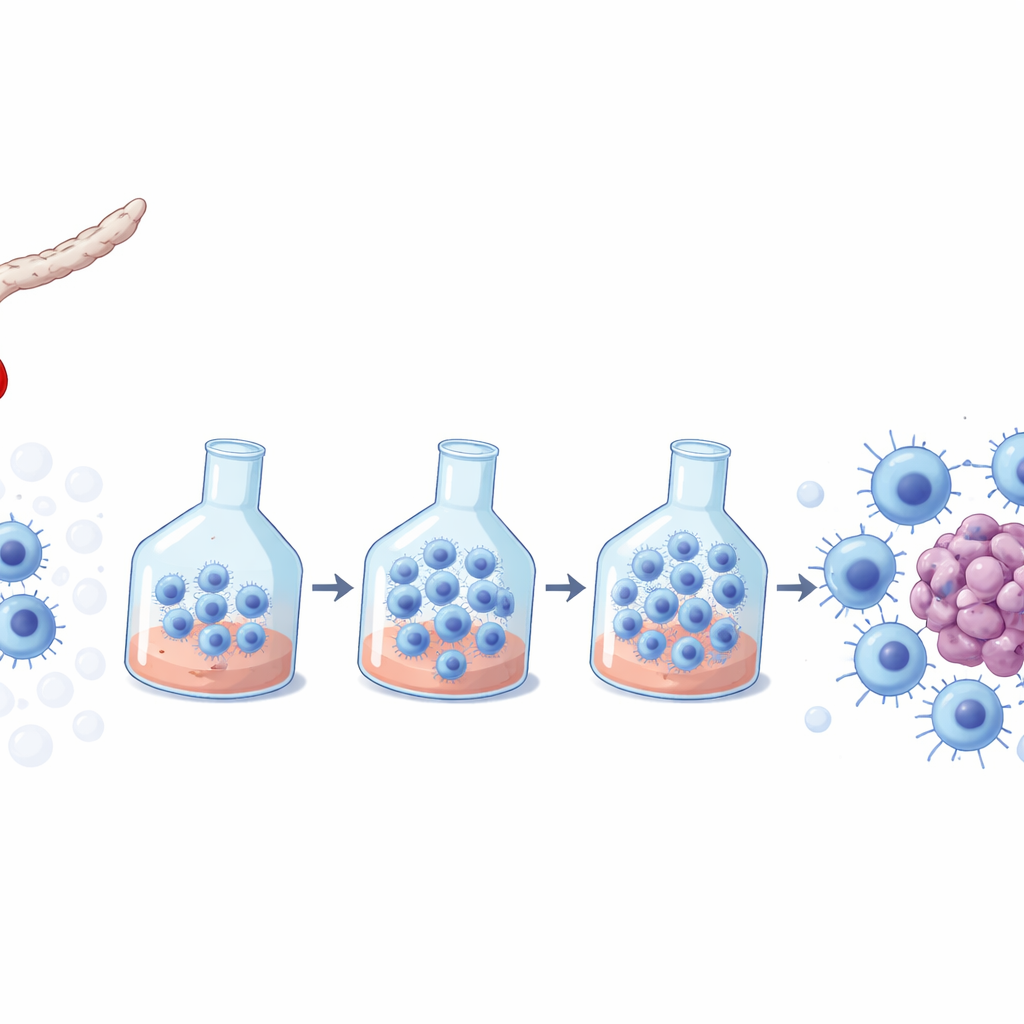
Una cellula che combatte il cancro dal sangue dei neonati
Le cellule NK sono sentinelle immunitarie che possono riconoscere e uccidere cellule infette da virus o tumorali. Il sangue cordonale, raccolto dal cordone ombelicale dopo la nascita, è una fonte attraente di NK perché è facilmente ottenibile, ampiamente conservato in banche e comporta un rischio minore di provocare reazioni immunitarie pericolose nei riceventi. Tuttavia, ogni unità di sangue cordonale contiene troppe poche NK per trattare direttamente un paziente, quindi le cellule devono essere moltiplicate ex vivo — cresciute fuori dal corpo — mantenendole potenti e sicure. Molte ricette commerciali per la crescita delle NK sono state concepite per sangue adulto, lasciando aperta la domanda su quali siano le migliori per supportare le NK derivate da sangue cordonale.
Testare diverse ricette di crescita
I ricercatori hanno iniziato isolando cellule ricche di NK positive per CD56 da campioni di sangue cordonale congelato usando perle magnetiche. Questo processo ha aumentato molto la percentuale di NK ma ha recuperato meno di un terzo delle cellule e ha causato un certo stress cellulare iniziale, evidenziando perché sono necessari protocolli di espansione robusti. Il team ha quindi confrontato sei terreni di coltura commerciali, tutti potenziati con il segnale immune interleuchina‑2, per vedere quale supportasse meglio la crescita delle NK senza feeder. Da questo screening hanno selezionato tre condizioni per un'analisi più approfondita: NK‑Xpander (NKX) e due versioni di NK MACS (NKM1 con livello di supplemento più basso e NKM2 con livello più alto).
Moltiplicare e potenziare le cellule
Coltivate per circa quattro settimane, le NK in NKX, NKM1 e NKM2 hanno tutte attraversato un periodo iniziale di “latenza” prima di entrare in una fase di crescita robusta in cui formavano ammassi e si moltiplicavano. In media, il numero totale di cellule è aumentato circa 15–19 volte, producendo intorno a 200 milioni di cellule per unità di sangue cordonale, con una viabilità elevata superiore al 90%. Allo stesso tempo, le loro capacità di uccidere il cancro sono migliorate notevolmente. Inizialmente, le cellule appena isolate mostravano solo una capacità modesta di uccidere una linea cellulare leucemica di riferimento e segni limitati di degranulazione — il rilascio di pacchetti tossici. Dopo l'espansione, le NK di tutti e tre i terreni hanno mostrato un'azione di uccisione dei bersagli molto più forte e livelli più elevati di degranulazione, indicando che il processo ex vivo non solo ha aumentato il numero di cellule ma le ha anche attivate funzionalmente.
Diversi profili di cellule killer e la questione dei costi
Sebbene i tre terreni abbiano prodotto un'espansione complessiva simile, hanno plasmato le NK in modi diversi. In tutte le condizioni, un marcatore di superficie attivante associato alla prontezza ad attaccare è aumentato nettamente, mentre un marcatore inibitorio è rimasto relativamente stabile. In NKX, l'espressione di un recettore chiave legato all'uccisione mediata da anticorpi è rimasta più alta, preservando una popolazione di cellule più citotossiche. Al contrario, le cellule coltivate in NKM1 e NKM2 si sono gradualmente spostate verso un profilo CD56‑bright, CD16‑low spesso associato a un comportamento più regolatorio e produttore di segnali piuttosto che a un'uccisione diretta. Il team ha anche condotto un'analisi dettagliata dei costi. NKX e NKM1 hanno prodotto cellule a costi simili per milione, mentre NKM2, che utilizzava il doppio del supplemento, ha quasi raddoppiato i costi di produzione senza fornire prestazioni chiaramente superiori.
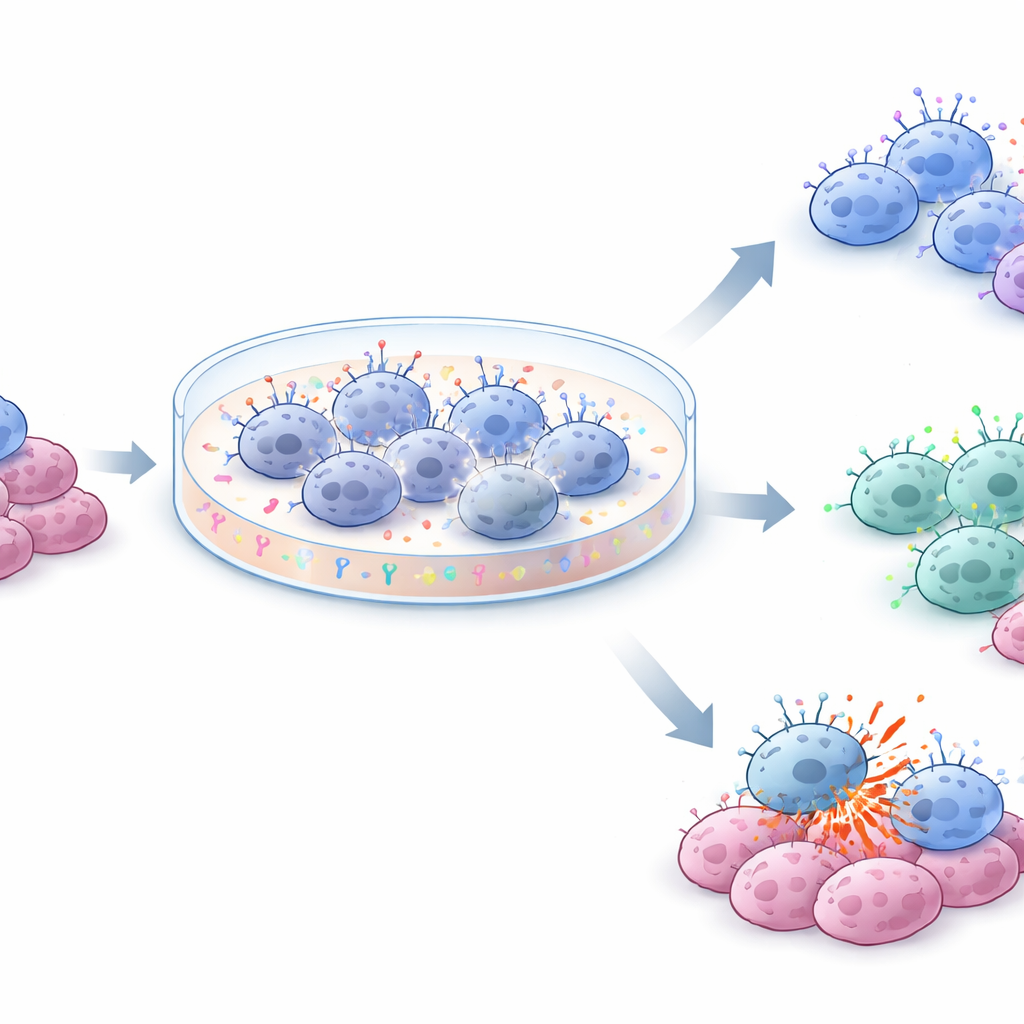
Cosa significa per le terapie future
Per i lettori non specialisti, il messaggio chiave è che ora è fattibile coltivare grandi lotti di NK derivate dal sangue cordonale in laboratorio senza sistemi feeder complessi, mantenendole vive, attive e relativamente poco costose. NK‑Xpander ha offerto l'espansione più prevedibile tra donatori diversi e ha meglio preservato le NK in grado di lavorare in sinergia con anticorpi terapeutici, rendendolo ben adatto ad applicazioni antitumorali. NK MACS, particolarmente a livelli di supplemento più bassi, ha comunque espanso efficacemente le cellule ma tendeva a generare un profilo NK più regolatorio che potrebbe adattarsi ad altri obiettivi clinici. Nel complesso, questo lavoro fornisce una road map pratica per trasformare il sangue cordonale donato in prodotti NK standardizzati e scalabili che potrebbero essere conservati in banca e spediti come immunoterapie pronte all'uso.
Citazione: Doutor, I., Costa, G., Filipe, B. et al. Feeder-free ex vivo expansion of cord blood-derived natural killer cells for enhanced proliferation and functional maturation. Sci Rep 16, 10417 (2026). https://doi.org/10.1038/s41598-026-41101-5
Parole chiave: sangue cordonale, cellule natural killer, immunoterapia del cancro, espansione cellulare, terapie pronte all'uso